Clear Sky Science · it
La metilazione del DNA e gli lncRNA controllano la replicazione asincrona del DNA in domini genici imprintati specifici
Perché conta il programma di copia del DNA della cellula
Ogni volta che una cellula si divide deve copiare l’intero DNA, ma non tutte le regioni vengono duplicate nello stesso momento. Alcuni tratti vengono copiati precocemente, altri più tardi, seguendo un preciso “orario” genomico. Questo articolo esplora perché, in alcuni particolari agglomerati genici che conservano la memoria dell’origine parentale, le copie materne e paterne vengono replicate in momenti diversi. Comprendere questa tempistica insolita aiuta a spiegare come marchi chimici sul DNA e lunghi RNA non codificanti (lncRNA) contribuiscano a organizzare il genoma e possano influenzare sviluppo e malattie.
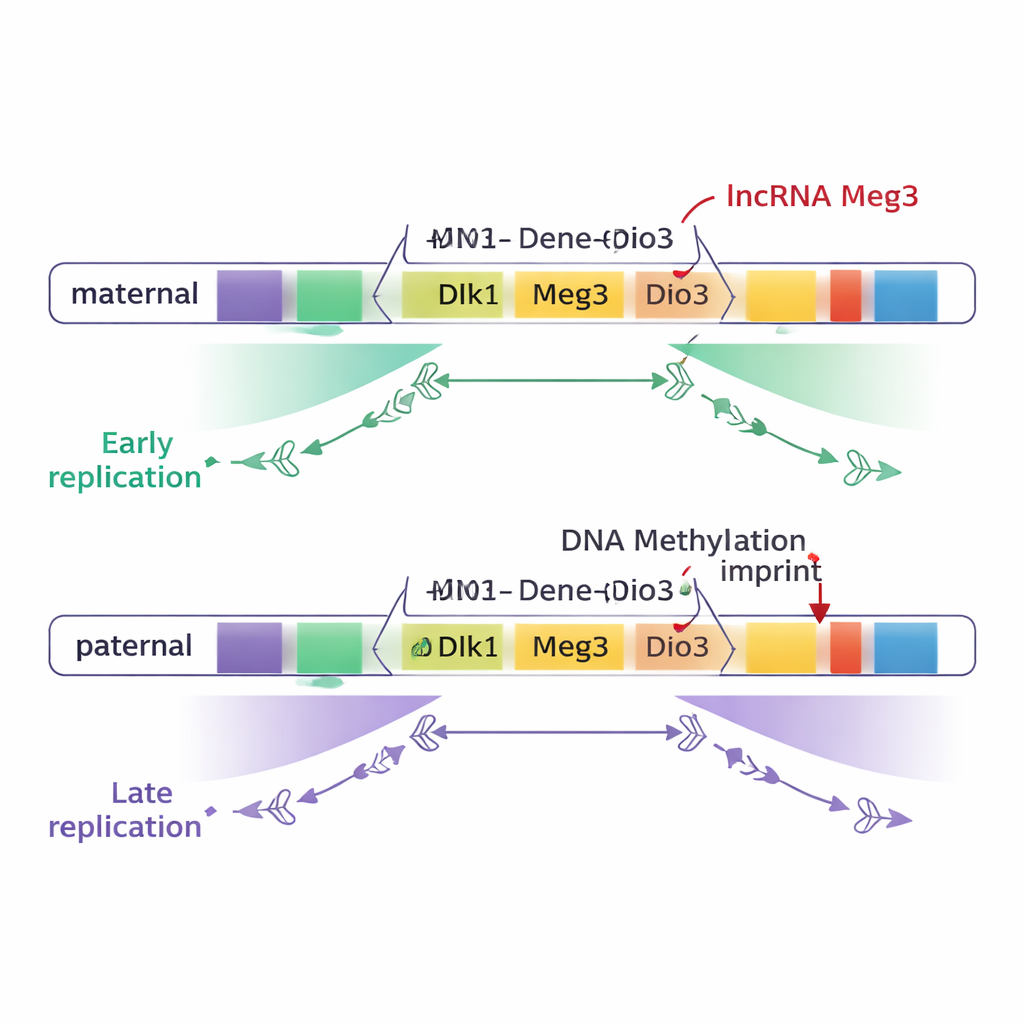
Memorie parentali scritte sul DNA
Nei mammiferi, un piccolo numero di domini genici “imprintati” si comporta diversamente a seconda che sia ereditato dalla madre o dal padre. Questo effetto dipendente dall’origine parentale è regolato dalla metilazione del DNA—piccoli marchi chimici aggiunti in regioni specifiche note come regioni differenzialmente metilate (DMR)—e da cambiamenti nel ripiegamento dei cromosomi. Gli autori hanno studiato cellule staminali embrionali di topo, che assomigliano a cellule dell’embrione molto precoce. Hanno confrontato cellule con solo genomi materni, solo genomi paterni e ibridi normali che portavano uno di ciascuno. Tracciando quando frammenti di DNA venivano copiati durante il ciclo cellulare, hanno mappato la tempistica di replicazione attraverso il genoma e si sono concentrati su regioni imprintate note.
Due regioni imprintate che infrangono le regole
La maggior parte del genoma, incluse la maggior parte delle regioni imprintate, risultava replicarsi nello stesso momento su cromosomi materni e paterni. Tuttavia, due grandi domini imprintati spiccavano: il dominio Dlk1–Dio3 sul cromosoma 12 e la regione Snrpn sul cromosoma 7. In queste zone, un ampio tratto di DNA—circa tre quarti di milione di paia di basi nel Dlk1–Dio3—veniva copiato precocemente su un cromosoma parentale e tardi sull’altro. Crucialmente, questa differenza seguiva l’origine parentale, non lo sfondo di ceppo: la copia materna di geni chiave come Dlk1 e del gene lncRNA Meg3 replicava consistentemente in anticipo, mentre le copie paterne replicavano in ritardo.
La metilazione del DNA fissa l’interruttore temporale
Per verificare cosa causasse questa differenza di tempistica, i ricercatori hanno ingegnerizzato cellule staminali in cui il normale schema di metilazione alle DMR veniva o cancellato o forzato su entrambi i cromosomi parentali. Quando entrambe le copie parentali delle DMR del Dlk1–Dio3 erano metilate, l’intera regione replicava tardi su entrambi i cromosomi. Quando la metilazione veniva in larga parte rimossa da entrambe le copie, la stessa regione replicava precocemente su entrambe. Esperimenti simili su Snrpn hanno prodotto anch’essi una perdita delle differenze di tempistica. Questi risultati mostrano che la metilazione specifica per parentela è essenziale per creare il contrasto precocemente-verso-tardi nella replicazione tra cromosomi materni e paterni, almeno in questi due domini.
Un lungo RNA regola finemente la replicazione precoce
Tuttavia la metilazione del DNA non era tutta la storia. Il dominio Dlk1–Dio3 produce anche un lungo RNA non codificante chiamato Meg3 come parte di un ampio “polycistrone” di RNA. Sul cromosoma materno, le DMR non metilate permettono l’espressione di Meg3; sul cromosoma paterno, la metilazione lo mantiene silente. Creando cancellazioni precise che spegnevano Meg3 lasciando intatta la metilazione del DNA, gli autori hanno mostrato che la perdita dell’RNA Meg3 causava lo spostamento di parti specifiche del dominio materno da una replicazione precoce verso una più tardiva. In altre parole, l’RNA Meg3 contribuisce a promuovere la copia precoce in tratti vicini del cromosoma materno, aggiungendo un secondo livello di controllo oltre la metilazione del DNA.
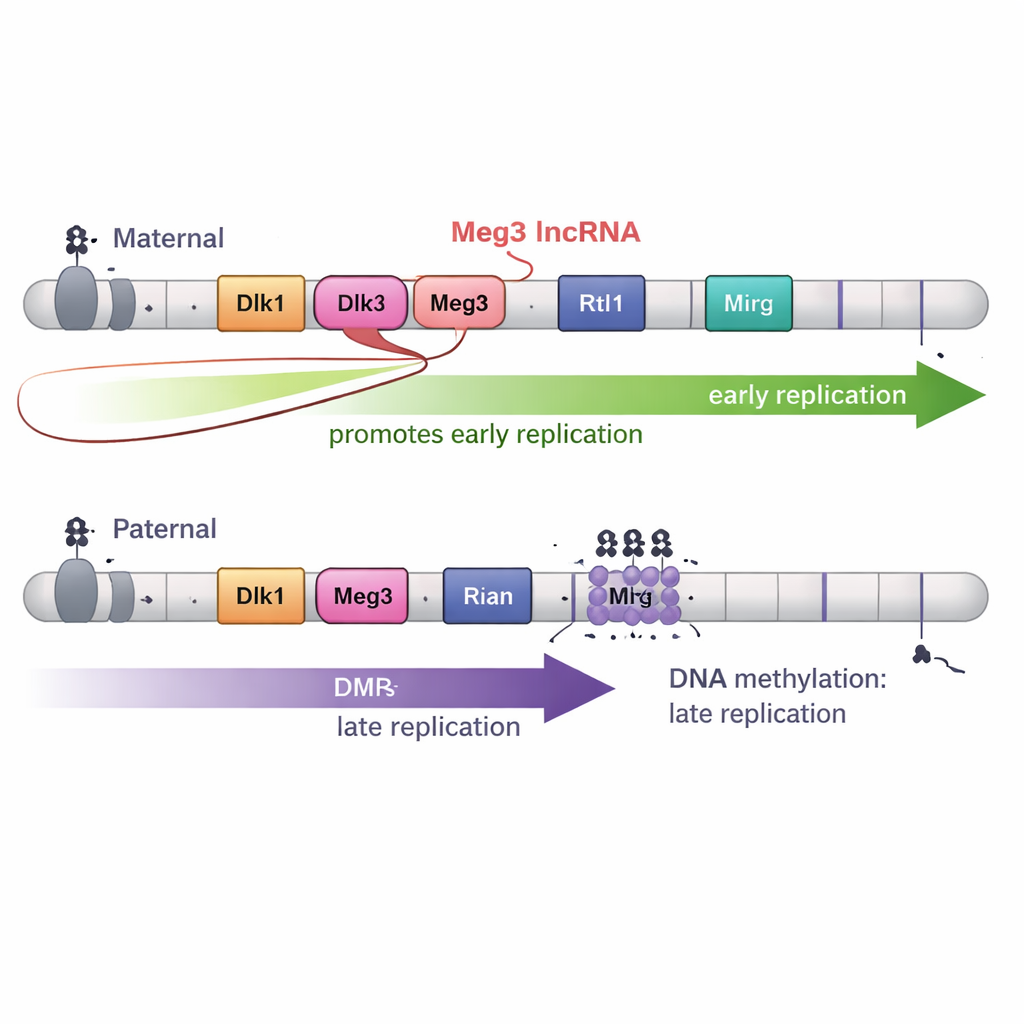
Il ripiegamento 3D e lo sviluppo aggiungono ulteriori complessità
Poiché il ripiegamento del genoma è spesso legato alla tempistica di replicazione, il team ha anche mappato l’architettura cromosomica 3D in dettaglio. Sorprendentemente, nel dominio Dlk1–Dio3 i confini delle unità 3D non coincidevano con i limiti di replicazione precoce e tardiva. Anche quando gli schemi di metilazione venivano alterati e la tempistica di replicazione cambiava, le unità di ripiegamento di base—i domini di associazione topologica—si spostavano in modi diversi. Infine, quando le cellule staminali venivano differenziate in progenitori neurali, le marcate differenze di tempistica tra copie materne e paterne scomparivano in gran parte, sebbene i marchi di imprinting e molti aspetti della struttura 3D rimanessero. Questo suggerisce che segnali dello sviluppo possono sovrascrivere il particolare schema precoce-verso-tardi osservato nelle cellule staminali.
Cosa significa in termini semplici
Questo studio rivela che, in alcuni speciali quartieri genici che ricordano da quale genitore provengono, il programma di copia del DNA della cellula è controllato da una combinazione di marchi chimici sul DNA e da lunghi RNA non codificanti. La metilazione del DNA nelle regioni di controllo imprintate stabilisce un’impostazione di base precoce-o-tardi per ciascun cromosoma parentale, e l’lncRNA Meg3 spinge ulteriormente il DNA materno vicino a replicarsi prima. Questi effetti agiscono in gran parte indipendentemente dal modo in cui il cromosoma si ripiega in 3D. Durante lo sviluppo, man mano che le cellule si specializzano, questa tempistica insolita si attenua, mostrando che è una caratteristica dello stato pluripotente delle cellule staminali. Nel complesso, il lavoro spiega come le “memorie” epigenetiche parentali e gli RNA non codificanti possano localmente sovrascrivere il normale orario di replicazione del genoma.
Citazione: Imaizumi, Y., Charon, F., Surcis, C. et al. DNA methylation and lncRNA control asynchronous DNA replication at specific imprinted gene domains. Nat Commun 17, 1844 (2026). https://doi.org/10.1038/s41467-026-68558-2
Parole chiave: imprinting genomico, metilazione del DNA, tempistica della replicazione, RNA non codificante lungo, cellule staminali embrionali