Clear Sky Science · it
L'attivazione microbica del GLP-2R attenua l'infiammazione gastrointestinale
Perché una proteina amica dell'intestino è importante
Mentre il mondo cerca modi sostenibili per nutrire una popolazione in crescita, gli scienziati guardano oltre fattorie e campi verso grandi serbatoi d'acciaio dove si coltivano microbI per il cibo. Questo studio esplora se una di queste proteine a base microbica può fare più che semplicemente nutrirci. I ricercatori si sono chiesti: una proteina derivata da batteri innocui può sia soddisfare le esigenze dietetiche sia proteggere attivamente l'intestino dall'infiammazione, un problema centrale in condizioni come le malattie infiammatorie intestinali e il danno intestinale indotto dalla chemioterapia?
Un nuovo tipo di proteina dai microbi
La proteina al centro di questo lavoro proviene da un batterio del suolo chiamato Methylococcus capsulatus Bath (McB). Invece di essere consumato come batterio vivo, McB viene trasformato in un lisato microbico—essenzialmente una polvere di cellule batteriche rotte—commercialmente prodotta con il nome FeedKind®. Ai topi sono state somministrate diete in cui questo lisato forniva la maggior parte della proteina, sia in una dieta semplice sia in una più «complessa» simile a quella umana. Il team ha quindi seguito come questa dieta ha modificato la composizione dei microbi intestinali, le cellule immunitarie che ispezionano l'intestino e la capacità dell'intestino di resistere a diversi tipi di danno.
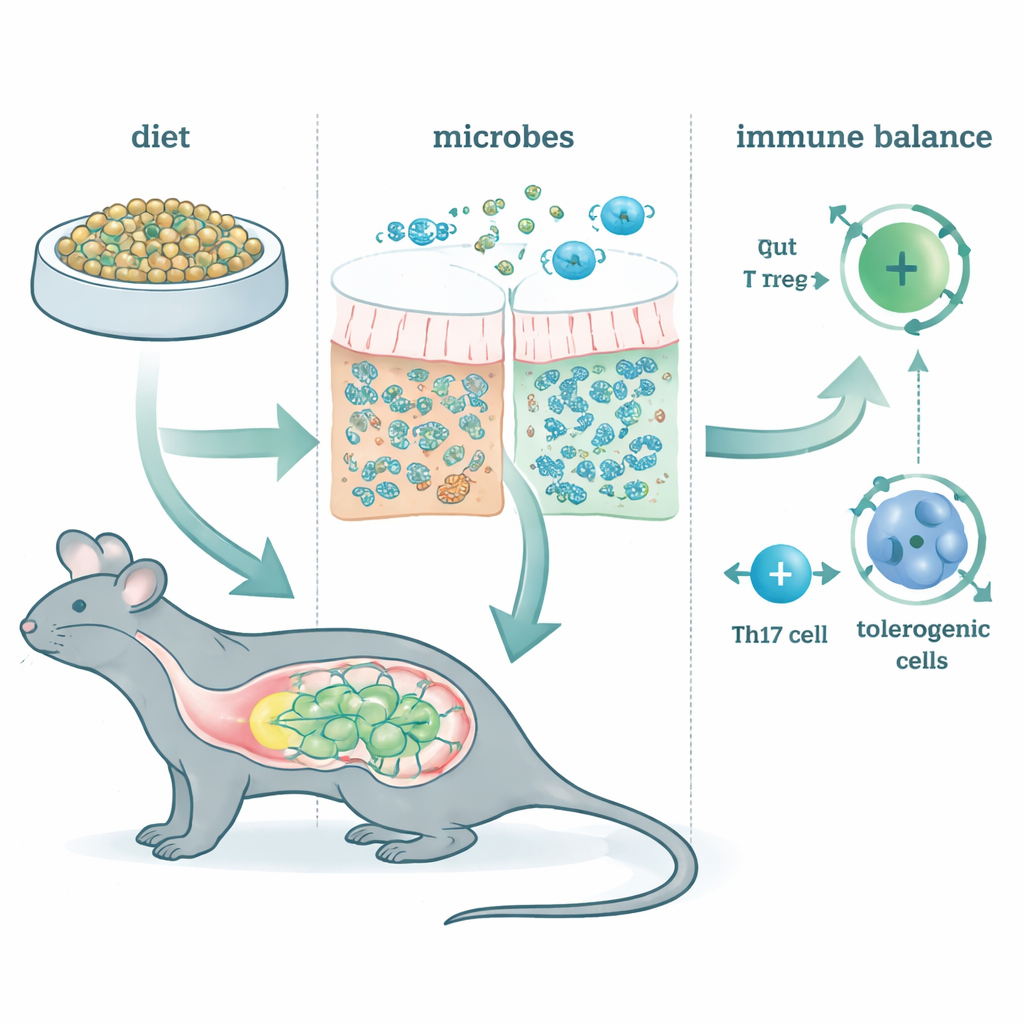
Rimodellare il vicinato microbico
La somministrazione di McB ha modificato rapidamente e in modo persistente il microbiota intestinale, indipendentemente dalla dieta di base degli animali. Solo una frazione minima di McB è comparsa nelle feci, il che indica che il materiale è stato quasi completamente usato nell'intestino. Al contrario, alcune specie batteriche di famiglie come Lachnospiraceae e Bacteroidaceae sono prosperate. Analisi genetiche hanno mostrato che queste comunità erano arricchite per vie fermentative che producono acidi grassi a catena corta—piccole molecole già note per nutrire le cellule intestinali e influenzare l'immunità. In altre parole, McB ha agito meno come una proteina convenzionale e più come un combustibile mirato che rimodella le funzioni dei microbi residenti.
Insegnare al sistema immunitario la tolleranza
Gli autori hanno poi esaminato tipi chiave di cellule T che contribuiscono a decidere se l'intestino reagisce in modo calmo o aggressivo a ciò che lo attraversa. Un gruppo, i linfociti T regolatori perifericamente indotti (pTreg), aiuta a prevenire reazioni eccessive al cibo e ai microbi amici. Un altro gruppo, le cellule Th17, può o promuovere infiammazione dannosa o aiutare a mantenere una barriera sana, a seconda del loro «stato». L'alimentazione con McB ha aumentato fortemente i pTreg lungo tutto l'intestino, anche quando la maggior parte dei microbi intestinali era eliminata con antibiotici. Al contrario, gli effetti di McB sulle cellule Th17 dipendevano dalla presenza e dal funzionamento normale dei batteri intestinali. Nei topi con microbi intatti, McB ha spinto le Th17 verso uno stato più calmante, produttore di IL‑10 e meno infiammatorio. Quando la fermentazione è stata bloccata, questo spostamento verso la tolleranza è svanito, sottolineando che McB opera in parte riorientando le conversazioni tra microbi e sistema immunitario.
Proteggere l'intestino durante il danno
Per verificare se questi cambiamenti si traducono in protezione reale, i ricercatori hanno sfidato i topi con due insulti intestinali gravosi. Uno era un farmaco chemioterapico, il 5‑fluorouracile, che causa danni diffusi e l'accorciamento dei villi, le strutture simili a dita che assorbono i nutrienti. L'altro era una sostanza chimica (DSS) che provoca colite, un modello di infiammazione del grosso intestino. I topi alimentati con la dieta a base di McB hanno perso meno peso, mantenuto villi e lunghezza del colon maggiori, mostrato meno lesioni sanguinanti e avuto punteggi di danno microscopico più bassi in entrambi i modelli. Questi benefici sono rimasti anche quando le cellule T CD4 sono state rimosse sperimentalmente, suggerendo che le azioni protettive di McB non sono dovute esclusivamente alle cellule immunitarie adattative ma coinvolgono anche effetti diretti sul rivestimento intestinale.
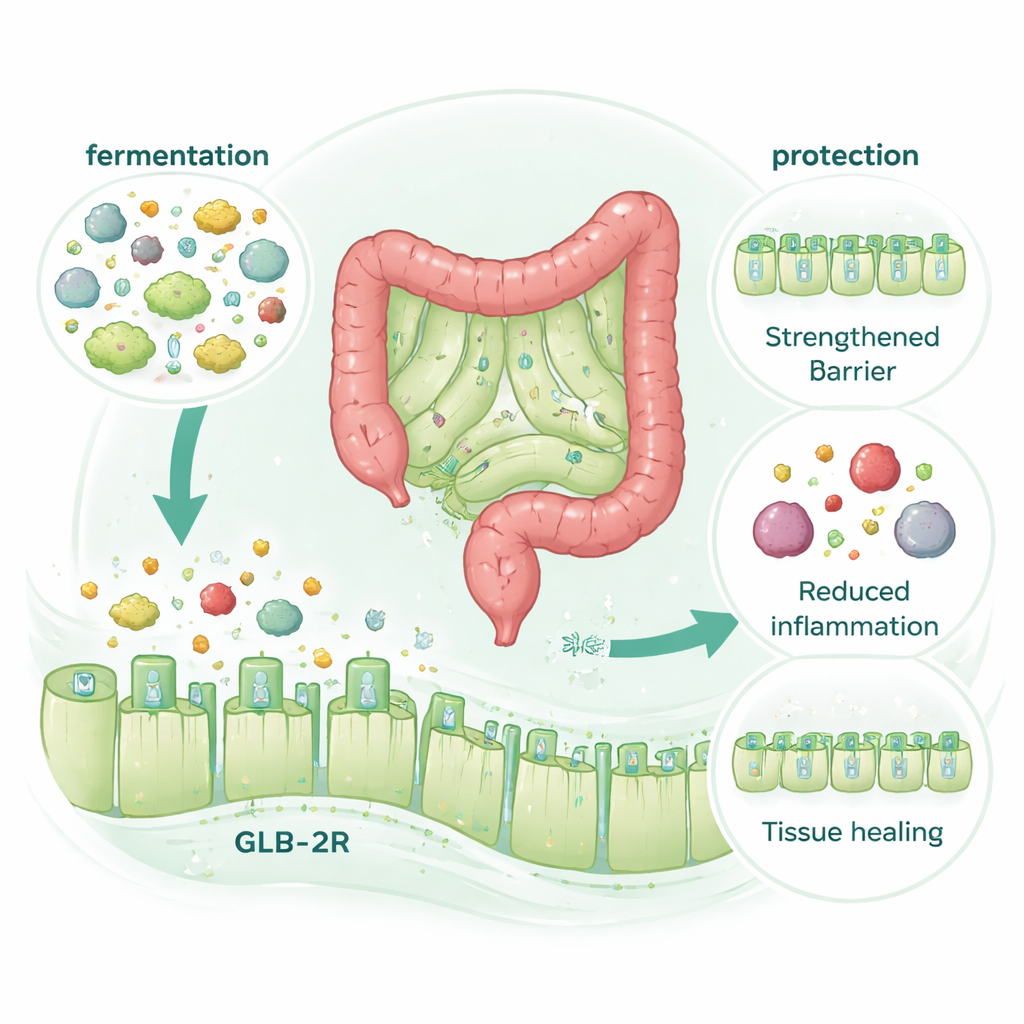
Un recettore ormonale, ma nessun ormone aggiuntivo
Una sorpresa è stata la scoperta che l'effetto protettivo di McB richiedeva assolutamente il recettore intestinale per un ormone che promuove la riparazione chiamato GLP‑2 (il recettore GLP‑2, o GLP‑2R), ma non il recettore correlato GLP‑1. Nei topi privi di GLP‑2R, McB non li ha più protetti dal danno da chemioterapia o da colite. Tuttavia McB di per sé non aumentava i livelli di GLP‑2 nel sangue, anche quando la digestione e la degradazione ormonale erano strettamente controllate. Al contrario, i benefici scomparivano quando la fermentazione microbica nel colon veniva bloccata chimicamente, anche se la composizione complessiva del microbiota cambiava molto poco. Ciò indica un meccanismo in cui la degradazione microbica di McB genera piccoli composti che si comportano come «mimici» del GLP‑2, attivando il suo recettore per rinforzare la barriera e favorire la riparazione senza il rilascio extra dell'ormone.
Cosa potrebbe significare per i cibi del futuro
Per il lettore non specialista, il messaggio chiave è che alcune fonti proteiche future potrebbero essere progettate non solo per essere a basso impatto climatico, ma anche per supportare attivamente la salute intestinale. Nei topi, un lisato commerciale scalabile di McB ha sia riprogrammato l'immunità verso la tolleranza sia aiutato l'intestino a resistere a gravi danni, attraverso due vie parzialmente indipendenti: un aumento diretto dei linfociti T regolatori e un'attivazione del recettore GLP‑2 guidata dalla fermentazione che favorisce la riparazione tissutale. Sebbene siano necessari studi sull'uomo, il lavoro suggerisce che le proteine derivate da microbi potrebbero costituire una nuova classe di alimenti «intelligenti»—in grado di nutrirci, collaborare con i nostri microbi e rafforzare silenziosamente le difese naturali dell'intestino contro l'infiammazione.
Citazione: Yang-Jensen, S.K., Choi, B.SY., Nägele, N.S. et al. Microbial activation of the GLP-2R mitigates gastrointestinal inflammation. Nat Commun 17, 1839 (2026). https://doi.org/10.1038/s41467-026-68551-9
Parole chiave: infiammazione intestinale, proteina microbica, microbioma, recettore GLP-2, linfociti T regolatori