Clear Sky Science · it
FUNDC1 endoteliale regola il riprogrammamento metabolico e la transizione obesità-diabete attraverso l’asse SIRT3/GATA2/endotelina-1
Perché le cellule dei vasi sanguigni contano nell’obesità e nel diabete
L’obesità e il diabete di tipo 2 vengono spesso attribuiti al tessuto adiposo, al fegato o al pancreas. Ma questo studio rivela un colpevole sorprendente: il sottile strato di cellule che riveste i nostri vasi sanguigni, chiamato endotelio. I ricercatori mostrano che una piccola proteina mitocondriale in queste cellule, denominata FUNDC1, può favorire il passaggio da un semplice aumento di peso a un diabete conclamato modificando il modo in cui i vasi comunicano con gli organi metabolici.
Stress sulla “pelle” interna del corpo
Le cellule endoteliali costituiscono una vasta e delicata rete che controlla il flusso sanguigno, la distribuzione dei nutrienti e i segnali verso i tessuti vicini. In condizioni di salute bilanciano fattori di rilassamento come l’ossido nitrico con fattori di costrizione come l’endotelina-1 (ET-1). Nell’obesità e nelle fasi iniziali del diabete questo equilibrio si sposta a favore di ET-1, che non solo restringe i vasi ma altera anche il modo in cui cellule adipose, muscolari e epatiche gestiscono zuccheri e grassi. Gli autori hanno iniziato mostrando nel topo che la disfunzione vascolare compare già dopo solo due mesi di alimentazione ricca di grassi, prima che si manifesti una chiara insulino-resistenza, suggerendo che l’endotelio danneggiato possa contribuire a scatenare la malattia metabolica piuttosto che limitarsi a rispondere ad essa.
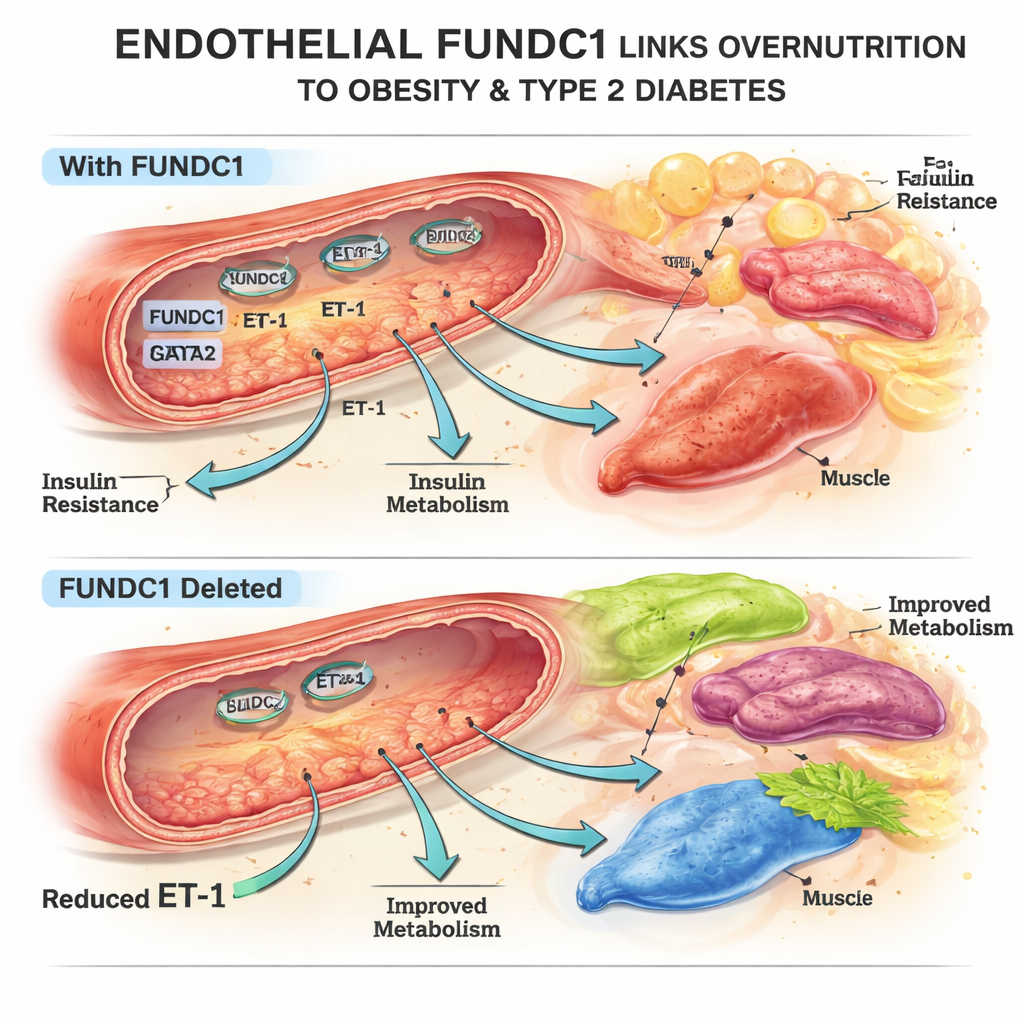
Un interruttore mitocondriale che modella il grasso corporeo
Il gruppo si è concentrato su FUNDC1, una proteina sulla superficie dei mitocondri, le centrali energetiche della cellula. Nelle cellule endoteliali di topo e umano esposte a un eccesso di grasso, i livelli di FUNDC1 cambiano nel tempo: diminuiscono inizialmente, poi aumentano marcamente con la sovralimentazione prolungata. Utilizzando topi geneticamente modificati privi di FUNDC1 solo nelle cellule endoteliali, i ricercatori hanno scoperto che questi animali erano parzialmente protetti dall’aumento di peso indotto da dieta ricca di grassi, avevano meno tessuto adiposo, adipociti più piccoli e un migliore controllo della glicemia. Tessuti adiposi, epatici e il grasso bruno rispondevano meglio all’insulina, pur senza un aumento dei livelli circolanti di insulina. Questi cambiamenti non potevano essere spiegati da differenze nell’assunzione di cibo o nell’attività, indicando piuttosto l’influenza del sistema vascolare sul metabolismo.
Un messaggero chimico che guida l’insulino-resistenza
Per capire come FUNDC1 endoteliale influenzi organi distanti, gli autori hanno analizzato diverse sostanze secrete dalle cellule endoteliali. Una è emersa in modo evidente: ET-1. Quando FUNDC1 veniva eliminata nelle cellule endoteliali, la produzione di ET-1 nei vasi e nel circolo diminuiva marcatamente, sia in condizioni normali sia in presenza di dieta ricca di grassi. Esperimenti in colture di adipociti, epatociti e miociti hanno mostrato che ET-1 promuove la proliferazione dei precursori adiposi, altera l’accumulo e la mobilizzazione dei grassi e aggrava l’accumulo lipidico in fegato e muscolo esposti a elevati livelli di grasso — un quadro noto per favorire l’insulino-resistenza. Nei topi vivi, l’infusione di ET-1 all’inizio di una dieta ricca di grassi annullava i benefici protettivi dell’eliminazione di FUNDC1 endoteliale: peso corporeo, massa grassa, controllo glicemico e funzione vascolare peggioravano, sottolineando ET-1 come collegamento chiave tra endotelio e malattia metabolica.
Un asse di segnalazione interno: FUNDC1, SIRT3 e GATA2
Lo studio delinea poi una catena molecolare dettagliata all’interno delle cellule endoteliali. Sotto stress da dieta ricca di grassi, una forma lunga dell’enzima SIRT3 (SIRT3-L), che può risiedere sia nel nucleo sia nei mitocondri, si sposta dal nucleo ai mitocondri con l’aiuto di FUNDC1 e di una proteina chaperone chiamata HSC70. Una volta sequestrata nei mitocondri, meno SIRT3-L è disponibile nel nucleo per rimuovere gruppi acetile da GATA2, un fattore di trascrizione che potenzia l’attività del gene ET-1. GATA2 più acetilata è più stabile e aumenta la produzione di ET-1. Quando FUNDC1 è assente, SIRT3-L rimane nel nucleo, dove deacetila GATA2, portando alla degradazione di GATA2 e a una minore produzione di ET-1. Intrigantemente, SIRT3 a sua volta promuove la degradazione di FUNDC1, creando un circuito di retroazione che normalmente limita la via ma che viene disgregato durante la sovralimentazione cronica.
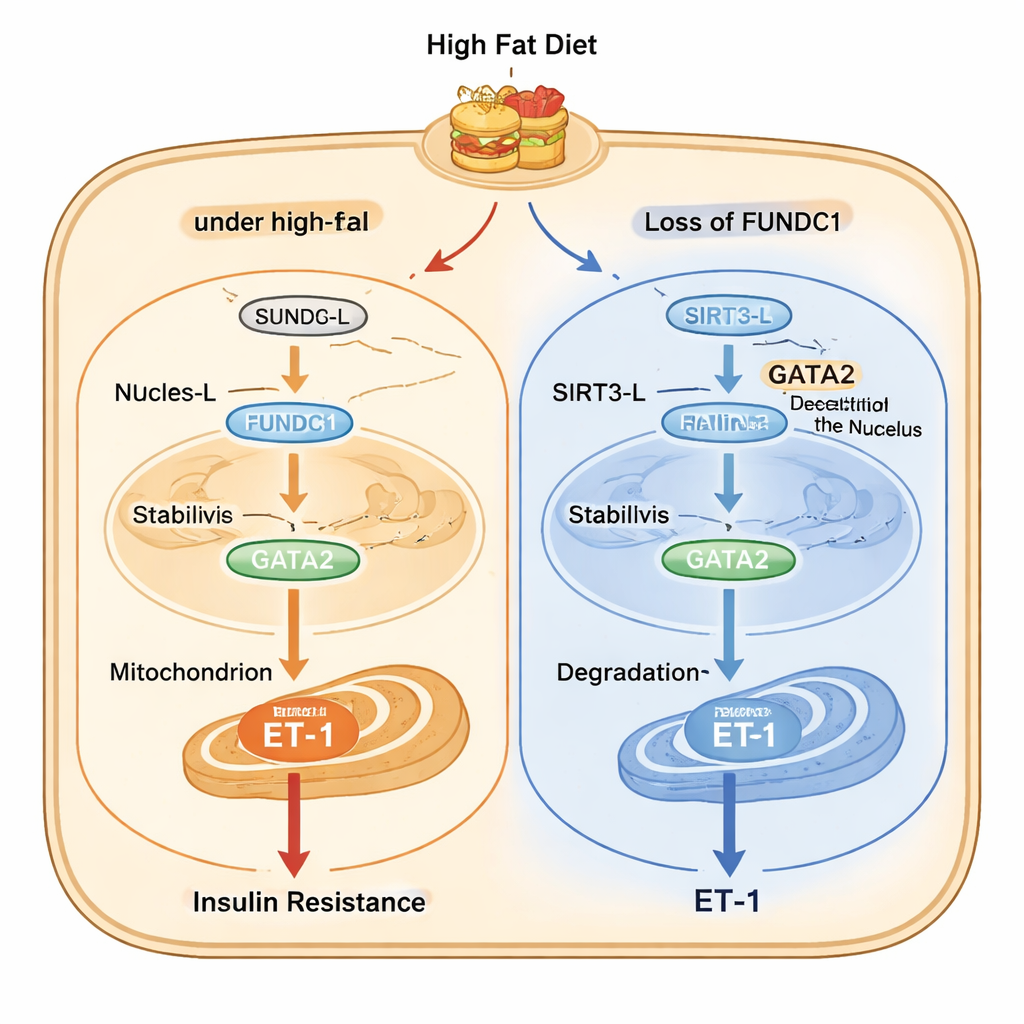
Da modelli murini alla malattia umana
Per verificare se questo meccanismo sia rilevante nelle persone, i ricercatori hanno esaminato sangue e piccole arterie di individui con obesità e diabete di tipo 2 e di volontari sani. I pazienti con entrambe le condizioni presentavano livelli ematici più elevati di ET-1 e una maggiore espressione di FUNDC1, GATA2 e del gene ET-1 nell’endotelio vascolare. La quantità di ET-1 nel sangue si correlava strettamente con l’indice di massa corporea e con la glicemia a lungo termine (HbA1c), e i livelli genici di ET-1 nei vasi si correlavano fortemente con FUNDC1 e GATA2. Questi schemi rispecchiano i risultati nei topi e sostengono l’idea che un asse FUNDC1–SIRT3–GATA2–ET-1 iperattivo sia operativo nel tessuto vascolare umano sotto stress metabolico.
Un nuovo bersaglio nella lotta contro il diabete
Per i non specialisti, il messaggio centrale è che il danno dovuto alla sovralimentazione può comparire inizialmente nelle cellule che rivestono i nostri vasi sanguigni. Lì, una proteina mitocondriale, FUNDC1, contribuisce a deviare un enzima regolatorio, SIRT3, lontano dal nucleo, permettendo a un altro fattore, GATA2, di aumentare la produzione di ET-1, un potente segnale ormonale che favorisce sia l’irrigidimento vascolare sia l’insulino-resistenza. Bloccare questa via — riducendo l’attività di FUNDC1 endoteliale o abbassando ET-1 — potrebbe aiutare a prevenire la transizione dall’obesità al diabete e contemporaneamente proteggere i vasi sanguigni.
Citazione: Li, J., Li, D., Zhao, F. et al. Endothelial FUNDC1 regulates metabolic reprogramming and the obesity-diabetes transition through the SIRT3/GATA2/endothelin-1 axis. Nat Commun 17, 1836 (2026). https://doi.org/10.1038/s41467-026-68548-4
Parole chiave: cellule endoteliali, mitocondri, endotelina-1, obesità, diabete di tipo 2