Clear Sky Science · it
Idrogenazione altamente selettiva e pratica di (etero)areni funzionalizzati
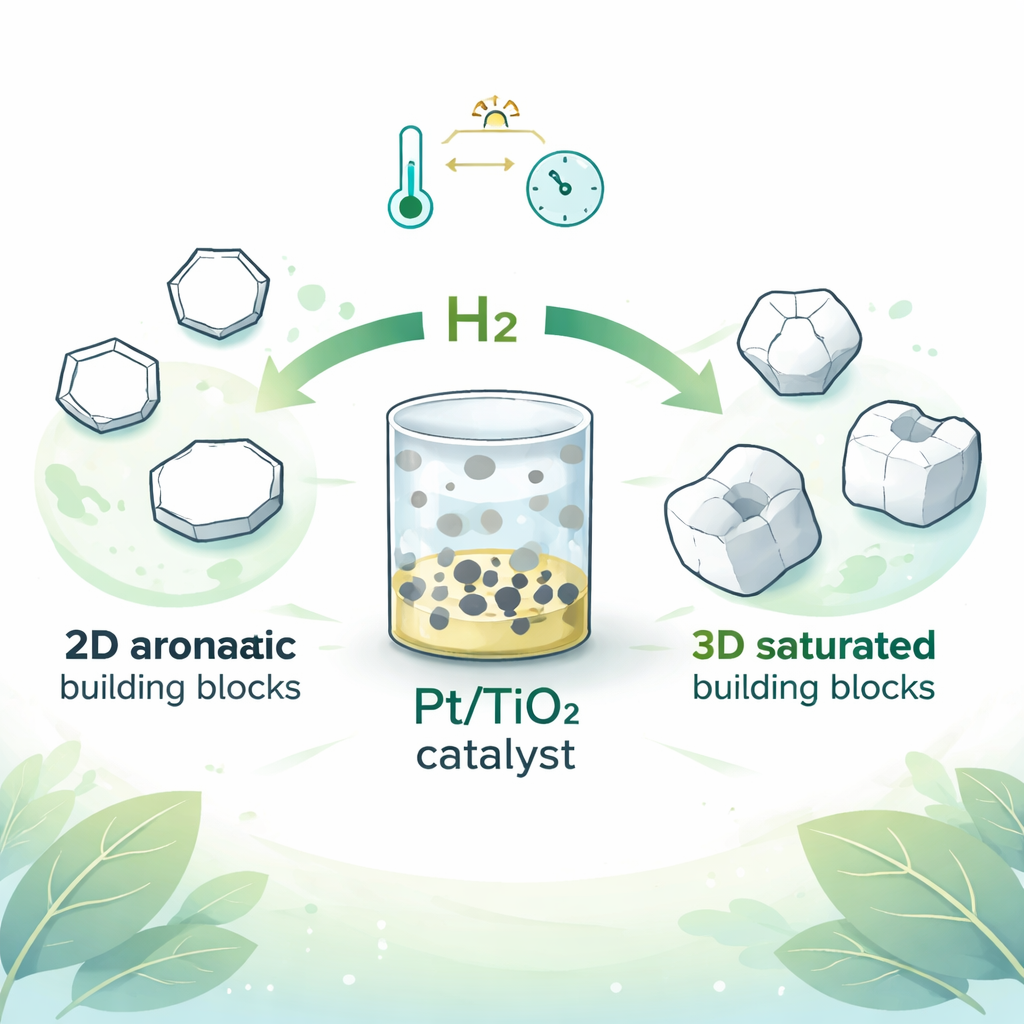
Da molecole piatte a blocchi costruttivi 3D
I farmaci moderni, le materie plastiche e molte sostanze chimiche di uso quotidiano sono costruiti a partire da piccoli “mattoncini” molecolari. La maggior parte di questi mattoncini è piatta e ad anello, chiamata arene, che gli chimici apprezzano perché è facile da sintetizzare e modificare. Tuttavia, chi sviluppa farmaci e i ricercatori dei materiali richiedono sempre più forme tridimensionali, che spesso si comportano meglio nell’organismo e conferiscono prestazioni superiori alle plastiche. Questo articolo descrive un nuovo metodo pratico per trasformare anelli piatti in strutture 3D precise usando un catalizzatore al platino robusto, aprendo una via più semplice verso farmaci di nuova generazione e additivi plastici più sicuri.
Perché la forma conta nelle molecole
Gli anelli aromatici piatti sono ovunque: in prodotti farmaceutici, agrochimici, vitamine e polimeri. La loro diffusione li rende economici e ampiamente disponibili. Al contrario, i loro cugini “saturi” — anelli privi di doppi legami — sono molto meno comuni sul mercato, pur offrendo vantaggi importanti. Quando un anello diventa saturo e tridimensionale, gli chimici ottengono un controllo molto più fine su proprietà come l’adattamento di un farmaco in una tasca proteica o il comportamento meccanico di una plastica. Per esempio, modificando il rapporto tra due disposizioni 3D speculari (dette forme cis e trans), i produttori di polimeri possono aggiustare la temperatura di transizione vetrosa, che determina se un materiale è rigido o flessibile a una data temperatura.
La sfida di piegare anelli piatti
Trasformare un anello aromatico piatto in un anello saturo 3D sembra semplice — basta aggiungere idrogeno. In pratica è molto difficile. Gli anelli aromatici sono straordinariamente stabili, quindi rompere la loro «aromaticità» richiede molta energia. Allo stesso tempo, le molecole reali spesso portano gruppi chimici sensibili, come esteri o ammidi, che devono restare intatti. Un catalizzatore deve dunque fare tre cose contemporaneamente: attivare anelli resistenti a condizioni miti, ignorare le altre parti sensibili della molecola e disporre i nuovi atomi di idrogeno in modo che una forma 3D sia fortemente favorita rispetto all’altra. I catalizzatori esistenti che raggiungono questi obiettivi sono di norma complessi, sensibili e difficili da riciclare, il che li rende poco attraenti per l’uso industriale su larga scala.
Un catalizzatore al platino robusto su un supporto noto
I ricercatori riportano un catalizzatore eterogeneo semplice: piccole particelle di platino depositate su biossido di titanio (Pt/TiO2). Con questo materiale sono in grado di idrogenare un’ampia varietà di areni e eteroareni multi‑sostituiti — anelli che contengono anche atomi come azoto o ossigeno — a temperature e pressioni di idrogeno relativamente miti. Notevolmente, le reazioni favoriscono nettamente una disposizione 3D, spesso raggiungendo un rapporto di diastereomeri fino a 99 a 1 a favore della forma cis. Diversamente da molti sistemi precedenti, il catalizzatore è solido, facile da filtrare e riutilizzabile. Inoltre preserva gruppi delicati come esteri, esteri boronici e ammidi, elemento cruciale quando l’anello fa parte di un farmaco complesso o di un materiale funzionale.
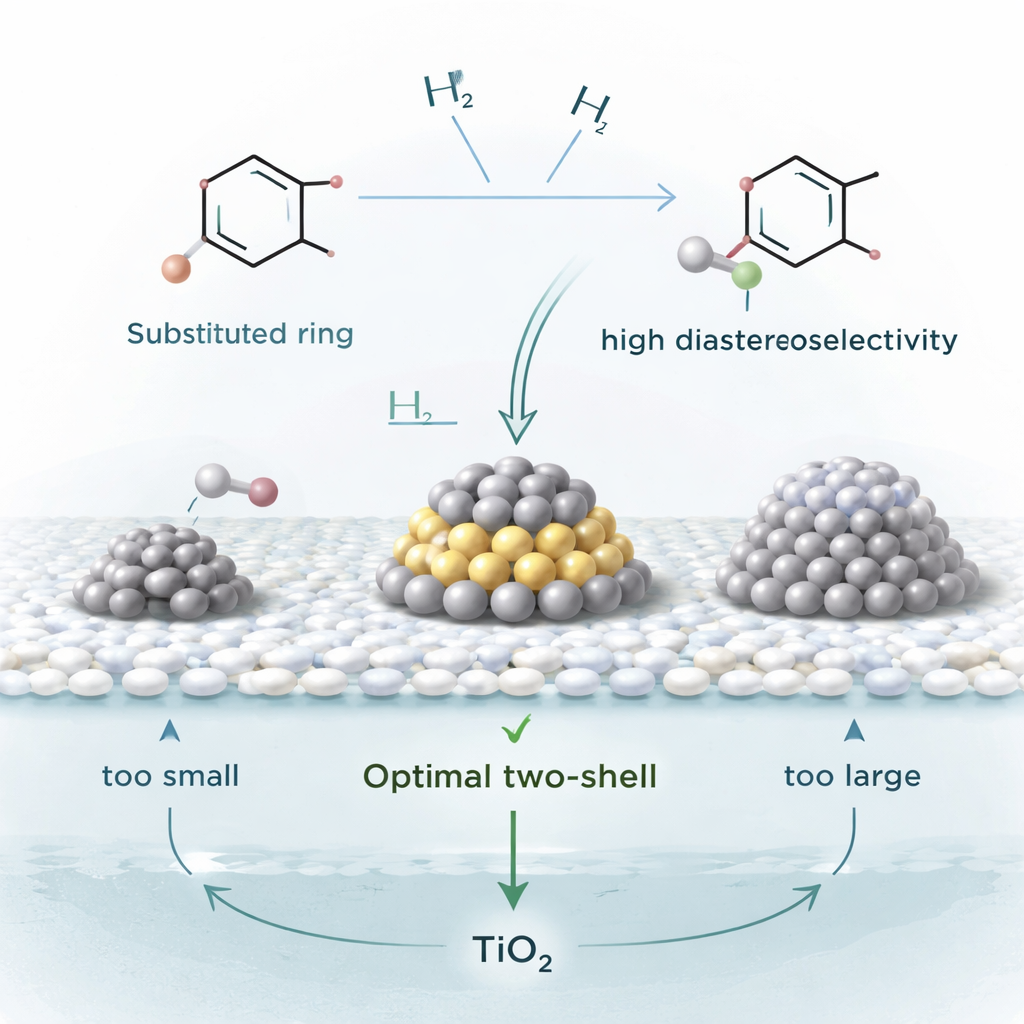
Analisi del punto ottimale
Per capire perché questo catalizzatore funzioni così bene, il gruppo ha studiato una reazione di riferimento: la trasformazione del dimetilftalato, un comune prodotto industriale, nel suo corrispondente saturo. Preparando Pt/TiO2 con diversi carichi di platino e misurando le velocità di reazione, hanno scoperto che l’attività massima si verifica quando le particelle di platino hanno una dimensione intermedia molto specifica. Immagini al microscopio elettronico e simulazioni al computer hanno mostrato che le particelle con una cosiddetta struttura a due gusci — abbastanza grandi da ospitare insieme l’anello piatto e l’idrogeno, ma non così grandi da rendere l’anello solo debolmente legato — sono il vero «punto dolce». Cluster più piccoli si intasano a causa dell’adesione troppo forte dell’anello, mentre particelle molto più grandi non lo trattengono con sufficiente fermezza per riprodurre il comportamento osservato.
Da reazioni modello a prodotti reali
Forti di questa intuizione, gli scienziati hanno esplorato l’applicabilità del catalizzatore. Hanno trasformato con successo molti derivati del benzene sostituiti e sistemi ad anello fusi o tesi, di solito con rese elevate e forte preferenza per i prodotti cis. Cruciale per la chimica farmaceutica, hanno inoltre applicato il metodo ad eteroareni contenenti azoto che fungono da mattoni per farmaci importanti, inclusi intermedi correlati all’antibiotico moxifloxacina. Per dimostrare la rilevanza industriale, hanno eseguito una reazione su scala chilogrammo che converte un plasticizzante ftalato commerciale in un’alternativa priva di ftalati in condizioni senza solventi, ottenendo quasi esclusivamente la forma cis desiderata e dimostrando che il catalizzatore può essere riciclato più volte.
Cosa significa per la chimica di tutti i giorni
In termini semplici, questo lavoro fornisce agli chimici uno strumento robusto e riutilizzabile per rimodellare comuni anelli piatti in forme più tridimensionali e definite, senza lunghi percorsi sintetici. Identificando con precisione quali strutture di platino svolgono il lavoro più intenso, lo studio apre la strada alla progettazione razionale di catalizzatori ancora migliori. L’impatto immediato potrebbe essere percorsi più rapidi verso nuovi candidati farmaceutici, plasticizzanti più sicuri e più facilmente tarabili, e un uso più efficiente dell’idrogeno nella produzione chimica — tutto ottenuto con un catalizzatore solido relativamente semplice che si integra bene nei processi industriali esistenti.
Citazione: Qu, R., Jena, S., Xiao, L. et al. Highly selective and practical hydrogenation of functionalized (hetero)arenes. Nat Commun 17, 2015 (2026). https://doi.org/10.1038/s41467-026-68537-7
Parole chiave: idrogenazione di areni, catalizzatore al platino, impalcature molecolari 3D, eteroareni, sintesi di plasticizzanti