Clear Sky Science · it
Interazione loop3-LRP4 nelle adipociti richiesta dalla sclerostatina per compromettere il metabolismo corporeo di lipidi e glucosio
Perché le ossa contano per lo zucchero nel sangue
La maggior parte delle persone pensa alle ossa come a uno scheletro inanimato, ma le cellule ossee rilasciano silenziosamente ormoni che comunicano con il resto del corpo. Questo studio mostra come una di queste proteine ossee, chiamata sclerostatina, contribuisca a collegare due problemi molto comuni nelle donne anziane: le ossa fragili (osteoporosi) e il diabete di tipo 2. Scoprendo una specifica “stretta di mano” tra la sclerostatina e le cellule adipose, i ricercatori descrivono un modo per rafforzare le ossa e migliorare glucosio e colesterolo nel sangue senza aumentare il carico sul cuore.
Un segnale osseo che va storto
La sclerostatina è una proteina prodotta principalmente dalle cellule ossee. Normalmente rallenta la formazione ossea e, in modo sorprendente, aiuta anche a proteggere i vasi sanguigni. Il team si è concentrato su un piccolo segmento di questa proteina, chiamato loop3, e ha chiesto se giochi un ruolo nei disordini del metabolismo lipidico e glucidico. Hanno riscontrato che donne in post-menopausa con osteoporosi e diabete di tipo 2, così come persone di nuova diagnosi di diabete, avevano livelli di sclerostatina nel sangue più alti rispetto a individui comparabili senza diabete. In topi alimentati con una dieta ad alto contenuto di grassi per simulare lo stress metabolico, i livelli di sclerostatina aumentavano insieme all’incremento di peso, ai trigliceridi elevati e a un controllo glicemico peggiore. Questi schemi suggerivano che un eccesso di sclerostatina potesse essere più di un semplice spettatore nella malattia metabolica.
Analizzare un piccolo loop con grandi effetti
Per capire cosa faccia il loop3, i ricercatori hanno ingegnerizzato topi nei quali la sclerostatina era alterata o il segmento loop3 era rimosso. I topi che sovrapproducevano sclerostatina normale accumulavano più grasso nei depositi adiposi bianchi, avevano adipociti più grandi, livelli circolanti di acidi grassi più alti e tolleranza al glucosio e risposta insulinica peggiori rispetto ai topi normali. Quando il loop3 veniva eliminato geneticamente o mutato in modo sottile, questi problemi si attenuavano: le riserve di grasso erano più piccole, gli adipociti si riducevano, i lipidi nel sangue calavano e la gestione del glucosio migliorava. Notevolmente, benefici simili apparivano quando i topi venivano trattati con un farmaco progettato come una molecola di DNA (un aptamero) che si lega al loop3 e ne impedisce il funzionamento, senza modificare la quantità di sclerostatina nel sangue.
Come le cellule adipose “ascoltano” il segnale osseo
Il gruppo ha poi osservato da vicino le cellule adipose per capire come il loop3 trasmetta il suo messaggio dannoso. Si sono concentrati su una proteina recettoriale sulla superficie degli adipociti chiamata LRP4, nota in precedenza per aiutare la sclerostatina ad agire sull’osso. Usando esperimenti in coltura cellulare, hanno mostrato che il loop3 si lega fisicamente a una porzione specifica di LRP4 sugli adipociti. Questo contatto innescava cambiamenti che aumentavano la capacità delle cellule di sintetizzare e degradare grassi e di prelevare più glucosio dal sangue, portando a adipociti sovradimensionati e iperattivi. Quando gli scienziati modificarono in modo sottile componenti chiave di LRP4 in modo che il loop3 non potesse più agganciarsi, oppure quando aggiunsero un piccolo peptide bloccante che imitava il sito di aggancio di LRP4, l’effetto della sclerostatina sull’accumulo di grasso e sull’assorbimento di glucosio risultò notevolmente ridotto. Sia nelle cellule che nei topi, bloccare l’interazione loop3–LRP4 ripristinava dimensioni più normali degli adipociti e migliorava la tolleranza al glucosio.
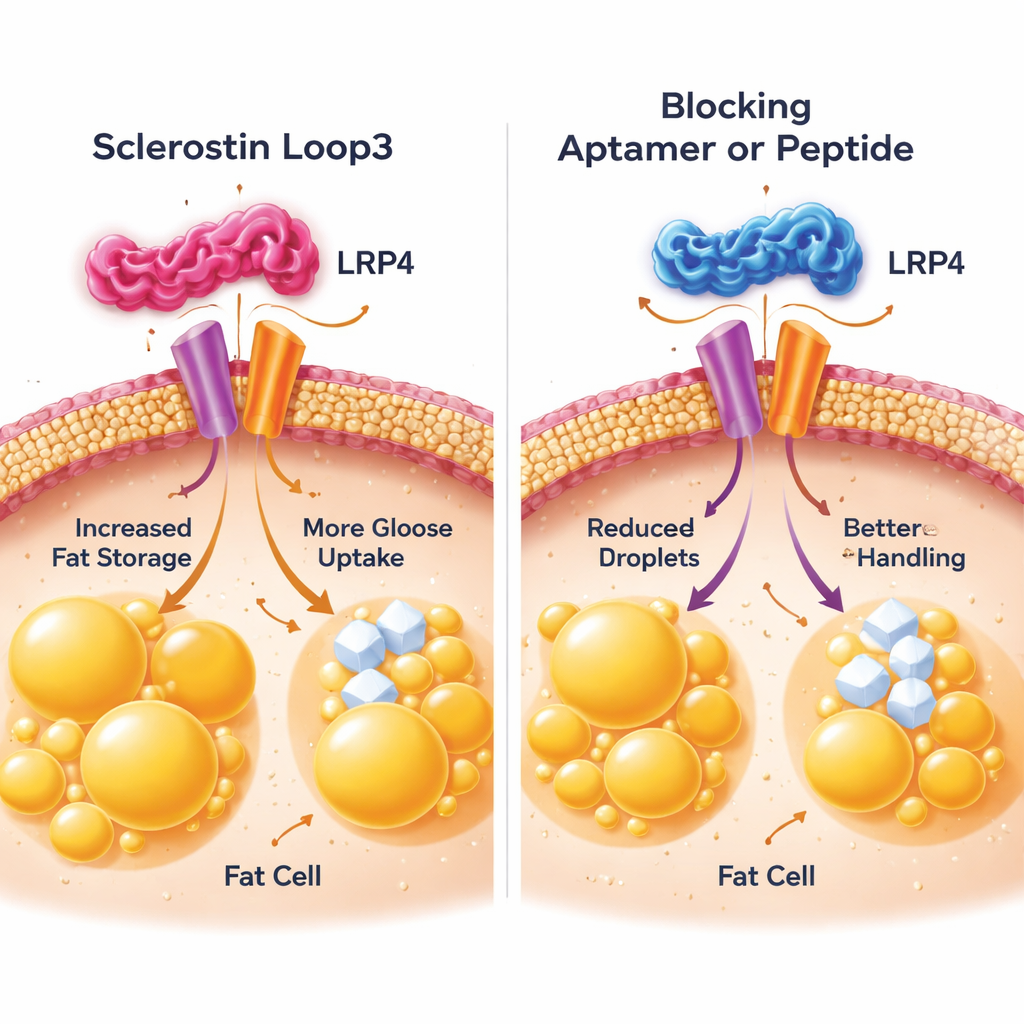
Ossa più forti, metabolismo più sano
Una preoccupazione importante con i farmaci attuali che bloccano la sclerostatina per l’osteoporosi è che, pur costruendo osso e migliorando il metabolismo, i regolatori hanno segnalato un aumento del rischio di gravi problemi cardiaci. Lavori precedenti di questo gruppo avevano mostrato che il loop3 è cruciale per il freno della sclerostatina sulla formazione ossea, ma non per le sue azioni protettive sul cuore. Qui mostrano inoltre che mirare al loop3 — sia tramite modifiche genetiche sia tramite farmaci focalizzati su loop3 — migliora il metabolismo corporeo di grassi e zuccheri in diversi modelli murini, aumentando al contempo massa e resistenza ossea. Diversamente dai medicinali attuali, questa strategia non ha scatenato un aumento compensatorio di un altro inibitore osseo, DKK1, che può attenuare i benefici a lungo termine.
Cosa potrebbe significare per i pazienti
In termini semplici, lo studio sostiene che un pezzo molto piccolo di un ormone osseo contribuisce a guidare sia il cattivo stato di salute delle ossa sia la malattia metabolica parlando direttamente con le cellule adipose. Interrompendo la conversazione tra il segmento loop3 della sclerostatina e il recettore LRP4 sulle cellule adipose, potrebbe essere possibile progettare terapie che rinforzino le ossa e normalizzino i grassi e gli zuccheri nel sangue, pur lasciando intatte le funzioni cardioprotettive della sclerostatina. Per le donne in post-menopausa che spesso affrontano sia osteoporosi sia diabete di tipo 2, terapie mirate al loop3 potrebbero un giorno offrire un modo più sicuro e duraturo per gestire contemporaneamente entrambe le condizioni.
Citazione: Jiang, H., Tao, X., Yu, S. et al. Adipocytic sclerostin loop3-LRP4 interaction required by sclerostin to impair whole-body lipid and glucose metabolism. Nat Commun 17, 1812 (2026). https://doi.org/10.1038/s41467-026-68526-w
Parole chiave: sclerostatina, loop3, LRP4, osteoporosi, diabete di tipo 2