Clear Sky Science · it
L’acido palmitico che induce la palmitoilazione di B7H3 favorisce l’evasione immunitaria
Perché questa ricerca è importante per i pazienti oncologici
La maggior parte delle persone ha sentito parlare dei nuovi farmaci immunoterapici che possono aiutare il sistema immunitario ad attaccare il cancro, tuttavia molti pazienti con il comune tumore colorettale traggono scarso beneficio. Questo studio mette in luce un trucco biochimico nascosto che i tumori colorettali usano per proteggersi dall’attacco immunitario e indica un nuovo tipo di farmaco — un piccolo peptide — che potrebbe migliorare l’efficacia dell’immunoterapia per questi pazienti.
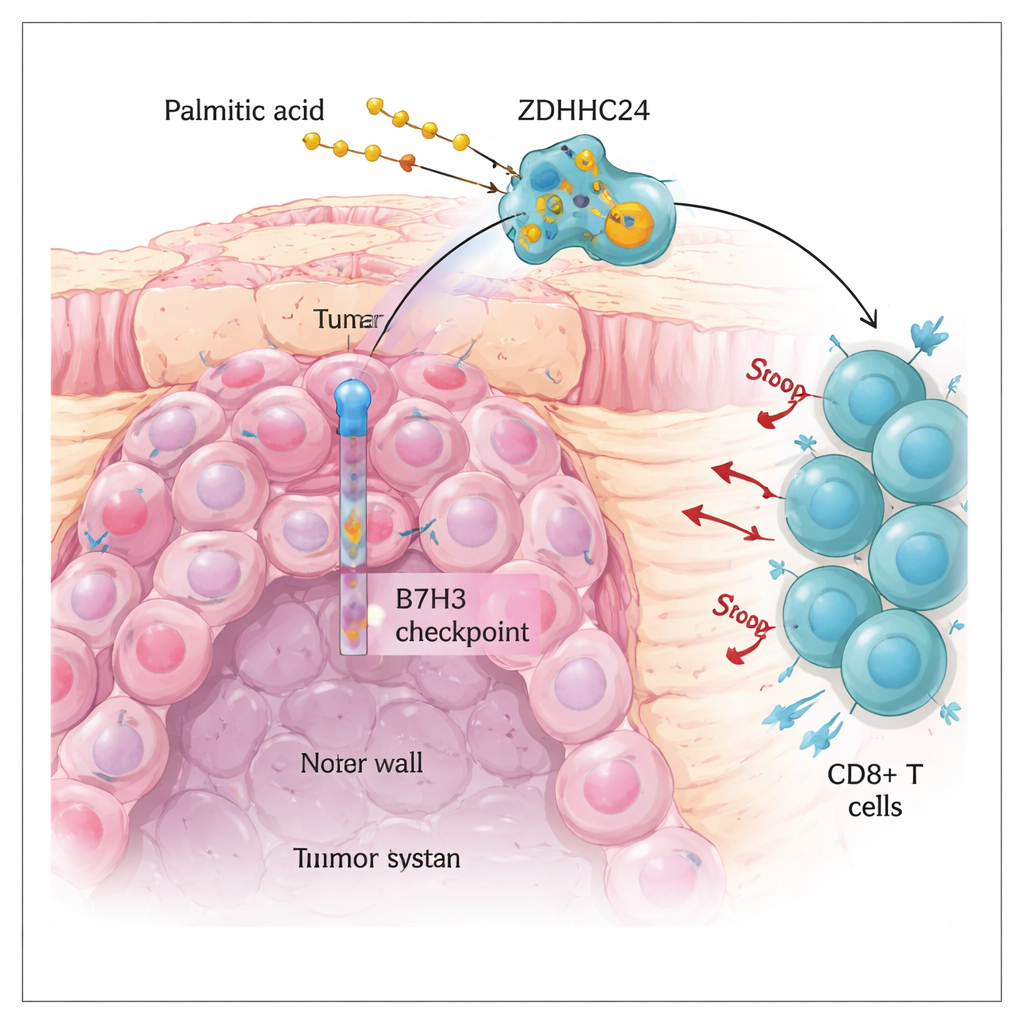
Un ostacolo nell’immunoterapia attuale del cancro del colon
Il cancro colorettale è uno dei tumori più comuni al mondo. I farmaci immunoterapici che tolgono i “freni” al sistema immunitario, come gli inibitori di PD‑1 e PD‑L1, hanno trasformato la cura per una minoranza di pazienti i cui tumori presentano molti errori del DNA (i cosiddetti tumori MSI‑H). Sfortunatamente, la maggior parte dei carcinomi colorettali è microsatellite‑stabile (MSS) e risponde poco a questi trattamenti. Gli autori si sono concentrati su un altro mediatore della soppressione immunitaria chiamato B7H3, che si trova sulla superficie delle cellule tumorali e riduce l’attività delle cellule immunitarie assassine, in particolare le cellule T CD8+. Hanno scoperto che la proteina B7H3 è fortemente elevata nei tumori MSS e correlata a una sopravvivenza peggiore, sebbene il gene B7H3 non risulti più attivo. Questa discrepanza ha posto una domanda importante: che cosa mantiene la proteina B7H3 così abbondante sulle cellule tumorali?
Come un grasso comune aiuta i tumori a nascondersi
Il team ha ipotizzato che il metabolismo tumorale potesse stabilizzare B7H3. Confrontando l’attività genica e i profili di piccole molecole dei tumori MSS e MSI‑H, hanno scoperto che molte vie legate ai lipidi differiscono, con un acido grasso che spiccava: l’acido palmitico. Quando hanno esposto in laboratorio cellule di cancro del colon a diversi prodotti della degradazione lipidica, solo l’acido palmitico ha provocato un netto aumento dei livelli della proteina B7H3. Ulteriori esperimenti hanno spiegato il motivo: l’acido palmitico alimenta un processo di modifica chimica chiamato palmitoilazione, in cui una catena grassa viene attaccata a siti specifici delle proteine. Questa modifica, mediata dall’enzima ZDHHC24 su una singola cisteina all’interno di B7H3, rendeva B7H3 più stabile e più abbondante sulla superficie delle cellule tumorali.
Bloccare la via di smaltimento di un freno immunitario
Le cellule normalmente eliminano le proteine indesiderate o danneggiate attraverso sistemi che funzionano come riciclaggio e smaltimento rifiuti. I ricercatori hanno mostrato che B7H3 viene principalmente degradato da una via cellulare di “auto‑digerimento” chiamata autofagia, che utilizza una proteina recettore chiamata SQSTM1/p62 per marcare il materiale destinato alla distruzione. Quando B7H3 era palmitoilata, si legava male a questo recettore ed eludeva la degradazione autofagica, determinando livelli persistenti e elevati del freno immunitario. Quando il sito di palmitoilazione veniva mutato in modo da non poter più ricevere il gruppo grasso, o quando l’enzima ZDHHC24 veniva eliminato, B7H3 veniva indirizzata in modo più efficiente verso i “sacchi dei rifiuti” cellulari e degradata. Nei topi, i tumori privi di B7H3 palmitoilata crescevano più lentamente, non mostravano cambiamenti del tasso di crescita intrinseco in animali immunodeficienti e contenevano molti più linfociti T CD8+ con un’attività citotossica più forte. Ciò dimostra che la modifica agisce principalmente disarmando l’immunità, non alterando la velocità di proliferazione delle cellule tumorali.
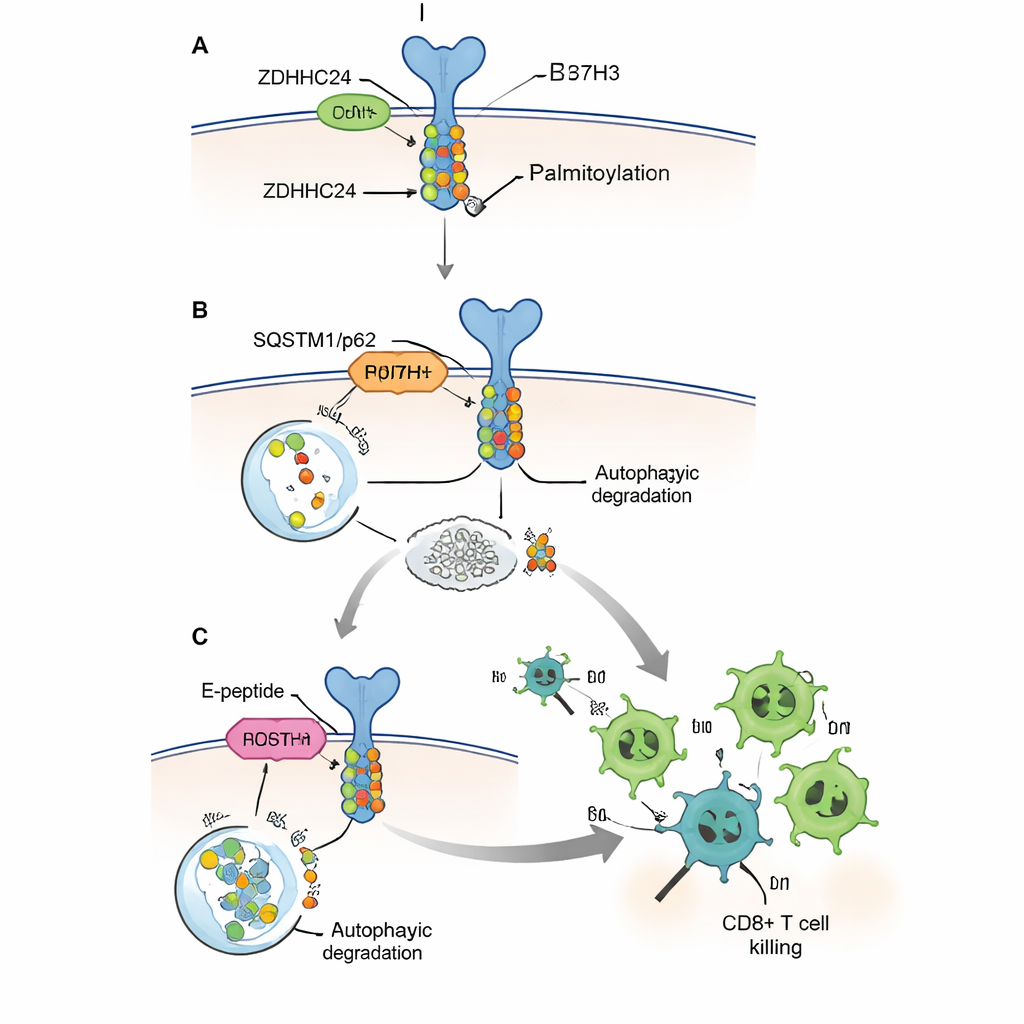
Abbassare lo scudo e potenziare le T
Poiché eliminare completamente ZDHHC24 o B7H3 con approcci genetici non è una strategia pratica per i pazienti, gli autori hanno progettato un peptide corto in grado di penetrare nelle cellule, che chiamano peptide E. Esso imita un breve tratto della proteina B7H3 che normalmente si lega a ZDHHC24, comportandosi da esca e impedendo all’enzima di modificare le molecole reali di B7H3. Nelle cellule coltivate, il peptide E ha ridotto la palmitoilazione e i livelli proteici di B7H3, ha ripristinato il suo riconoscimento dalla macchina dell’autofagia e ha permesso alle cellule T CD8+ umane di uccidere le cellule tumorali in modo più efficiente. In diversi modelli murini, compreso un topo umanizzato con cellule immunitarie umane e tumori colorettali umani, le iniezioni di peptide E hanno ridotto le dimensioni dei tumori, aumentato il numero di T CD8+ al loro interno e potenziato la produzione di molecole killer chiave come la granzyme B e l’interferone‑gamma.
Un nuovo compagno per l’immunoterapia esistente
Infine, i ricercatori hanno verificato se questa strategia potesse funzionare insieme al blocco standard di PD‑1. Nei modelli murini di cancro colorettale, sia il peptide E da solo sia l’anticorpo anti‑PD‑1 da solo offrivano un certo controllo tumorale. Ma in combinazione, i due trattamenti produssero una soppressione tumorale molto più forte e duratura, in alcuni casi causando la scomparsa dei tumori e raddoppiando la sopravvivenza media rispetto ai controlli. Ciò suggerisce che disabilitare lo scudo B7H3 tagliando il suo “ancora” lipidica può integrare gli attuali farmaci checkpoint che bersagliano la via PD‑1.
Cosa significa per le terapie oncologiche future
In termini semplici, questo studio mostra che un grasso alimentare comune, l’acido palmitico, può essere sfruttato dai tumori colorettali per corazzare chimicamente una proteina che blocca l’immunità (B7H3) e aiutare il cancro a nascondersi. Bloccando quell’unico attacco chimico, gli autori sono riusciti a spogliare la corazza, permettere ai sistemi di smaltimento della cellula di rimuovere B7H3 e riaprire la strada alle cellule T CD8+ per attaccare. Sebbene il peptide E sia ancora uno strumento sperimentale in fase iniziale, il lavoro individua la palmitoilazione di B7H3 — e il suo enzima ZDHHC24 — come bersagli farmacologici promettenti. Se agenti simili si dimostrassero sicuri ed efficaci nell’uomo, potrebbero un giorno trasformare più tumori colorettali da “freddi”, insensibili all’immunoterapia, a “caldi”, riconoscibili e eliminabili dal sistema immunitario.
Citazione: Rao, Z., Huang, C., Wu, Q. et al. Palmitic acid-triggered B7H3 palmitoylation promotes immune escape. Nat Commun 17, 1810 (2026). https://doi.org/10.1038/s41467-026-68525-x
Parole chiave: immunoterapia del cancro colorettale, checkpoint B7H3, metabolismo dell’acido palmitico, palmitoilazione delle proteine, immunità tumorale delle cellule T CD8