Clear Sky Science · it
Cellule liquide ultrafini per cryo-EM risolto nel tempo a microsecondi
Osservare le proteine in azione in tempo reale
Molte delle macchine che mantengono vive le nostre cellule sono costituite da proteine, e spesso conosciamo l’aspetto di queste proteine quando sono congelate. Ma ciò che vogliamo davvero vedere è come si muovono mentre svolgono il loro lavoro. Questo studio presenta un nuovo modo per osservare questi movimenti su scale temporali incredibilmente brevi — milionesimi di secondo — senza sacrificare il livello di dettaglio estremamente elevato che la moderna criomicroscopia elettronica (cryo-EM) può offrire.
Una nuova finestra sul mondo microscopico
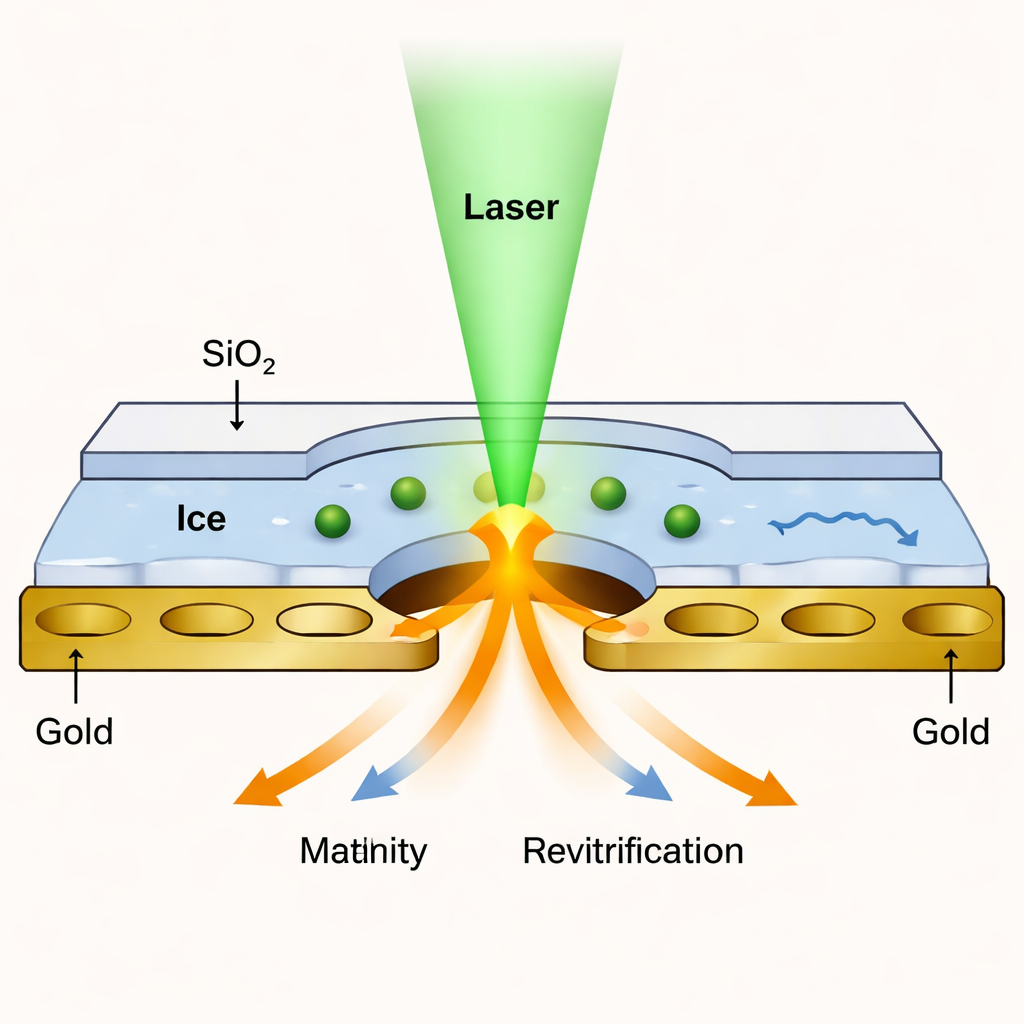
La cryo-EM ha rivoluzionato la biologia strutturale permettendo di ottenere immagini di proteine vitrificate a risoluzione prossima a quella atomica. Tuttavia, i metodi tradizionali forniscono solo istantanee. Per catturare il moto, i ricercatori hanno sviluppato la “cryo-EM risolta nel tempo a microsecondi”, in cui un laser fonde brevemente un campione congelato permettendo alle proteine di muoversi, e poi il campione viene rapidamente ricongelato per intrappolarle in nuove posizioni. Il problema è che il sottilissimo film liquido creato dal laser tende a frammentarsi dopo poche decine di microsecondi, limitando il tempo in cui le proteine possono essere osservate. Il nuovo lavoro risolve questo collo di bottiglia racchiudendo il campione in una cella liquida ultrafina, mantenendolo stabile abbastanza a lungo da osservare movimenti più lenti e complessi.
Costruire una cella liquida ultrafina
Il gruppo ha creato una sorta di sandwich nanoscopico: la soluzione proteica viene vitrificata su una griglia d’oro perforata standard, quindi entrambe le superfici vengono ricoperte con strati di biossido di silicio spessi circa 1,4 nanometri — solo poche decine di atomi. Questi strati simili al vetro fungono da coperchi trasparenti che impediscono al liquido di evaporare quando il laser fonde il ghiaccio. Brevi impulsi laser riscaldano il campione sigillato a una temperatura controllata e poi permettono il rinnovamento della vetrificazione in pochi microsecondi. Poiché le membrane sono così sottili, lasciano comunque passare abbastanza elettroni perché il microscopio produca immagini con una risoluzione quasi pari a quella della cryo-EM convenzionale, fino a circa 1,7–1,8 angstrom per una proteina di prova chiamata apoferritina.
Visioni più nitide e angoli più equi
Una sfida nascosta nella cryo-EM è che le proteine tendono ad aderire all’interfaccia aria‑acqua nel sottile strato di ghiaccio, disponendosi in orientamenti simili e rendendo più difficile la ricostruzione completa in 3D. I rivestimenti di biossido di silicio in queste celle liquide trasformano la superficie da aria‑acqua a acqua‑solido e la rendono più favorevole all’acqua. Di conseguenza, le proteine sono meno propense a aderire in una singola posa. Quando gli autori hanno testato una grande macchina cellulare chiamata subunità ribosomiale 50S, hanno riscontrato che la distribuzione angolare delle particelle è diventata quasi perfettamente uniforme, eliminando di fatto il problema di lunga data della “preferenza di orientamento” pur mantenendo alta risoluzione nelle ricostruzioni finali.
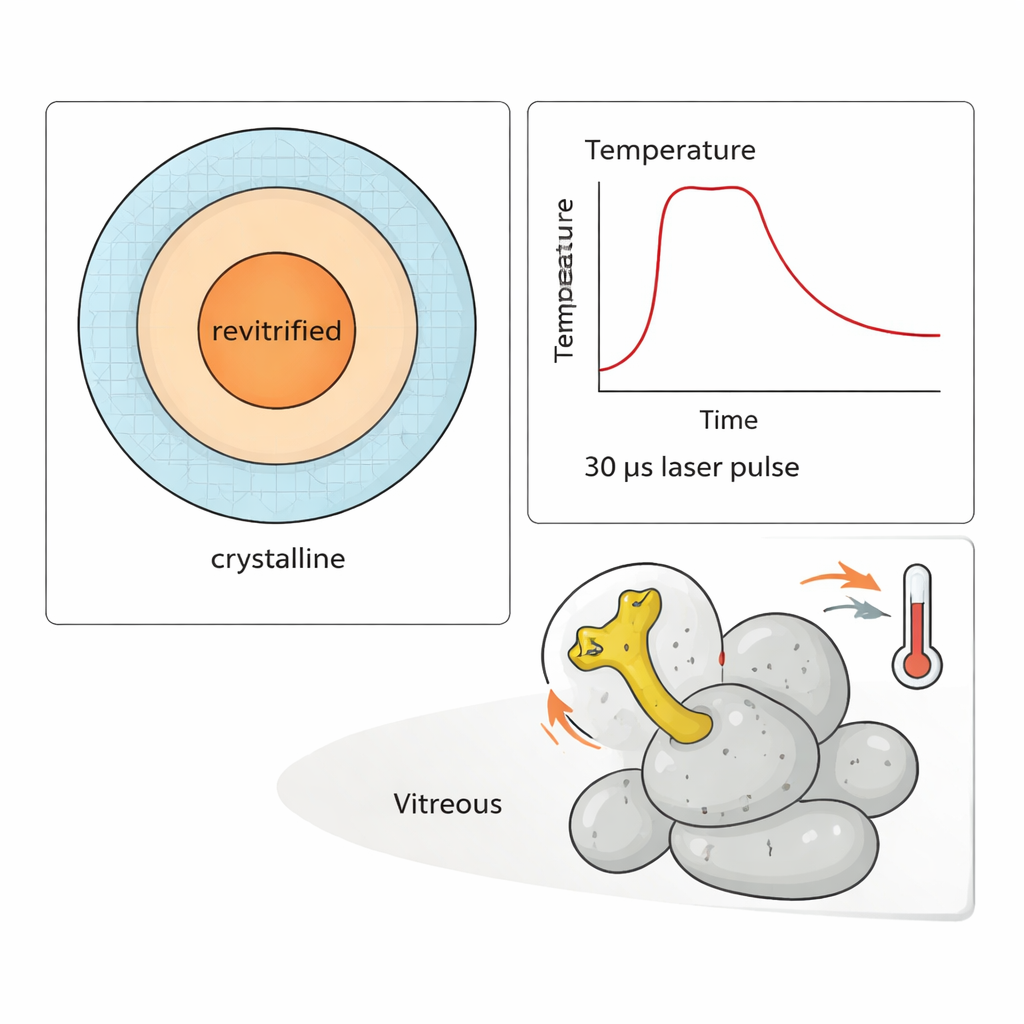
Temporizzare il movimento di una leva molecolare
Per mostrare la potenza del loro metodo, i ricercatori hanno condotto un esperimento di “temperature jump” sulla subunità 50S. Un braccio flessibile di questa particella, noto come stelo L1, oscilla come una leva durante la sintesi proteica. Consegnando treni di impulsi laser da 30 microsecondi, hanno potuto riscaldare il campione a diverse temperature per fino a circa 300 microsecondi e poi ricongelarlo. Simulazioni e misure delle regioni che si sono ritrasformate in vetro hanno permesso di stimare la temperatura di ciascuna particella osservata. Analizzando migliaia di immagini, hanno mostrato che l’ampiezza del movimento dello stelo L1 aumenta chiaramente con la temperatura — ma solo dopo che sono passati centinaia di microsecondi. Nei tempi più brevi, la distribuzione delle conformazioni riflette ancora lo stato originale a temperatura ambiente prima del congelamento.
Perché questo è importante per la biologia futura
Per i non specialisti, il messaggio chiave è che questo design di cella liquida ultrafina estende in modo significativo il tempo durante il quale le proteine possono essere osservate in movimento senza sfocare i dettagli strutturali. Sposta la cryo-EM risolta nel tempo a microsecondi dal catturare solo gli eventi più rapidi allo svelare riorganizzazioni più lente e biologicamente rilevanti, come la risposta ritardata dello stelo L1 a un impulso termico. Con ulteriori perfezionamenti, questo approccio potrebbe coprire la gamma dei millisecondi e oltre, e offre anche nuovi modi per preparare i campioni, ridurre artefatti dell’imaging e innescare reazioni direttamente sulla griglia. In termini pratici, ciò significa che gli scienziati sono sempre più vicini a realizzare “film molecolari” che collegano le forme delle proteine a ciò che effettivamente fanno all’interno delle cellule viventi.
Citazione: Curtis, W.A., Wenz, J., Krüger, C.R. et al. Ultrathin liquid cells for microsecond time-resolved cryo-EM. Nat Commun 17, 1799 (2026). https://doi.org/10.1038/s41467-026-68515-z
Parole chiave: cryo-EM risolto nel tempo, dinamica delle proteine, microscopia elettronica a cella liquida, stelo L1 del ribosoma, membrane ultrafini di biossido di silicio