Clear Sky Science · it
Le forze meccaniche dall’autoassemblaggio peptidico intercellulare guidano la formazione di sfere cellulari
Costruire piccoli tessuti in laboratorio
I ricercatori stanno accelerando la creazione di versioni in miniatura di tessuti umani che si comportino come quelli reali. Questi modelli viventi possono rendere più sicuri i test sui farmaci antitumorali e avvicinare nuove terapie per il diabete e altre malattie. Questo studio presenta un metodo intelligente per indurre le cellule a formare aggregati tridimensionali realistici, completi di reti primitive “simili a vasi” che migliorano il trasporto di nutrienti e la funzione.
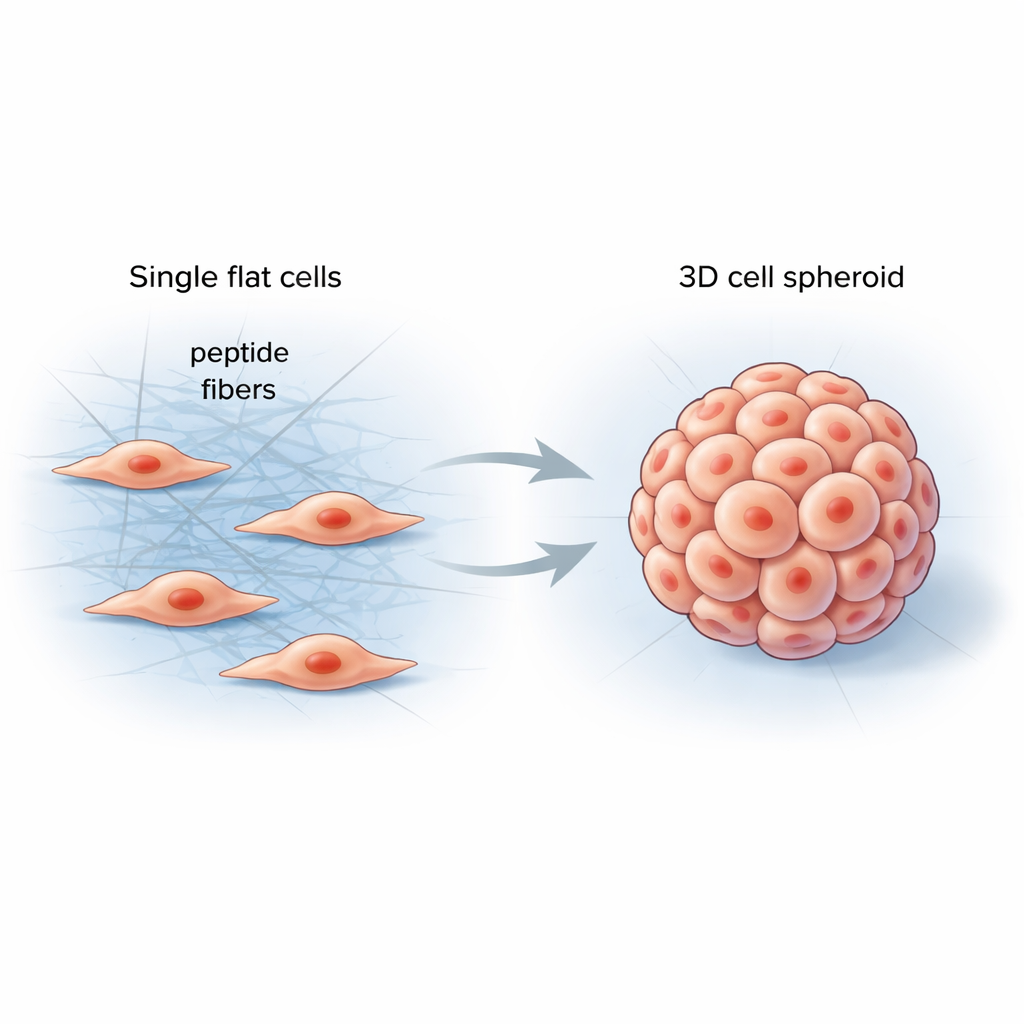
Aiutare le cellule a percepire l’ambiente
Nel nostro corpo le cellule vivono in un ambiente morbido ma strutturato chiamato matrice extracellulare — una rete di proteine che sostiene i tessuti e trasmette segnali meccanici continui alle cellule. I materiali convenzionali da laboratorio faticano a riprodurre questa complessità, spesso generando strati cellulari piatti che si comportano in modo molto diverso rispetto a organi o tumori reali. I ricercatori si sono quindi posti l’obiettivo di progettare un materiale semplice e programmabile che si formi direttamente tra le cellule, irrigidisca il loro intorno in modo controllato e le spinga a assumere forme tridimensionali più naturali.
Peptidi intelligenti che si assemblano tra le cellule
Il gruppo ha creato brevi frammenti proteici, detti peptidi, che possono legarsi tra loro in fibre lunghe e sottili quando incontrano specifici enzimi sulla superficie cellulare. Aggiunti a cellule tumorali, i peptidi restavano inizialmente inattivi, come una soluzione chiara. Quando gli enzimi delle cellule rimuovevano una parte della molecola, i peptidi si autoassemblavano rapidamente in una rete fibrosa avvolgendo e posandosi tra le cellule vicine. Questa nuova maglia di fibre modificava le forze meccaniche locali, incoraggiando le cellule a tirarsi a vicenda, rimodellare la loro impalcatura interna e raccogliersi in sfere 3D anziché disporsi in un foglio.
Dagli aggregati cellulari a reti simili a vasi
Per avvicinarsi ulteriormente al tessuto reale, gli scienziati hanno poi introdotto cellule endoteliali umane, il tipo che normalmente riveste i vasi sanguigni, insieme a un secondo peptide recante un piccolo “tag di indirizzo” che attira queste cellule. Insieme, i peptidi originali e quelli modificati hanno formato un impalcatura comune di nanofibre. Le cellule endoteliali hanno usato questa impalcatura per germogliare in estensioni tubolari che avvolgevano e penetravano le sfere cellulari, creando strutture simili a capillari. Quando il team ha fatto scorrere molecole fluorescenti simili a zuccheri attorno a queste strutture, hanno osservato una penetrazione molto più profonda nel nucleo delle sfere rispetto a sfere prive di questi tubi interni, dimostrando che il trasporto di nutrienti e segnali era nettamente migliorato.
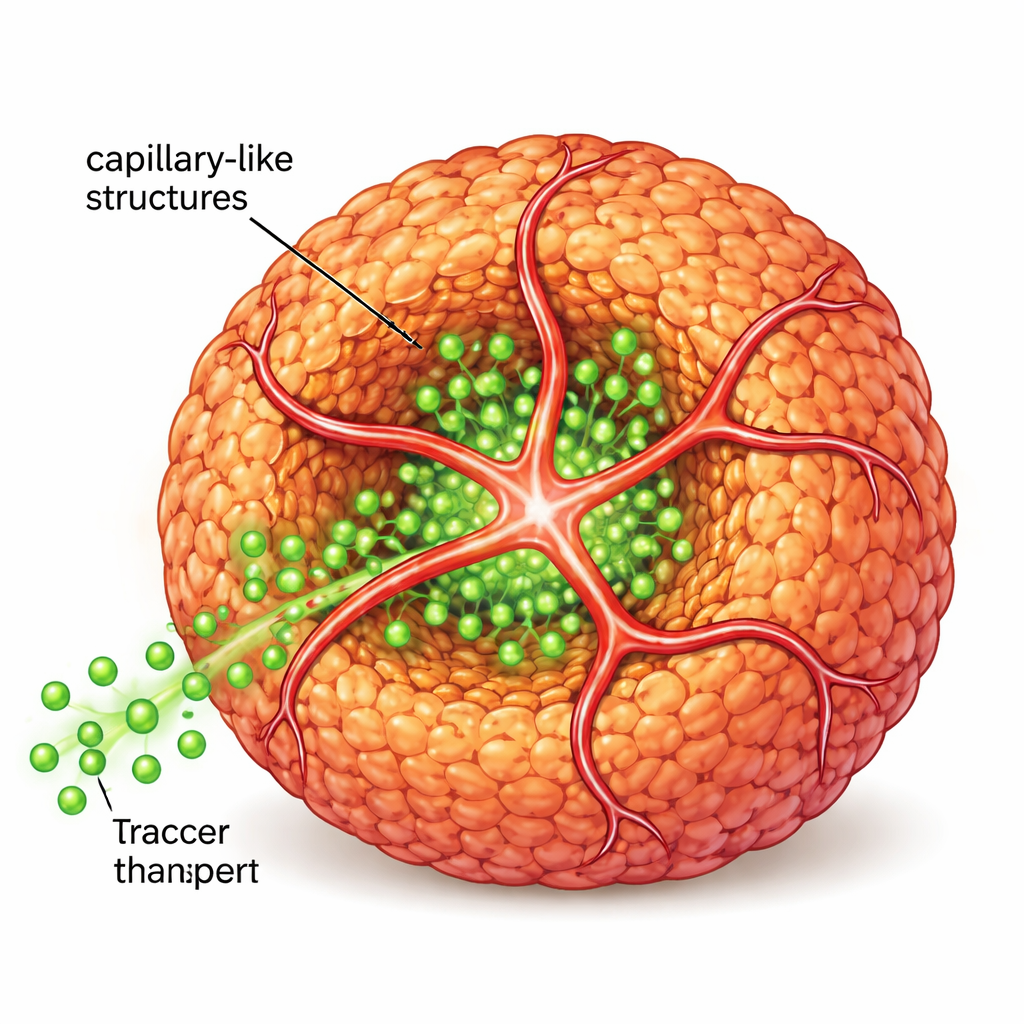
Più simili a veri tumori e agli isolotti funzionanti
L’analisi dell’attività genica ha rivelato che le sfere tumorali con strutture simili a capillari somigliavano maggiormente ai campioni di glioblastoma dei pazienti rispetto alle colture piatte tradizionali o alle sfere non vascolarizzate. Nei topi, le sfere contenenti queste reti vascolari primitive sono cresciute in tumori più grandi e maggiormente vascolarizzati, indicando che il modello in vitro cattura caratteristiche chiave del comportamento tumorale reale. La stessa strategia è stata applicata alle cellule beta pancreatiche, che normalmente vivono in isolotti altamente vascolarizzati e secernono insulina in risposta al glucosio. Quando gli isolotti di cellule beta sono stati dotati di strutture simili a capillari usando il sistema peptidico e le cellule endoteliali, hanno mostrato un rilascio di insulina molto più forte e finemente regolato, suggerendo uno strumento potente per la ricerca sul diabete e la medicina rigenerativa.
Perché questo è importante per le terapie future
Permettendo a semplici peptidi di autoassemblarsi tra cellule vive, questo lavoro offre una ricetta generale per costruire tessuti in miniatura vascolarizzati che si percepiscono e funzionano in modo più simile a quelli interni al corpo. Le sfere ottenute rispecchiano meglio i tumori dei pazienti e gli isolotti funzionali, rendendole preziose per testare farmaci, studiare i meccanismi della malattia e progettare nuove terapie a base cellulare. Per i non specialisti, il punto chiave è che dare alle cellule coltivate in laboratorio la “sensazione” corretta e piccole reti simili a vasi può migliorare drasticamente la fedeltà con cui imitano i tessuti umani, accelerando potenzialmente il percorso dalla ricerca fondamentale a trattamenti efficaci.
Citazione: Lu, H., Li, Y., Yang, X. et al. Mechanical forces from intercellular peptide self-assembly drive spheroid formation. Nat Commun 17, 1801 (2026). https://doi.org/10.1038/s41467-026-68513-1
Parole chiave: ingegneria dei tessuti, modelli tumorali, angiogenesi, organoidi, autoassemblaggio peptidico