Clear Sky Science · it
Digiuno intermittente inibisce il glioma guidato da Tp53 tramite la regolazione metionina-m6A mediata dal microbiota intestinale
Perché concedere una pausa all’intestino potrebbe rallentare tumori cerebrali letali
Il glioblastoma è uno dei tumori cerebrali più aggressivi e i trattamenti attuali—chirurgia, radioterapia e chemioterapia—spesso offrono ai pazienti solo un modesto prolungamento della sopravvivenza. Questo studio pone una domanda semplice ma potente, con grandi implicazioni per la vita quotidiana: il modo in cui mangiamo, nello specifico il digiuno intermittente, può cambiare i batteri intestinali e la chimica del sangue a sufficienza da rallentare in modo significativo alcuni tumori cerebrali?
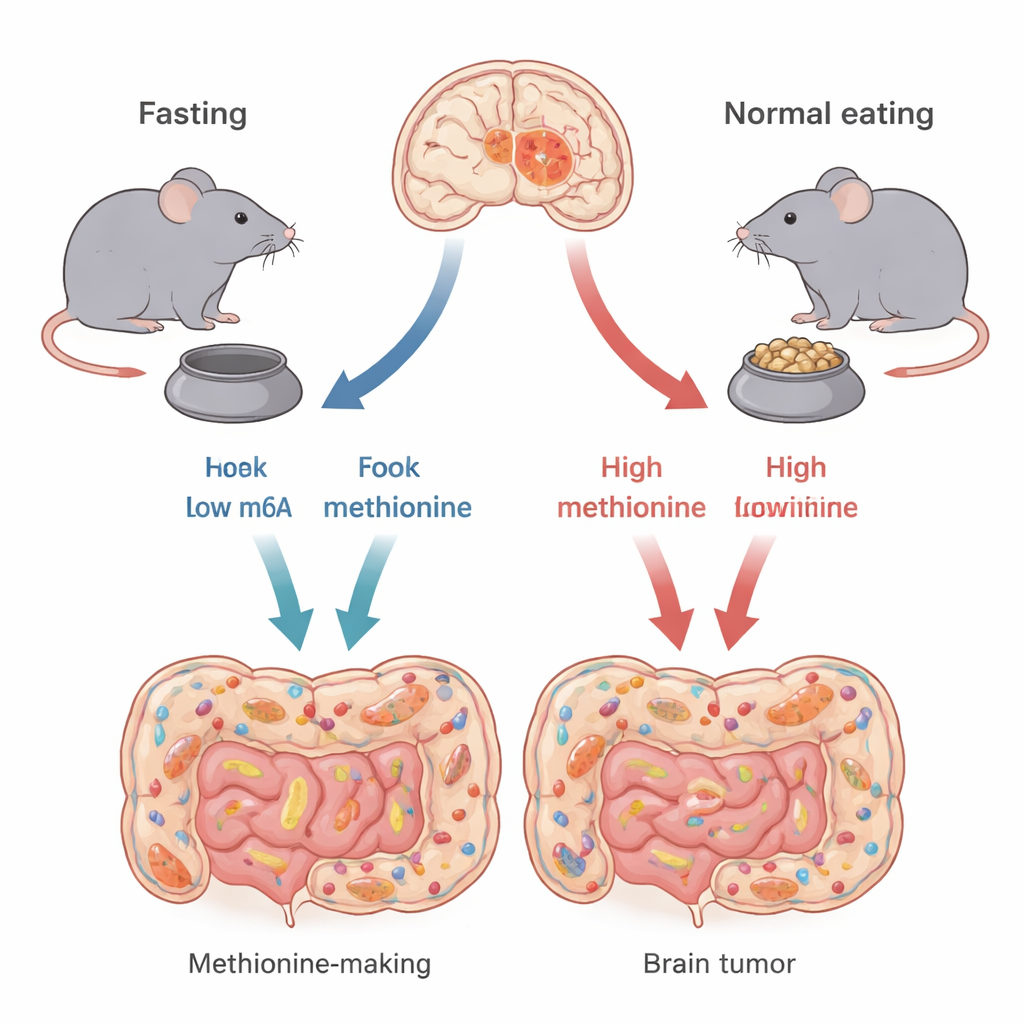
Diversi tipi dello “stesso” tumore cerebrale
Non tutti i glioblastomi sono uguali. Gli autori si concentrano su due principali tipi genetici, definiti da alterazioni nei geni chiamati TP53 e CDKN2A. Questi geni aiutano a controllare come le cellule crescono o muoiono. Usando modelli murini che riproducono fedelmente ogni sottotipo umano, i ricercatori mostrano che il digiuno intermittente—24 ore senza cibo seguite da 24 ore di alimentazione—non giova a tutti i tumori cerebrali allo stesso modo. I topi con tumori di tipo TP53 vissero più a lungo e presentarono tumori più piccoli quando digiunarono, mentre i topi con tumori di tipo CDKN2A mostrarono scarso beneficio. Ciò suggerisce che l’efficacia del digiuno può dipendere fortemente dalla “cablaggio” genetico del tumore.
Dal ritmo alimentare ai batteri intestinali fino alla chimica cerebrale
Il gruppo ha quindi indagato come il digiuno eserciti il suo effetto selettivo. Poiché la quantità totale di cibo è stata mantenuta uguale tra i gruppi, la differenza chiave era il timing dell’alimentazione. Quel ritmo rimodellò in modo significativo il microbiota intestinale—l’immensa comunità di batteri nell’intestino. Nei topi TP53 sottoposti a digiuno, alcuni gruppi batterici che producono efficacemente l’amminoacido metionina, come ceppi specifici di Alistipes e Prevotella, diminuirono in abbondanza. Poiché la metionina è un elemento essenziale che gli animali devono ottenere dalla dieta o dai microbi intestinali, questo cambiamento microbico comportò meno metionina che passava dall’intestino al flusso sanguigno e, in ultima istanza, al cervello.
Come un singolo nutriente regola segnali che favoriscono il cancro
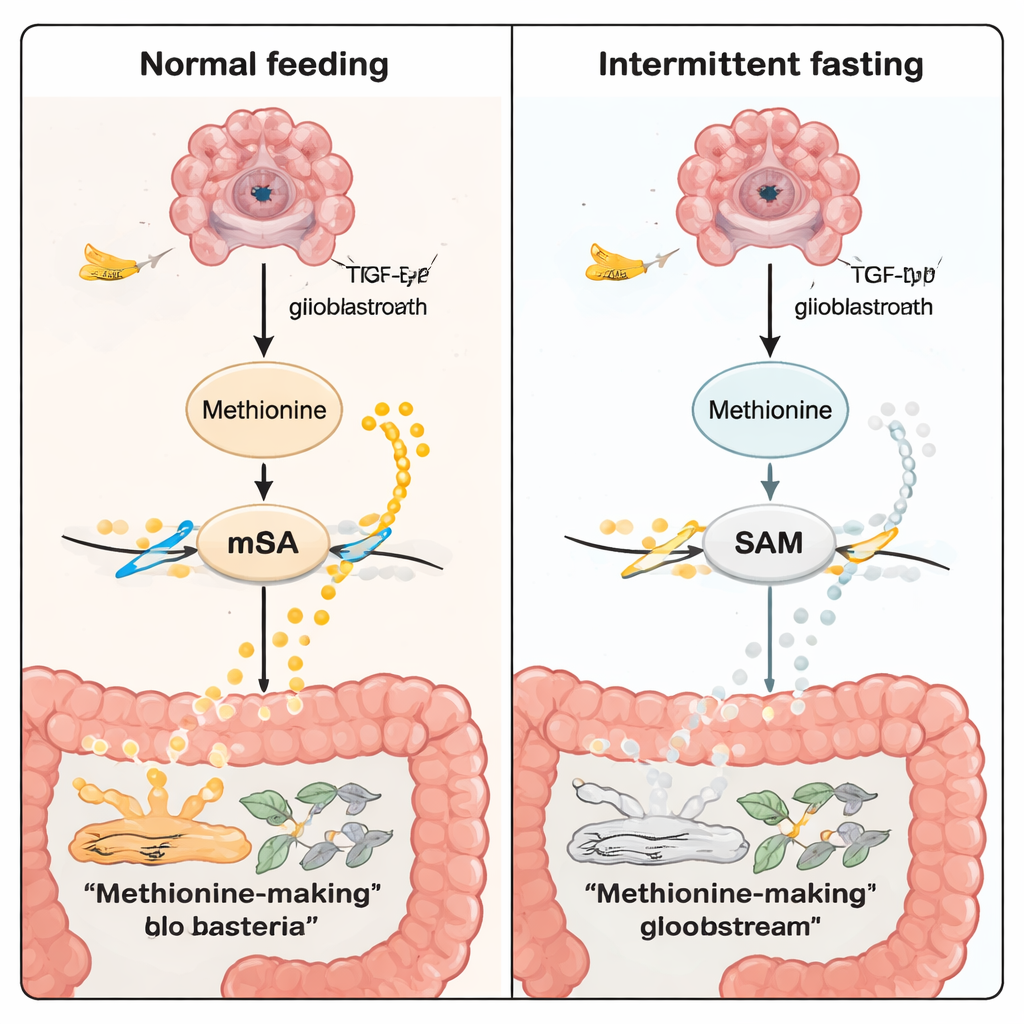
La metionina non è solo un nutriente; è anche materia prima per la S-adenosilmetionina (SAM), il “donatore di metili” universale della cellula. La SAM alimenta un processo chimico di marcatura dell’RNA chiamato m6A. Queste marche aiutano a controllare l’intensità con cui alcuni geni vengono espressi. Nel modello tumorale TP53, il digiuno ridusse i livelli di metionina e di SAM nel sangue e nelle regioni del tumore cerebrale. Utilizzando diversi livelli di tecnologie “omiche”—sequenziamento RNA standard, profiling RNA a singola cellula e mappe spaziali sia dell’attività genica sia dei metaboliti—i ricercatori osservarono un numero minore di marche m6A su RNA legati al cancro sotto digiuno. Un bersaglio importante fu TGFB2, un gene della via di segnalazione TGF‑β, noto per promuovere crescita e invasione tumorale. Con il digiuno, l’enzima METTL3 (che scrive le marche m6A) e TGFB2 risultarono entrambi ridotti, e la segnalazione TGF‑β si indebolì.
Dimostrare causa ed effetto con interventi mirati
Per andare oltre la correlazione, gli scienziati eseguirono esperimenti di “salvataggio”. Bloccarono METTL3 con un farmaco, o trasferirono batteri intestinali da topi digiuni in topi alimentati normalmente, e osservatono un rallentamento della crescita tumorale anche senza digiuno—a sostegno dell’idea che tanto il microbiota quanto il meccanismo m6A siano attori chiave. Al contrario, quando ai topi in digiuno fu somministrata metionina extra o trattati con un farmaco che aumenta le marche m6A, i loro tumori crebbero in modo simile a quelli dei topi alimentati normalmente e il vantaggio di sopravvivenza svanì. Importante, la perturbazione dei batteri intestinali con antibiotici a largo spettro cancellò molte delle modifiche legate al digiuno, sottolineando che la comunità intestinale è un hub centrale in questa catena di eventi.
Cosa significa per le persone e per le terapie future
Per un lettore non specialista, il messaggio centrale è che non tutti i tumori, né tantomeno tutti i glioblastomi, risponderanno allo stesso modo a una strategia dietetica come il digiuno intermittente. Nei gliomi di tipo TP53, il digiuno sembra “parlare” al cervello attraverso l’intestino: rimodella i batteri intestinali, che a loro volta riducono la produzione di metionina, diminuiscono le marcature chimiche sull’RNA e attenuano potenti segnali di crescita all’interno delle cellule tumorali. Pur essendo uno studio condotto sui topi e richiedendo una traduzione clinica accurata, il lavoro indica una possibile direzione futura in cui semplici schemi di vita, trattamenti basati sul microbiota intestinale e farmaci che prendono di mira la metionina o le vie m6A potrebbero essere adattati al sottotipo genetico del tumore di un paziente.
Citazione: Lin, Y., Li, S., Xu, X. et al. Intermittent fasting inhibits Tp53-driven glioma through gut microbiota-mediated methionine-m6A regulation. Nat Commun 17, 1804 (2026). https://doi.org/10.1038/s41467-026-68512-2
Parole chiave: digiuno intermittente, glioblastoma, microbioma intestinale, metabolismo della metionina, modifica RNA m6A