Clear Sky Science · it
Ossidazione del solfuro e riduzione del solfato simultanee per l'omeostasi redox intracellulare in condizioni altamente acide
Perché la pulizia dei gas tossici richiede microbi astuti
Molte industrie rilasciano idrogeno solforato, un gas velenoso dall'odore di uova marce che può corrodere le attrezzature, inquinare l'aria e danneggiare i lavoratori. Per depurarlo, gli ingegneri si affidano sempre più a microbi che trasformano il solfuro in forme di zolfo meno pericolose. Questo articolo rivela una strategia microbica inaspettata: un Mycobacterium appena identificato che porta avanti contemporaneamente due vie chimiche normalmente opposte per disintossicare rapidamente il solfuro e allo stesso tempo proteggersi dai danni intracellulari, anche in condizioni estremamente acide.
Un tiro alla fune nel ciclo dello zolfo
In natura, il ciclo dello zolfo è guidato da due reazioni opposte. Alcuni microbi ossidano il solfuro (la forma più ridotta e tossica) in prodotti meno nocivi come zolfo elementare o solfato, ottenendo energia nel processo. Altri compiono la via opposta, riducendo il solfato fino al solfuro per sintetizzare componenti cellulari essenziali come amminoacidi contenenti zolfo. Poiché queste reazioni si annullano a vicenda, i biologi hanno a lungo assunto che una singola cellula evitasse di far funzionare entrambe contemporaneamente; farlo sembrerebbe uno spreco, come riscaldare e raffreddare una casa con le finestre aperte. 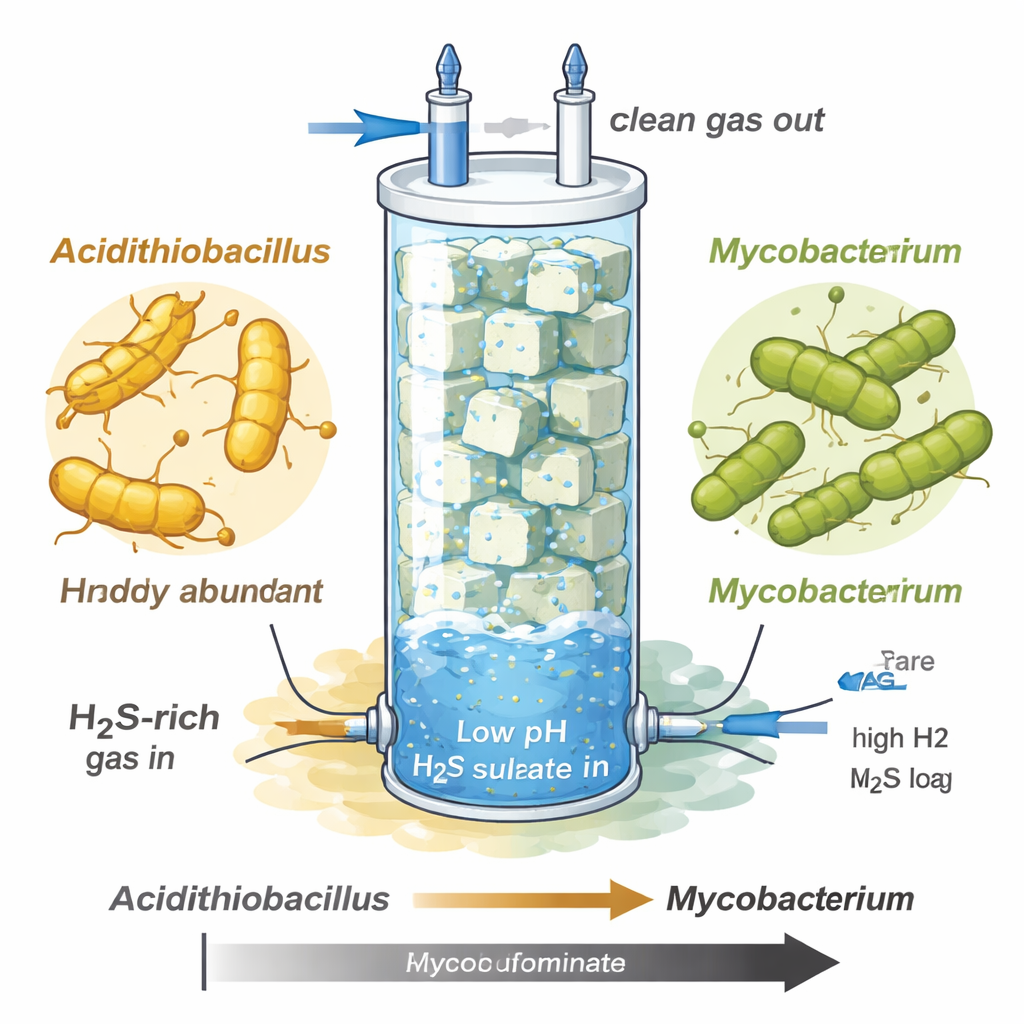
Trovare un sopravvissuto in un reattore estremo
I ricercatori hanno studiato un biotrickling filter—una colonna di vetro alta riempita di cubi di schiuma—progettata per rimuovere l'idrogeno solforato da flussi di gas simili al biogas grezzo o al gas naturale. Aumentando il carico di solfuro e mantenendo il sistema molto acido (pH intorno a 1–1,5), la comunità microbica cambiò drasticamente. All'inizio prosperava un noto ossidante di solfuro chiamato Acidithiobacillus, che convertiva gran parte del solfuro in solfato, ma poi crollò sotto lo stress estremo da solfuro. Al suo posto, una specie di Mycobacterium precedentemente non caratterizzata, etichettata MAG-M116, prese il sopravvento su quasi tutta la comunità, nonostante una crescita più lenta nella fase iniziale, meno severa.
Un microbo che rompe le regole abituali
Analisi genetiche e proteiche mostrarono che MAG-M116 possiede un assetto metabolico insolito. Contiene un enzima chiave, la solfuro:chinone ossidoreduttasi, che ossida il solfuro solo fino allo zolfo elementare solido, che si accumula sotto forma di particelle minute. Allo stesso tempo, il microbo ha un set completo di geni per la riduzione assimilativa del solfato, la via che incorpora il solfato nella cellula e lo riduce per costruire amminoacidi come cisteina e metionina. In condizioni di alto contenuto di solfuro, entrambe le vie risultarono attivate contemporaneamente. L'ossidazione del solfuro immetteva elettroni nella macchina energetica della cellula, mentre la riduzione del solfato assorbiva parte di quel flusso elettronico, collegando le due direzioni del ciclo dello zolfo all'interno di una singola cellula.
Trasformare un ciclo “sprecone” in una valvola di sicurezza
Eseguire entrambe le vie contemporaneamente potrebbe, in teoria, essere futile—bruciare energia senza guadagno netto. Ma il gruppo dimostra che per MAG-M116 ciò funge da valvola di sicurezza per gli elettroni in eccesso. L'ossidazione di grandi quantità di solfuro rilascia una scarica di elettroni nella catena respiratoria della cellula, che può fuoriuscire e generare specie reattive dell'ossigeno (ROS)—molecole dannose che attaccano DNA, proteine e membrane. Riducendo attivamente il solfato in amminoacidi, la cellula devia il 10–14% di quegli elettroni verso lavoro costruttivo, riducendo l'accumulo di uno stato eccessivamente ridotto e soggetto a perdite. Esperimenti che confrontavano condizioni con e senza solfato mostrarono che la riduzione attiva del solfato riduceva la produzione di ROS fino a circa il 60% e preveniva l'accumulo di cofattori ridotti che altrimenti alimenterebbero danni ossidativi. 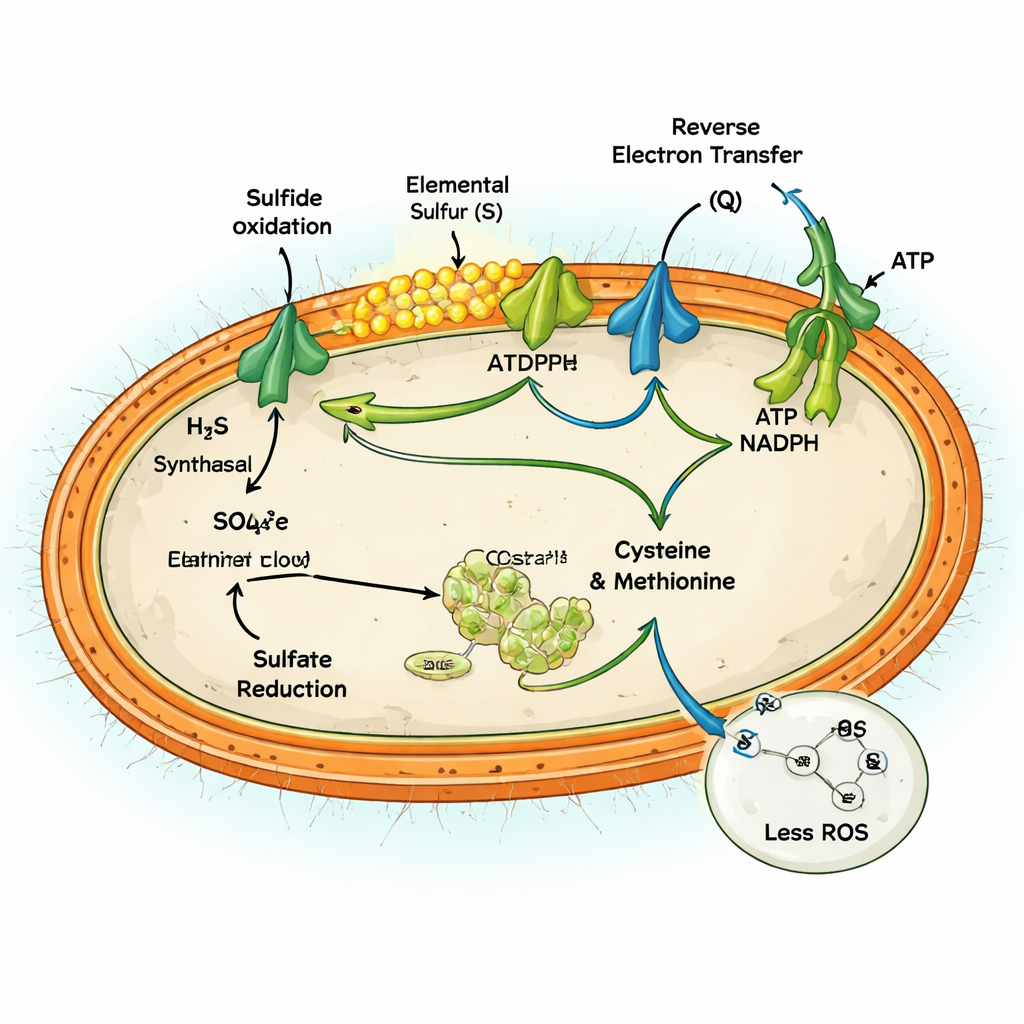
Dal gas tossico a prodotti utili
Nelle fasi successive del funzionamento del reattore, quando MAG-M116 dominava, quasi tutto l'idrogeno solforato in ingresso veniva convertito in zolfo elementare solido, anziché in solfato. Allo stesso tempo, i ricercatori rilevarono livelli crescenti di cisteina e metionina nella fase liquida, suggerendo che il microbo rilasciasse amminoacidi ricchi di zolfo in eccesso nel suo ambiente. Questa combinazione—zolfo elementare stabile più composti organici dello zolfo di valore—trasforma un tempo un inquinante pericoloso in una miscela di prodotti recuperabili con impieghi in agricoltura, materiali e sistemi energetici.
Cosa significa per la salute e la tecnologia
Per un non specialista, il messaggio chiave è che questo Mycobacterium ha risolto un doppio problema: può rimuovere elevate concentrazioni di un gas tossico mantenendo al contempo l'equilibrio chimico interno. Lo fa eseguendo reazioni dello zolfo “push–pull” che normalmente sarebbero tenute separate, utilizzando il ciclo apparentemente sprecone come ammortizzatore integrato per gli elettroni in eccesso e i radicali ossigeno dannosi. Questa scoperta non solo suggerisce nuovi modi per progettare bioreattori robusti a basso pH per la rimozione di solfuro e solfato, ma lascia anche intendere che microbi affini, comprese specie di Mycobacterium patogene, possano usare trucchi simili per sopravvivere ad attacchi ossidativi all'interno del corpo umano.
Citazione: Jia, T., Peng, Y., Niu, L. et al. Simultaneous sulfide oxidation and sulfate reduction for intracellular redox homeostasis under highly acidic conditions. Nat Commun 17, 1797 (2026). https://doi.org/10.1038/s41467-026-68508-y
Parole chiave: ciclo dello zolfo, idrogeno solforato, Mycobacterium, omeostasi redox, biodesolforizzazione