Clear Sky Science · it
Sintesi elettrochimica selettiva dell'urea da nitrato e anidride carbonica a basso sovratensione
Trasformare i rifiuti in fertilizzante
L’agricoltura moderna dipende fortemente dall’urea come fertilizzante, ma la sua produzione convenzionale consuma molta energia fossile e rilascia grandi quantità di anidride carbonica. Questo studio esplora una via più pulita: usare elettricità e materiali appositamente progettati per convertire direttamente anidride carbonica e nitrato—entrambi inquinanti comuni—in urea a condizioni miti. Se scalata, una simile procedura potrebbe aiutare a nutrire la popolazione riducendo le emissioni di gas serra e valorizzando flussi di rifiuto.
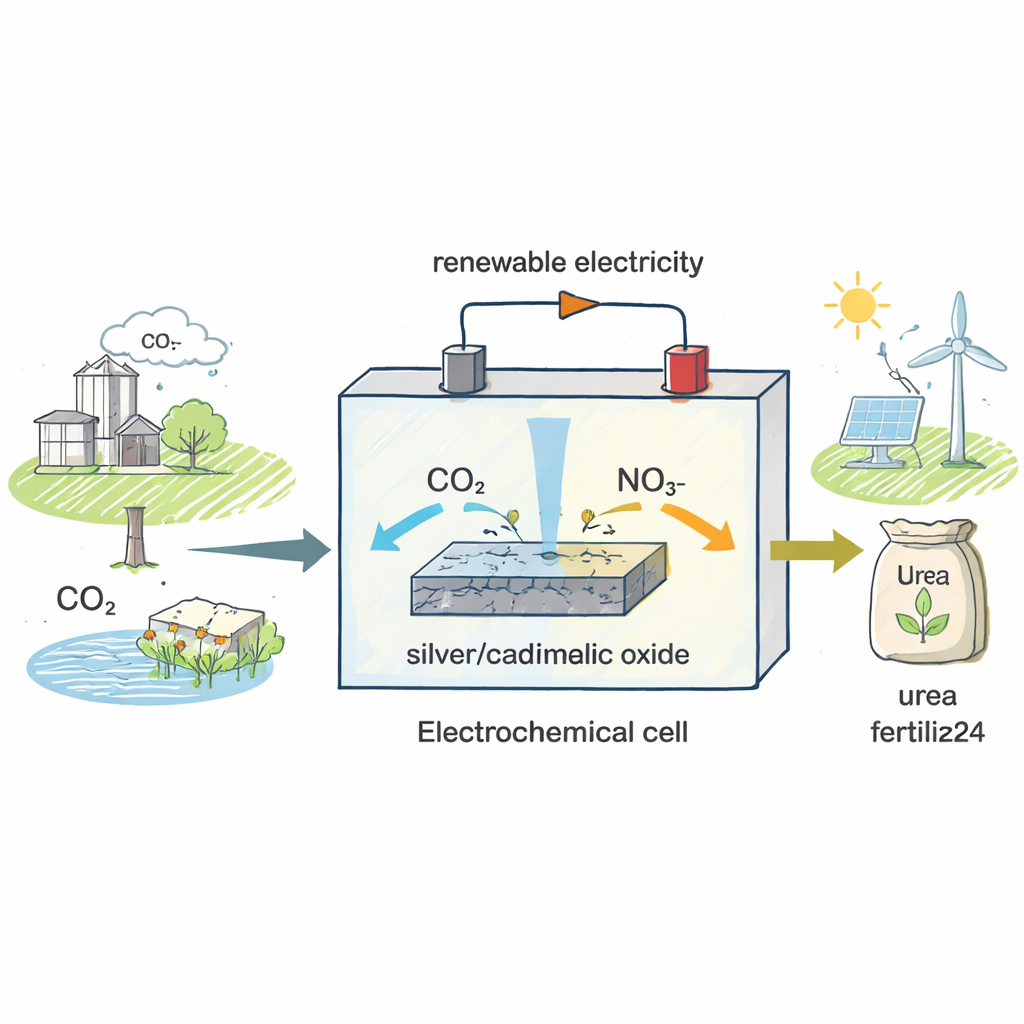
Un nuovo modo per produrre un vecchio fertilizzante
Le attuali fabbriche di urea operano a temperature e pressioni elevate e si basano sulla produzione preventiva di ammoniaca da azoto gassoso, un passaggio che da solo consuma oltre il 2% dell’energia globale. Gli autori si sono proposti di eludere questo percorso energivoro. Invece di partire dall’azoto gassoso, impiegano il nitrato, un composto dell’azoto presente nelle acque di dilavamento agricole e nelle acque reflue industriali, e lo combinano con l’anidride carbonica, il principale gas serra. Entrambe le sostanze vengono alimentate in una cella elettrochimica—un dispositivo in cui l’elettricità guida reazioni chimiche—così che, con il catalizzatore giusto, possano essere unite in urea a temperatura ambiente e a voltaggi relativamente bassi.
Progettare una superficie efficace
Il cuore del dispositivo è un catalizzatore solido costituito da particelle minute che combinano argento (Ag) con ossido di cadmio (CdO). Microscopia e tecniche a raggi X mostrano che queste particelle formano “eterostrutture” intime, in cui l’argento metallico e il CdO sono a contatto alla scala nanometrica e scambiano elettroni. Questa interazione elettronica altera sottilmente il modo in cui ciascun componente lega le molecole in arrivo. In condizioni operative, la porzione di CdO si riconverte in carbonato di cadmio (CdCO₃) contenente atomi di ossigeno mancanti, noti come vacanze di ossigeno. Questi siti vuoti funzionano come piccoli punti di ormeggio che aiutano a catturare e attivare l’anidride carbonica, mentre le regioni di argento vicine sono particolarmente efficaci nell’afferrare specie contenenti azoto derivate dal nitrato.
Produrre urea in modo efficiente e selettivo
Quando anidride carbonica e nitrato scorrono su questo catalizzatore Ag/CdO in una cella di laboratorio, il materiale li converte in urea a una sovratensione insolitamente bassa, ovvero la tensione aggiuntiva oltre il requisito termodinamico ideale è ridotta. In una semplice cella a forma di H, la composizione ottimizzata, chiamata Ag₀.₀₇/CdO, raggiunge una selettività per l’urea di circa il 50% a soli −0,10 volt rispetto a un riferimento standard, producendo poca ammoniaca o monossido di carbonio come sottoprodotti. In una cella a flusso più avanzata, dove gas e liquidi sono forniti continuamente, lo stesso catalizzatore ottiene un elevato tasso di produzione di urea di circa 112 millimoli per grammo di catalizzatore all’ora a −0,15 volt. Ottimizzando ulteriormente il design del reattore e le condizioni operative, il team aumenta il tasso di produzione a circa 427 millimoli per grammo all’ora a correnti più elevate, mantenendo le prestazioni per 1.000 ore di operazione continua—un segnale importante di stabilità.
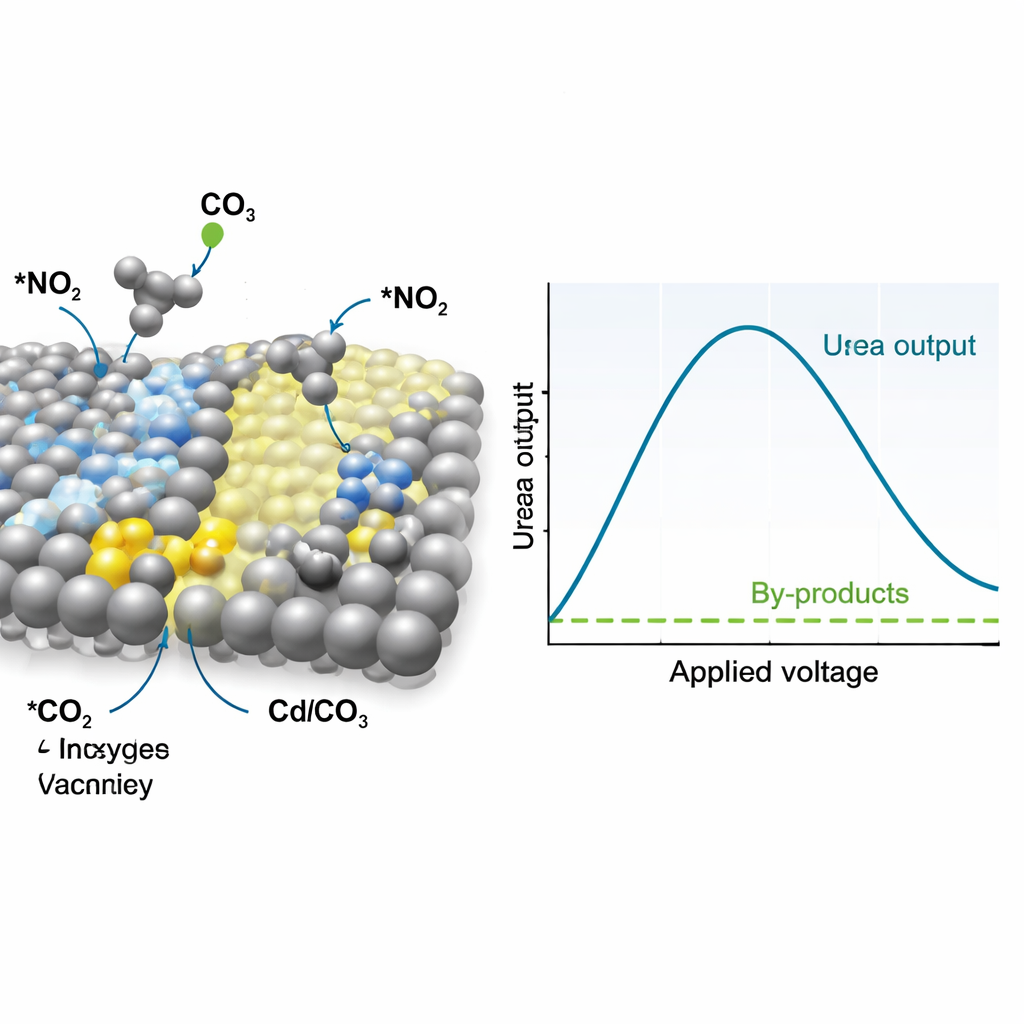
Come il catalizzatore guida la reazione
Per capire perché questo materiale funziona così bene, i ricercatori hanno seguito in tempo reale il catalizzatore e gli intermedi della reazione usando spettroscopia Raman e infrarossa, insieme a sonde avanzate a raggi X. Queste misure indicano che i siti di argento convertono preferenzialmente il nitrato in un intermedio reattivo spesso descritto come *NO₂, mentre il CdCO₃ ricostruito con vacanze di ossigeno lega l’anidride carbonica e la trasforma in *CO, un altro intermedio di breve durata. A tensioni operative compaiono segnali associati a legami carbonio–azoto, mostrando che *NO₂ e *CO si accoppiano nelle fasi iniziali per formare una specie simile all’urea piuttosto che disperdersi per formare separatamente ammoniaca o monossido di carbonio. Simulazioni al computer supportano questo quadro, rivelando che l’interfaccia tra l’argento e il CdCO₃ ricco di vacanze abbassa la barriera energetica per questo passo chiave di accoppiamento C–N e lo rende più favorevole rispetto a reazioni concorrenti.
Cosa può significare per fertilizzanti e clima
Nel complesso, il lavoro dimostra che superfici catalitiche progettate con cura possono indirizzare molecole di scarto semplici come anidride carbonica e nitrato lungo una via energeticamente efficiente verso l’urea, a condizioni miti e con lunga durata. Per un non specialista, la conclusione principale è che il team ha costruito una sorta di “filtro elettronico” che preferisce unire carbonio e azoto in urea piuttosto che lasciarli sfuggire come altri prodotti. Sebbene l’applicazione su scala reale richiederà di affrontare questioni quali il costo dei materiali, l’ingegneria dei reattori e la gestione sicura del cadmio, lo studio offre un progetto esemplare per una futura produzione di fertilizzanti che potrebbe essere alimentata da elettricità rinnovabile e integrata in un ciclo del carbonio e dell’azoto più sostenibile.
Citazione: Liu, S., Wang, T., Liu, J. et al. Selective electrosynthesis of urea from nitrate and carbon dioxide with low overpotential. Nat Commun 17, 1787 (2026). https://doi.org/10.1038/s41467-026-68497-y
Parole chiave: sintesi elettrochimica dell'urea, utilizzo dell'anidride carbonica, riduzione del nitrato, progettazione di elettrocatalizzatori, fertilizzante verde