Clear Sky Science · it
Identificazione di peptidi antimicrobici nei microbiomi intestinali antichi
Scavare indizi antichi per combattere i germi moderni
Con l’aumento della resistenza antibiotica in tutto il mondo, i medici stanno esaurendo le opzioni per trattare infezioni pericolose. Questo studio adotta un approccio insolito: non punta ai laboratori di chimica ad alta tecnologia, ma ai resti fossilizzati di feci umane—«capsule del tempo» dell’intestino—per scoprire molecole naturali contro i germi che potrebbero essere ancora efficaci contro i batteri odierni.
Microbi antichi come armadi dei medicinali nascosti
Molto prima della medicina moderna, l’intestino umano era già un campo di battaglia in cui microbi utili e germi invasori competevano per spazio e nutrimento. Molti batteri intestinali amichevoli producono peptidi antimicrobici—brevi frammenti proteici che possono perforare le cellule batteriche o disabilitarle in altri modi. La ricerca moderna ha cercato prevalentemente questi peptidi nei microbiomi attuali. Ma le comunità intestinali contemporanee si sono evolute insieme all’uso di antibiotici e agli stili di vita moderni, offrendo ai batteri dannosi molte opportunità di sviluppare resistenza. Per contro, le comunità intestinali antiche, preservate in feci essiccate chiamate coproliti, si sono formate in un mondo senza antibiotici da prescrizione. Questo le rende una promettente fonte di difese «dimenticate» che i patogeni moderni potrebbero non aver ancora imparato a eludere.
Uno strumento AI leggero per leggere il DNA fossilizzato
Per esplorare questa farmacia antica, i ricercatori hanno sviluppato un nuovo strumento informatico chiamato AMPLiT (AMP Lightweight Identification Tool). Anziché richiedere grandi supercomputer, AMPLiT funziona in modo efficiente su un normale portatile pur mantenendo alta accuratezza. Scansiona enormi dataset di DNA provenienti da campioni di microbioma e segnala brevi sequenze che probabilmente codificano peptidi antimicrobici. Il team ha messo a punto il design di AMPLiT in modo che potesse gestire milioni di frammenti provenienti da DNA danneggiato e secolare in poche ore, riducendo i tempi di addestramento di circa l’80% rispetto ai metodi precedenti, pur mantenendo prestazioni quasi allo stato dell’arte nell’individuare i candidati potenzialmente in grado di uccidere i germi.
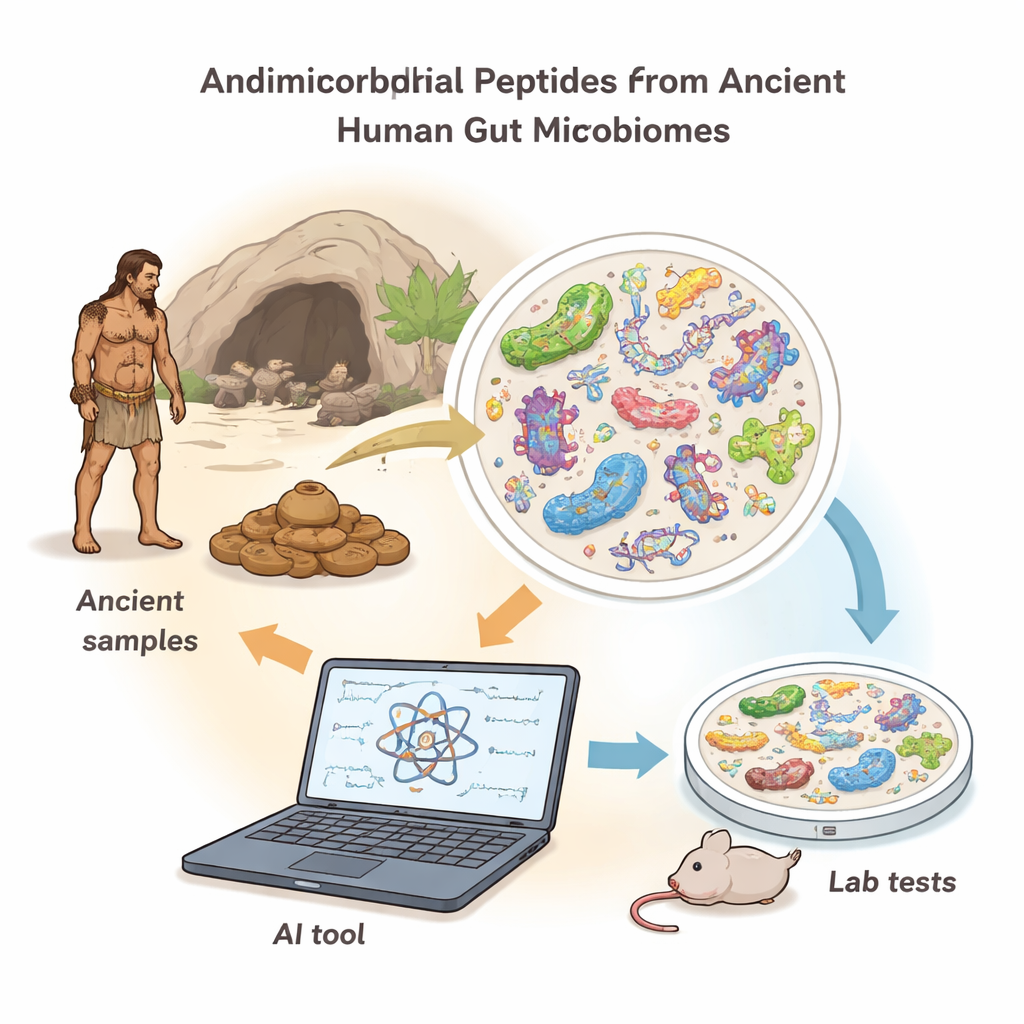
Resuscitare killer dei germi da un abitante intestinale antico
Usando AMPLiT, gli scienziati hanno esaminato il DNA intestinale di sette antichi individui umani vissuti 1.000–2.000 anni fa in Nord America. Dopo aver rimosso le contaminazioni ambientali e concentrato l’attenzione su lunghezze peptidiche brevi e pratiche, lo strumento ha previsto centinaia di migliaia di possibili sequenze antimicrobiche. Una serie più rigorosa di filtri—presenza in più individui, proprietà chimiche e bassa tossicità predetta—ha ridotto il numero a 41 candidati ad alta confidenza, 40 dei quali potevano essere sintetizzati chimicamente in laboratorio. Testati contro batteri sia «Gram-positivi» sia «Gram-negativi» (due grandi gruppi che includono molti patogeni comuni), 36 dei 40 peptidi hanno rallentato o arrestato la crescita batterica a dosi relativamente basse, un tasso di successo insolito per questo tipo di ricerca.
La stella sorprendente: un alleato intestinale in via di sparizione
Circa due terzi dei peptidi più attivi provenivano da un singolo batterio intestinale: Segatella copri, un parente vicino di un microbo precedentemente classificato come Prevotella copri. Questa specie era abbondante negli intestini antichi ed è ancora comune in persone con diete più tradizionali e meno industrializzate, ma oggi è rara in molte popolazioni urbane di stampo occidentale. Tracciando la posizione dei geni peptidici nel genoma di Segatella, il team ha scoperto che la maggior parte sono in realtà frammenti di geni più grandi, «di servizio» quotidiano, che il microbo sembra aver riciclato come armi—un trucco evolutivo efficiente. Molti di questi peptidi antichi appaiono molto diversi da quelli presenti nei database moderni, suggerendo che rappresentano progetti chimici genuinamente nuovi, non semplici variazioni su antibiotici già noti.
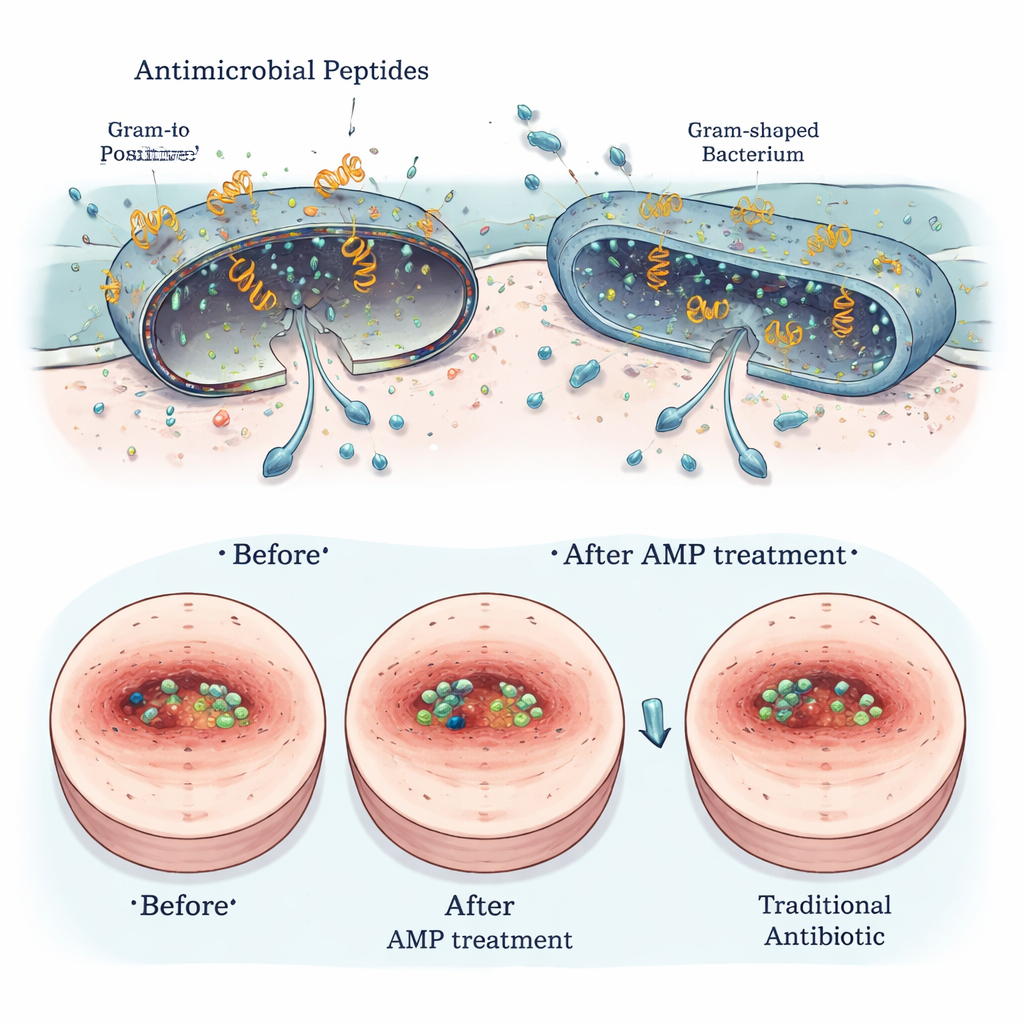
Sicuri per l’ospite, aggressivi con i batteri—e promettenti nelle ferite
Diversi dei peptidi di Segatella più promettenti sono stati testati per sicurezza e utilità nel mondo reale. In vitro, hanno causato pochi o nessun danno ai globuli rossi e solo effetti lievi, se presenti, su cellule simili a quelle intestinali umane. La microscopia ad alta risoluzione ha mostrato che i peptidi danneggiano fisicamente le membrane esterne dei batteri dannosi, risparmiando le cellule dei mammiferi. In modelli di ferite infette su roditori, l’applicazione cutanea di peptidi selezionati ha ridotto il carico batterico, accelerato la chiusura delle ferite e attenuato i segni di infiammazione, con prestazioni comparabili ad antibiotici consolidati come vancomicina e polimixina B, specialmente contro batteri Gram-positivi come Staphylococcus aureus.
Che cosa significa per i farmaci del futuro
Per un non specialista, il messaggio è chiaro: i microbi intestinali dei nostri antenati potrebbero contenere progetti per nuovi antibiotici ancora efficaci contro le infezioni difficili da trattare oggi. Questo studio mostra che con strumenti AI intelligenti ed efficienti come AMPLiT, gli scienziati possono estrarre dal DNA antico peptidi antimicrobici potenti e relativamente benigni per le cellule umane. Sebbene restino molti passaggi prima che una di queste molecole diventi un farmaco, il lavoro suggerisce che resuscitare partner microbici «persi» come Segatella copri—o almeno prendere in prestito le loro armi molecolari—potrebbe aiutare a reintegrare il nostro arsenale in diminuzione contro i batteri resistenti.
Citazione: Chen, S., Yuan, Y., Wang, Y. et al. Identification of antimicrobial peptides from ancient gut microbiomes. Nat Commun 17, 1788 (2026). https://doi.org/10.1038/s41467-026-68495-0
Parole chiave: peptidi antimicrobici, microbioma antico, Segatella copri, resistenza agli antibiotici, mining metagenomico