Clear Sky Science · it
Colpire la cascata UFL1-AKT reprime la progressione del carcinoma mammario triple-negative
Perché questa ricerca conta
Il carcinoma mammario triple-negative (TNBC) è una delle forme più letali di tumore al seno perché manca dei recettori ormonali e dei percorsi di crescita su cui si basano molti farmaci moderni. I pazienti spesso ricevono solo chemioterapia tradizionale, che può perdere efficacia quando i tumori sviluppano resistenze. Questo studio mette in luce un “motore” molecolare finora nascosto che aiuta le cellule TNBC a crescere e a resistere alla chemioterapia, e propone un nuovo tipo di farmaco che blocca direttamente questo motore.
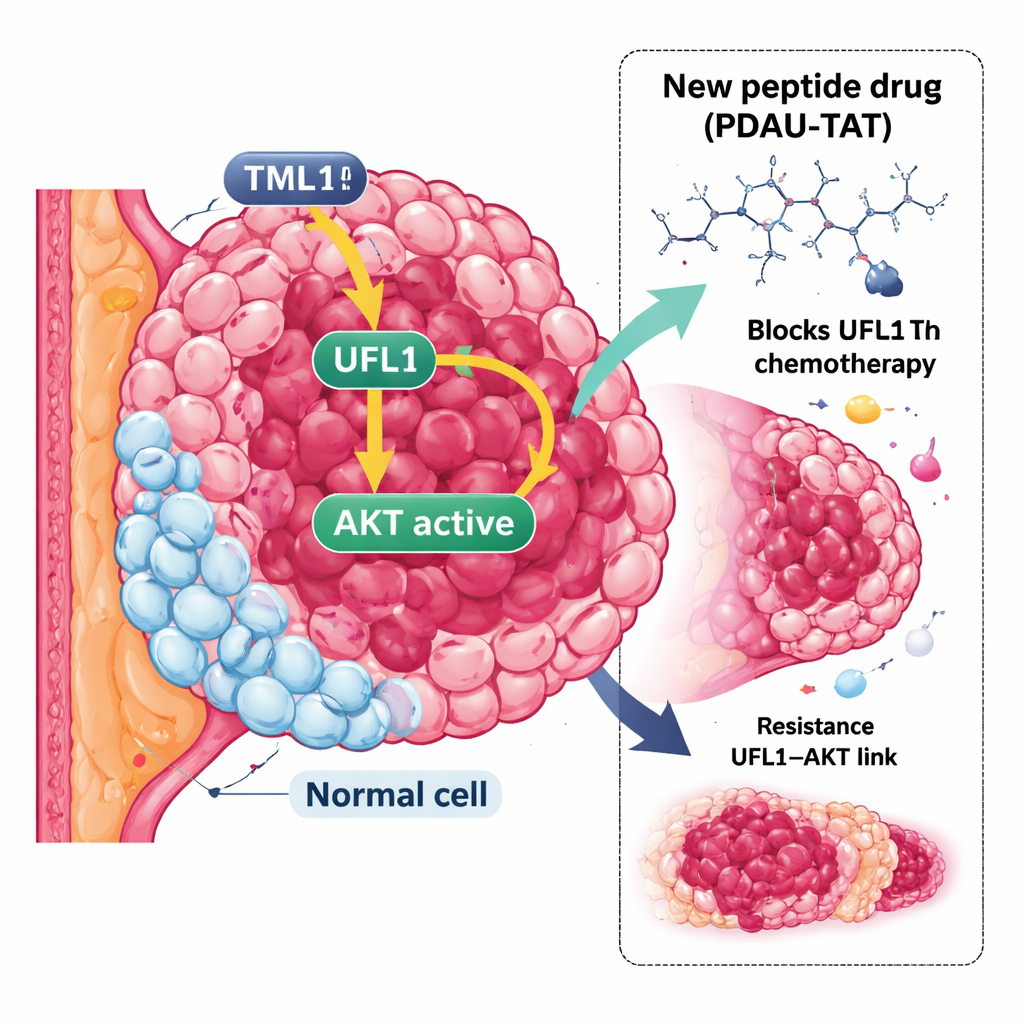
Una forma ostinata di tumore al seno
Il TNBC è definito dall’assenza di tre marcatori comuni: il recettore per gli estrogeni, il recettore per il progesterone e il recettore di crescita HER2. Senza questi marcatori, molte terapie mirate efficaci semplicemente non si applicano. Al loro posto si utilizzano farmaci standard come cisplatino e doxorubicina, ma i tumori TNBC spesso resistono o si adattano rapidamente a questi trattamenti e hanno una maggiore tendenza a metastatizzare. Ciò crea un’urgenza di strategie nuove che vadano oltre i bersagli abituali e cerchino altre vulnerabilità nei sistemi di controllo del tumore.
Una proteina poco nota con grande impatto
I ricercatori si sono concentrati su UFL1, una proteina che attacca un piccolo segnale, chiamato UFM1, ad altre proteine in un processo noto come UFMilazione. Questo sistema di marcatura è stato scoperto solo di recente e il suo ruolo nel cancro è stato poco chiaro e a volte contraddittorio. Analizzando dati di pazienti e campioni tumorali, il gruppo ha dimostrato che UFL1 è significativamente elevato nel TNBC rispetto al tessuto mammario normale. Quando hanno ridotto i livelli di UFL1 in linee cellulari TNBC e in modelli tumorali murini, le cellule cancerose si sono moltiplicate più lentamente e sono diventate molto più sensibili alla chemioterapia, suggerendo che UFL1 svolge un ruolo promotore del tumore in questo contesto.
Collegare UFL1 a un interruttore maestro della crescita
Approfondendo, gli scienziati hanno scoperto che UFL1 si lega direttamente ad AKT, una proteina di segnalazione centrale che guida crescita cellulare, sopravvivenza e metabolismo ed è spesso iperattiva nei tumori. Nel TNBC, AKT è frequentemente sovraattivato anche in assenza delle mutazioni a monte di solito implicate. Il team ha trovato che UFL1 marca chimicamente AKT in tre posizioni specifiche, il che rende più facile l’attivazione di AKT da parte dei suoi partner attivanti, proteggendolo al contempo dagli enzimi che normalmente lo disattiverebbero. Le cellule prive di UFL1 o che esprimevano una forma ingegnerizzata di AKT incapace di ricevere questi segnali hanno mostrato attività AKT molto più bassa, crescita rallentata e maggiore vulnerabilità alla chemioterapia sia in colture cellulari sia in modelli animali.
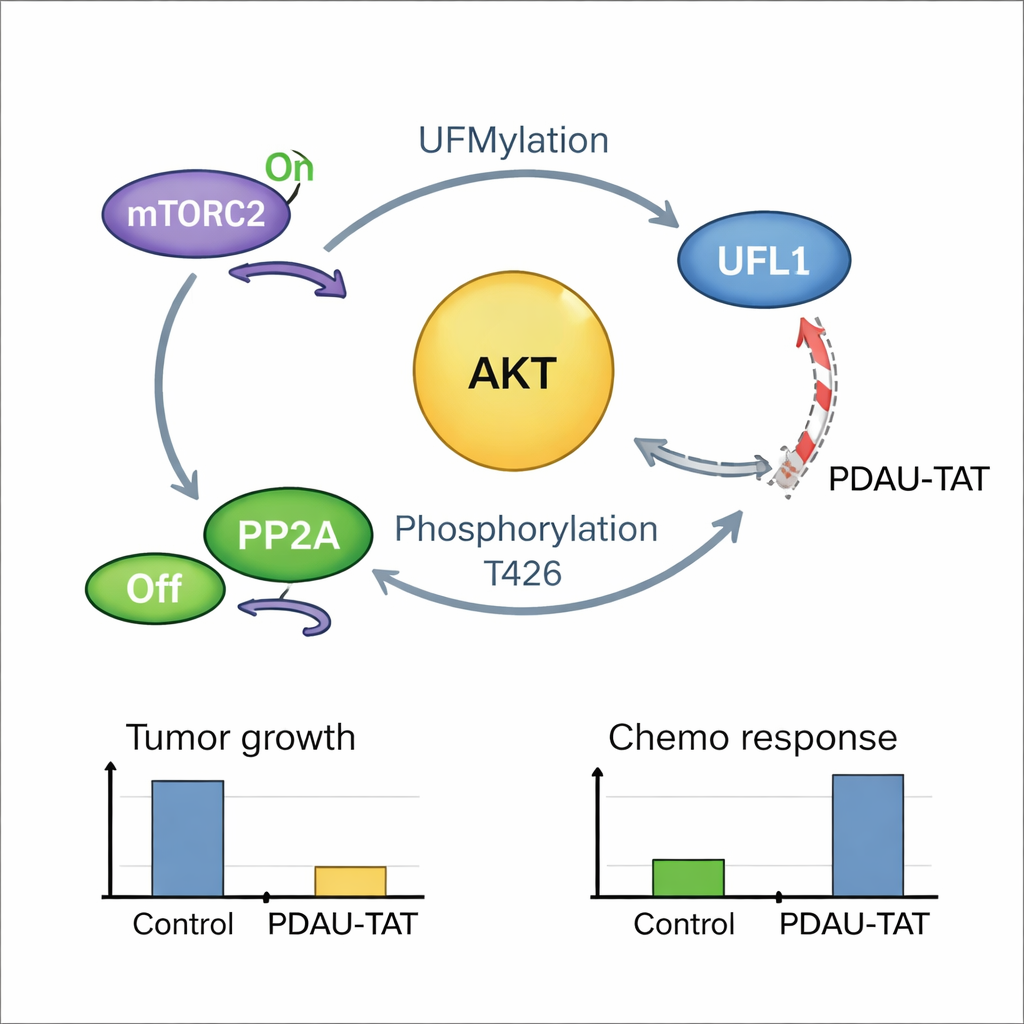
Un circuito tumorale auto‑rinforzante e come spezzarlo
La storia si è rivelata ancora più intrecciata: una volta che AKT è attivato, esso retroagisce e modifica UFL1 in un sito cruciale, potenziando l’attività di marcatura di UFL1 su AKT e altri bersagli. Questo crea un circuito di feedback positivo in cui UFL1 attiva AKT e AKT attivo, a sua volta, potenzia UFL1. I campioni tumorali dei pazienti hanno mostrato che alti livelli di UFL1 modificato correlano fortemente con alti livelli di AKT attivo, a supporto dell’esistenza di questo circuito nella malattia umana. Per sfruttare questa vulnerabilità, il gruppo ha progettato un breve peptide capace di penetrare nelle cellule, chiamato PDAU-TAT, che imita una piccola regione di UFL1 e si inserisce tra UFL1 e AKT. Questo peptide interrompe la loro interazione, riduce l’attivazione di AKT, rallenta la crescita tumorale e rende le cellule TNBC e i tumori derivati da pazienti più sensibili alla chemioterapia, il tutto senza danni evidenti agli organi principali nei topi.
Cosa potrebbe significare per i pazienti
In termini semplici, i ricercatori hanno scoperto un cablaggio nascosto all’interno delle cellule TNBC: UFL1 e AKT sono intrappolati in un circuito autoamplificante che mantiene i segnali di crescita in posizione “accesa” e aiuta i tumori a resistere ai trattamenti. Costruendo un piccolo peptide che si inserisce in questo circuito e scollega UFL1 da AKT, mostrano un modo plausibile per indebolire i tumori TNBC risparmiando le cellule normali, che tendono ad avere livelli più bassi di UFL1. Sebbene questo lavoro sia ancora in fase preclinica, indica una nuova classe di terapie mirate non dirette ai recettori abituali ma alle connessioni proteina‑proteina che alimentano alcuni dei carcinomi mammari più aggressivi.
Citazione: Yang, X., Wen, Y., Ma, X. et al. Targeting the UFL1-AKT cascade suppresses triple-negative breast cancer progression. Nat Commun 17, 613 (2026). https://doi.org/10.1038/s41467-026-68493-2
Parole chiave: carcinoma mammario triple-negative, segnalazione AKT, UFMilazione, UFL1, peptide terapia oncologica