Clear Sky Science · it
Il circuito di retroazione positivo UFL1‑AKT promuove la progressione del cancro al seno potenziando la sintesi lipidica
Perché le cellule tumorali danno tanta importanza ai grassi
Le cellule del cancro al seno, come tutte le cellule a rapida crescita, necessitano di un rifornimento costante di mattoni per costruire nuove membrane e molecole di segnalazione. I grassi, o lipidi, sono una componente chiave di questo rifornimento. Questo studio svela come un sistema proteico poco noto spinga le cellule tumorali in una "modalità di produzione di grassi" accelerata, favorendo la crescita del tumore e la resistenza ai trattamenti. Comprendere questa linea di carburante nascosta potrebbe aprire nuove strade per rallentare o affamare i tumori mammari.
Un marcatore proteico nascosto con grandi conseguenze
Le nostre cellule regolano continuamente il comportamento delle loro proteine usando piccole etichette chimiche. Una di queste etichette, chiamata UFM1, è aggiunta da un enzima denominato UFL1. L’etichettatura con UFM1 (UFMilazione) è stata collegata alla riparazione del DNA e alle risposte allo stress, ma il suo ruolo nel cancro era poco chiaro. Gli autori mostrano che UFL1 è molto più attivo nei tumori mammari umani rispetto al tessuto mammario normale, in tutti i sottotipi principali. I pazienti i cui tumori presentano livelli più elevati di UFL1 tendono ad avere una sopravvivenza peggiore. Quando i ricercatori hanno ridotto UFL1 in cellule di cancro al seno o in tumori murini, la crescita tumorale rallentava, la divisione cellulare diminuiva e la morte cellulare aumentava, suggerendo che UFL1 si comporta come un fattore che promuove il cancro.
Come un centro di segnalazione viene convertito in modalità produttiva di lipidi
Per capire come UFL1 favorisca i tumori, il gruppo ha cercato i suoi partner molecolari e ha individuato una proteina chiave di controllo della segnalazione chiamata AKT1. AKT1 è un interruttore centrale che istruisce le cellule a crescere e a sintetizzare nuovi lipidi. Lo studio dimostra che UFL1 si lega fisicamente ad AKT1 e lo decora con tag UFM1 in diversi siti specifici. Questa etichettatura modifica la conformazione di AKT1, allentando un "freno" interno che normalmente lo mantiene inattivo. Aiuta inoltre AKT1 a trasferirsi in un compartimento di membrana all’interno della cellula, il reticolo endoplasmatico, dove altri enzimi possono attivarlo completamente aggiungendo gruppi fosfato. In assenza delle etichette UFM1 in quei siti, AKT1 è molto più difficile da attivare.
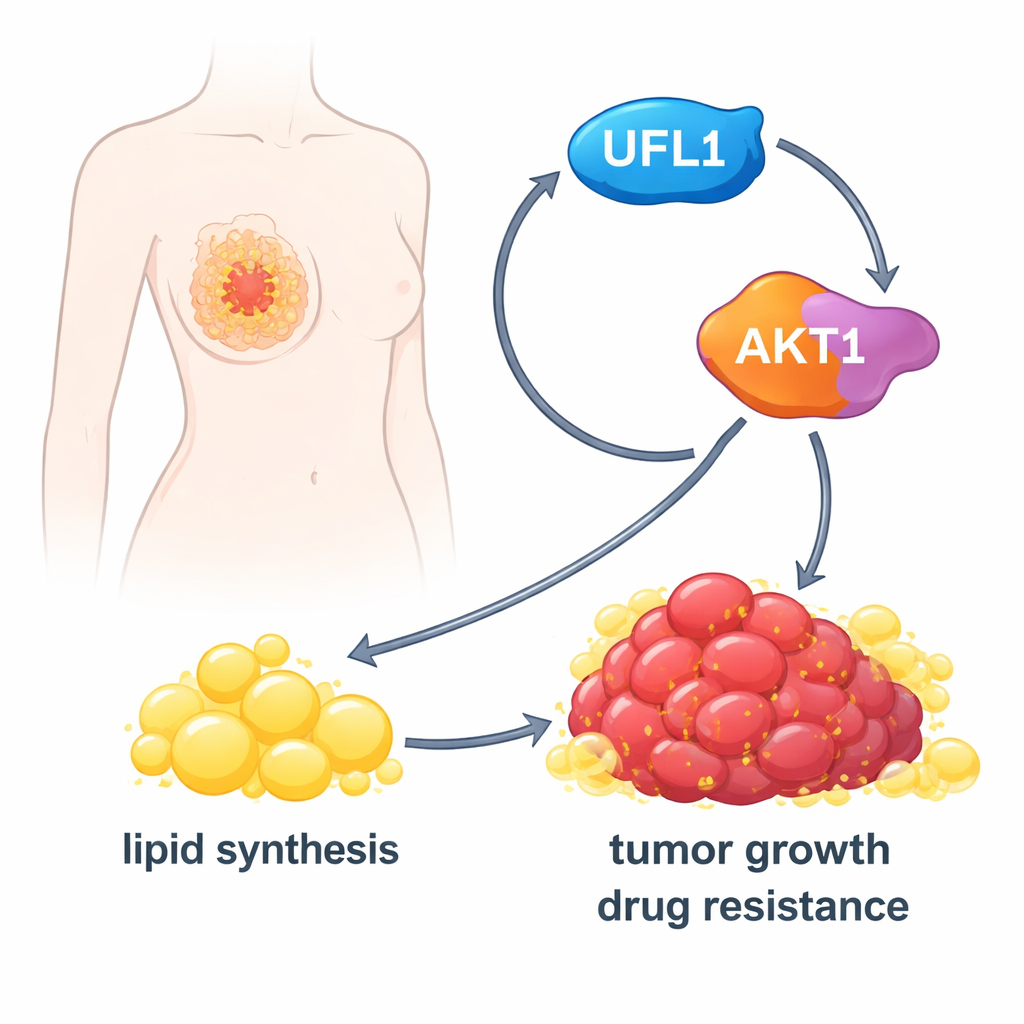
Accendere la fabbrica di grassi del cancro
Una volta attivato, AKT1 spinge le cellule ad aumentare la produzione di lipidi. Potenzia l’attività di un enzima metabolico chiave, ACLY, e aumenta i livelli di regolatori principali come SREBP1 che attivano molti geni della lipogenesi. Nelle cellule di cancro al seno coltivate in vitro, UFL1 ha fatto accumulare alle cellule più gocce lipidiche, acidi grassi liberi e colesterolo. L’eliminazione di UFL1 ha ridotto drasticamente queste riserve lipidiche, sia nelle colture sia nei tumori cresciuti nei topi. Fornire acidi grassi supplementari dall’esterno ha potuto in larga misura ripristinare la crescita delle cellule tumorali carenti di UFL1, indicando che l’effetto principale di UFL1 è assicurare lipidi sufficienti a sostenere l’espansione del tumore.
Un circuito autoamplificativo che guida la crescita tumorale
Sorprendentemente, la relazione tra UFL1 e AKT1 è bidirezionale. I ricercatori hanno scoperto che una volta attivato, AKT1 a sua volta aggiunge un gruppo fosfato a UFL1 in un sito particolare. Questa modifica potenzia ulteriormente la capacità di UFL1 di etichettare AKT1 con UFM1, creando un circuito di retroazione positiva: UFL1 attiva AKT1 e AKT1 attiva UFL1. Mutare i siti di UFM1 su AKT1 o il sito di fosforilazione su UFL1 interrompe questo circuito. Nei topi, i tumori che portavano queste versioni mutanti crescevano poco, contenevano meno lipidi e mostravano più cellule in morte. In campioni di pazienti con carcinoma mammario triplo negativo, livelli più elevati di UFL1 attivato e AKT1 attivato tendevano a presentarsi insieme, sottolineando che questo circuito opera anche nei tumori reali.
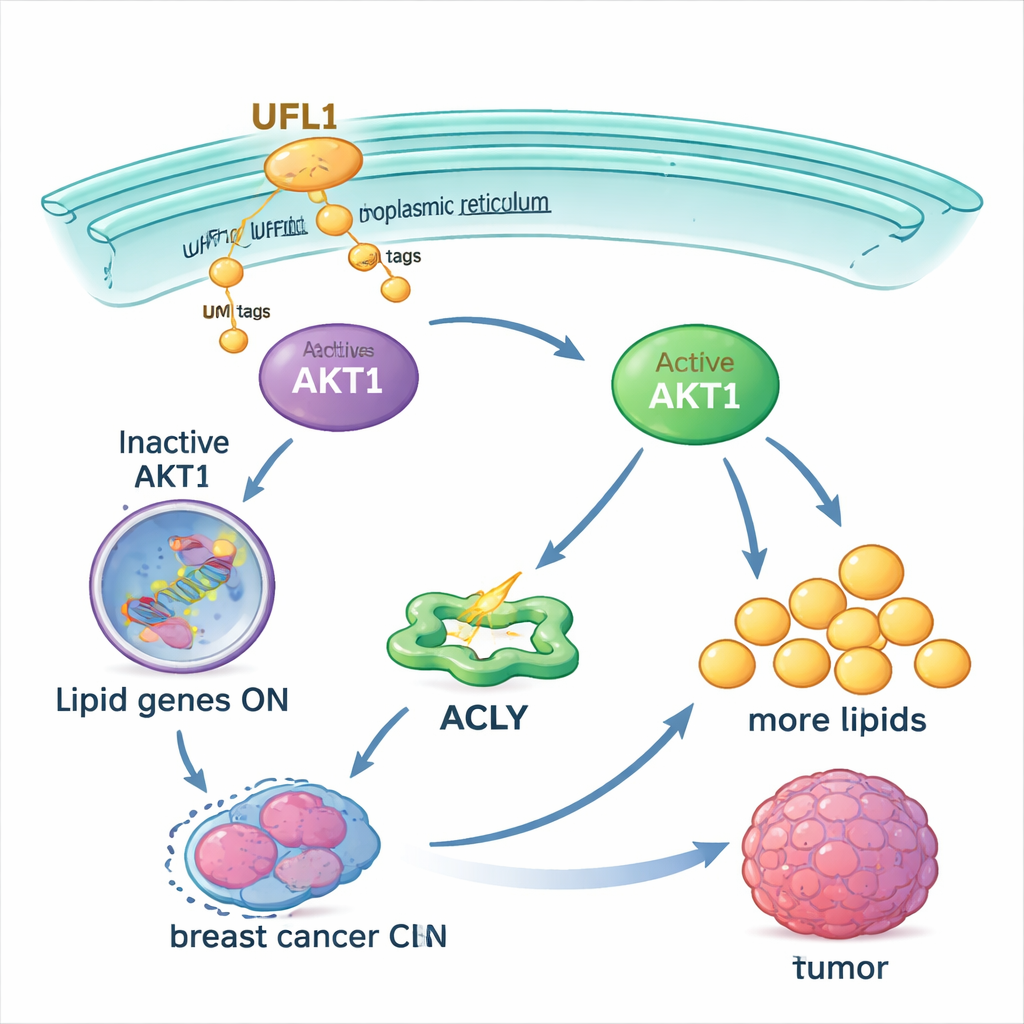
Indebolire il circuito per rendere i trattamenti più efficaci
Poiché molti trial farmacologici già mirano ad AKT, gli autori hanno testato se bloccare l’UFMilazione potesse rendere questi trattamenti più efficaci. Nelle cellule di cancro al seno, un inibitore di piccole molecole dell’UFMilazione e un inibitore di AKT hanno ciascuno ridotto l’attività di AKT1 e l’accumulo lipidico, ma usarli insieme ha funzionato molto meglio rispetto all’uno o all’altro da soli. La combinazione ha anche rallentato la crescita tumorale e ridotto il contenuto di grassi nei tumori murini senza perdita di peso evidente negli animali. Bloccare l’UFMilazione ha inoltre reso le cellule tumorali più sensibili a chemioterapie standard come cisplatino ed etoposide, le quali spesso falliscono quando AKT è altamente attivo.
Cosa significa per i pazienti
Per il lettore non specialista, lo studio mostra che alcuni tumori mammari si cablano con un circuito auto‑rinforzante che alimenta sia la loro crescita sia il loro approvvigionamento lipidico. UFL1 e AKT1 agiscono insieme come due pedali premuti contemporaneamente: uno etichetta, l’altro segnala, e insieme spingono la produzione di lipidi e l’espansione tumorale. Individuando farmaci che interferiscano con questo circuito—bloccando l’UFMilazione, AKT1 o la loro interazione—le terapie future potrebbero rallentare la crescita tumorale e rendere più efficaci i trattamenti esistenti, soprattutto nei tipi di cancro al seno più aggressivi.
Citazione: Meng, F., Du, Y., Liang, J. et al. The UFL1-AKT positive feedback loop promotes breast cancer progression by enhancing lipid synthesis. Nat Commun 17, 614 (2026). https://doi.org/10.1038/s41467-026-68492-3
Parole chiave: cancro al seno, metabolismo dei lipidi, segnalazione AKT, UFMilazione, terapia mirata