Clear Sky Science · it
Idrogel serbatoio cellulare auto-assemblante in situ per manovrare la radioimmunoterapia multistadio
Trasformare la radiazione in un’arma oncologica più intelligente
La radioterapia è uno dei trattamenti più diffusi contro il cancro, ma i tumori spesso sopravvivono nascondendosi dal sistema immunitario e sviluppandosi in condizioni a basso contenuto di ossigeno (ipossia) che attenuano l’efficacia delle radiazioni. Questo studio descrive un “idrogel intelligente” iniettabile che si forma direttamente all’interno del tumore e funziona come una piccola fabbrica di farmaci e generatore di ossigeno. Fornendo al tumore sia radiazione sia segnali immunostimolanti rilasciati in momenti calibrati, il sistema mira a trasformare un cancro difficile da curare in un bersaglio che le difese dell’organismo possono riconoscere e distruggere.
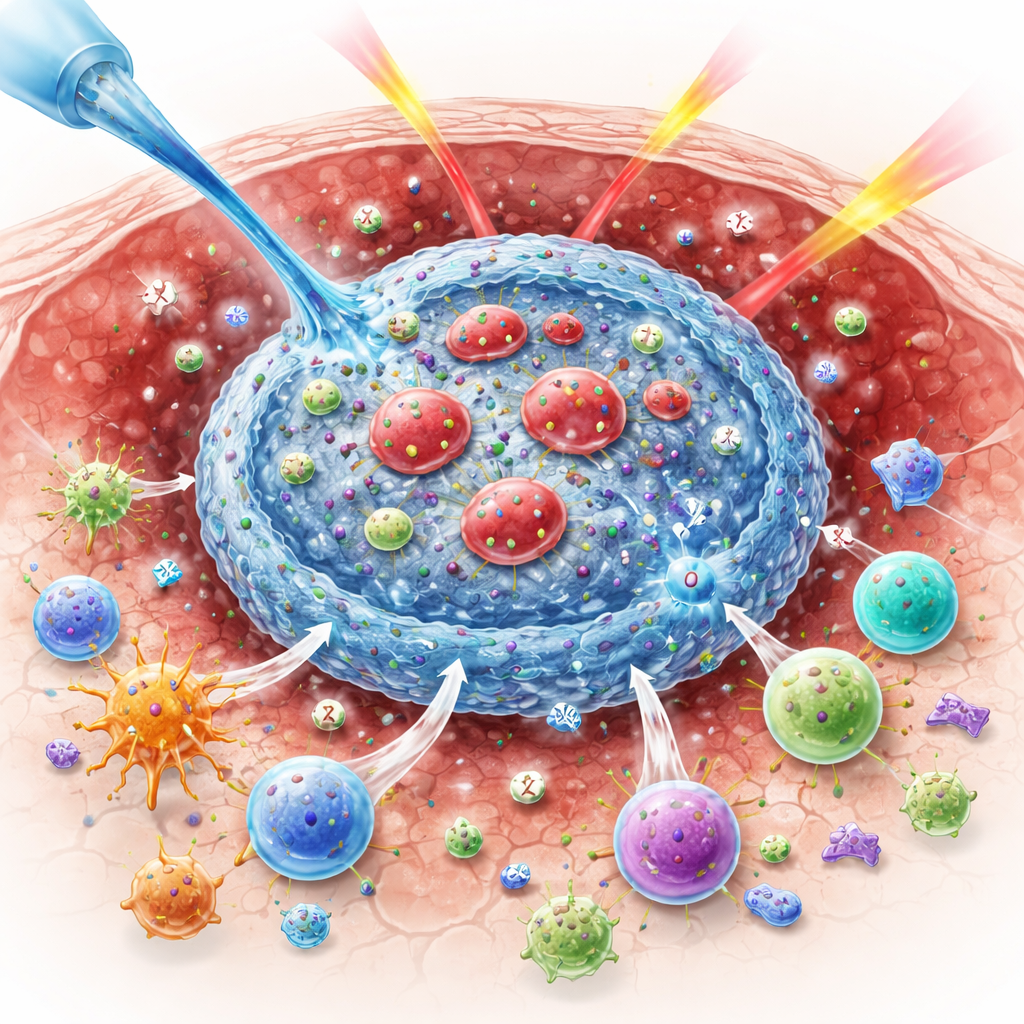
Perché l’ossigeno è cruciale per sconfiggere i tumori
La radiazione uccide le cellule tumorali in parte generando molecole di ossigeno altamente reattive che danneggiano il DNA. Quando i tumori sono privi di ossigeno, questa chimica è meno efficace e più cellule tumorali sopravvivono. Allo stesso tempo, la radiazione invia messaggi contrastanti al sistema immunitario. Può esporre proteine tumorali che segnalano il pericolo, ma può anche aumentare i “freni” delle cellule immunitarie, come la proteina di checkpoint CTLA-4, e favorire le cellule T regolatorie che sopprimono l’attacco. Questi effetti opposti spiegano in parte perché la combinazione di radiazione e farmaci immunoterapici non ha sempre funzionato nei pazienti come nei modelli murini.
Un gel vivente costruito dentro il tumore
I ricercatori hanno progettato un materiale che si auto-assembla solo nell’ambiente acido del tumore. È composto da tre parti chiave: un polimero naturale a base di zucchero chiamato alginato, una polvere inorganica detta perossido di bario e globuli rossi leggermente ingegnerizzati per trasportare due farmaci immunitari. Quando la miscela viene iniettata nel tumore, le condizioni acide provocano la decomposizione del perossido di bario, rilasciando ioni bario e perossido di idrogeno. Gli ioni bario reticolano immediatamente l’alginato formando un idrogel morbido, intrappolando i globuli rossi ingegnerizzati e impedendo che i farmaci vengano dilavati. Contemporaneamente, enzimi naturalmente presenti nei globuli rossi convertono il perossido di idrogeno in ossigeno, contribuendo ad alleviare l’ipossia tumorale e preparando il tumore a una radioterapia più efficace.
Rilascio temporizzato di due segnali immunitari
La vera potenza del sistema sta nel rilascio scaglionato di due agenti immunitari: un anticorpo che blocca CTLA-4 e una citochina chiamata interleuchina-12 (IL-12). L’anticorpo è caricato all’interno dei globuli rossi, mentre l’IL-12 è ancorata sulla loro superficie. Quando viene generato ossigeno, si formano pori nella membrana dei globuli rossi, permettendo all’anticorpo anti–CTLA-4 di fuoriuscire rapidamente. Questo primo impulso rimuove la soppressione immunitaria, incoraggia le cellule dendritiche a trasportare gli antigeni tumorali ai linfonodi vicini e aiuta ad attivare le cellule T specifiche per il tumore. L’IL-12, al contrario, fuoriesce lentamente man mano che la struttura dell’idrogel si allenta gradualmente. Questo segnale tardivo spinge le cellule T e le cellule natural killer a produrre interferone-gamma, favorisce l’ulteriore reclutamento di cellule immunitarie citotossiche nel tumore e rafforza un circuito di retroazione positiva tra sentinelle immunitarie ed effettori.
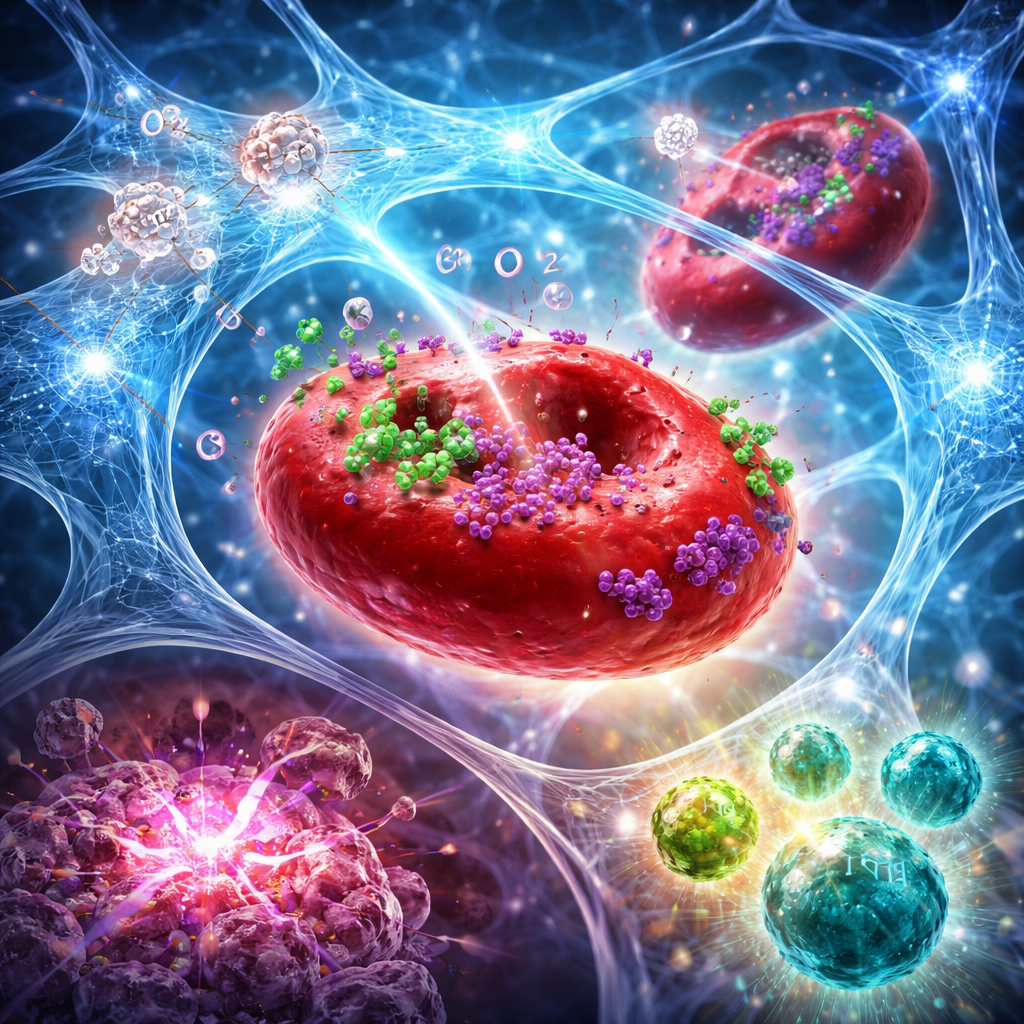
Dall’iniezione locale all’attacco immunitario sistemico
Nei modelli murini di tumori aggressivi al seno e al pancreas, l’associazione di questo idrogel con radiazione mirata ha fatto più che ridurre il tumore trattato. L’approccio combinato ha aumentato i livelli di ossigeno nei tumori per giorni, amplificato i danni al DNA indotti dalle radiazioni e innescato una forma di morte cellulare più propensa a segnalare il tumore per il riconoscimento immunitario. Citometria a flusso e colorazioni tissutali hanno mostrato un marcato cambiamento nel microambiente tumorale: più cellule T CD8 citotossiche e cellule natural killer, meno cellule T regolatorie e un rapporto più elevato tra cellule “effettori” e “soppressive”. Anche le cellule dendritiche specializzate nei linfonodi sono aumentate, indicativo di una migliore presentazione antigenica. Molti topi hanno sperimentato una regressione tumorale completa e alcuni sono stati protetti contro la ricomparsa del tumore quando cellule cancerose sono state reintrodotte settimane dopo, suggerendo la formazione di una memoria immunitaria duratura.
Sicurezza, praticità e direzioni future
Poiché il gel si forma localmente e trattiene il suo carico, solo piccole quantità di IL-12 e anti-CTLA-4 fuoriescono nel flusso sanguigno, riducendo il rischio di effetti collaterali gravi come tempeste citochiniche o danni d’organo che in passato hanno limitato l’uso di questi agenti. I componenti di base—alginato, globuli rossi e perossido di bario—sono relativamente economici e scalabili, alimentando la speranza che questa strategia possa essere adattata a diversi tipi di cancro. Sebbene permangano sfide nella produzione, nel controllo di qualità e nella somministrazione del gel a tumori profondi o ampiamente diffusi, il lavoro mette in luce un modo promettente per sincronizzare la radiazione con un’attivazione immunitaria temporizzata e precisa, trasformando un trattamento fisico del cancro in un potente innesco per un’immunità antitumorale sistemica.
Cosa potrebbe significare per i pazienti
In termini semplici, questa ricerca suggerisce che invece di somministrare radiazione e farmaci immunoterapici separatamente e sperare che cooperino, possiamo confezionarli in un materiale intelligente che si deposita nel tumore, produce il proprio ossigeno e rilascia segnali immunitari in una sequenza accuratamente coreografata. Negli animali, questo approccio non solo ha reso la radiazione più letale per le cellule tumorali, ma ha anche addestrato il sistema immunitario a riconoscere e ricordare il tumore, contribuendo a prevenirne la ricomparsa. Se risultati simili venissero ottenuti nell’uomo, tali idrogel potrebbero un giorno trasformare tumori difficili da trattare in bersagli che le difese naturali dell’organismo possono trovare e distruggere con affidabilità.
Citazione: Chen, Y., Chen, Q., Ma, Y. et al. In situ self-assembled cell reservoir hydrogel for maneuvering multistage radioimmunotherapy. Nat Commun 17, 1784 (2026). https://doi.org/10.1038/s41467-026-68490-5
Parole chiave: radioimmunoterapia, idrogel, immunoterapia del cancro, microambiente tumorale, radioterapia