Clear Sky Science · it
Multistabilità continuamente modulabile nelle reti di replicazione del DNA
Dai semplici interruttori a molti stati possibili
I sistemi biologici, dalla divisione cellulare allo sviluppo embrionale, raramente funzionano come semplici interruttori acceso/spento. Spesso mantengono invece molti stati duraturi, come un dimmer che può fermarsi in innumerevoli posizioni. Questo articolo presenta una rete chimica a base di DNA che si comporta più come quel dimmer: può mantenere stabilmente non solo pochi stati distinti, ma essenzialmente qualsiasi composizione lungo uno spettro continuo. Questa capacità potrebbe diventare una base potente per materiali intelligenti futuri, memorie molecolari e computer biochimici che elaborano informazioni analogiche, non solo digitali.
Perché gli stati multipli sono importanti
Molte decisioni cellulari — se una cellula staminale differenziarsi, se una cellula attivi l’autodistruzione o se una rete genica memorizzi un segnale passato — dipendono dalla “multistabilità”, la capacità di rimanere in più di un modello stabile di attività nelle stesse condizioni. Le versioni sintetiche tradizionali di tali sistemi sono state costruite con circuiti genici, enzimi o filamenti di DNA che si attivano o si inibiscono reciprocamente. Questi progetti tipicamente producono una manciata di esiti discreti, come i classici interruttori bistabili con due stati di lunga durata. Scalare questa idea è difficile: un sistema a N stati può richiedere dell’ordine di N×(N−1) collegamenti inibitori finemente regolati, e il sistema salta comunque solo tra un piccolo insieme di punti fissi anziché offrire una continua gamma di possibilità.
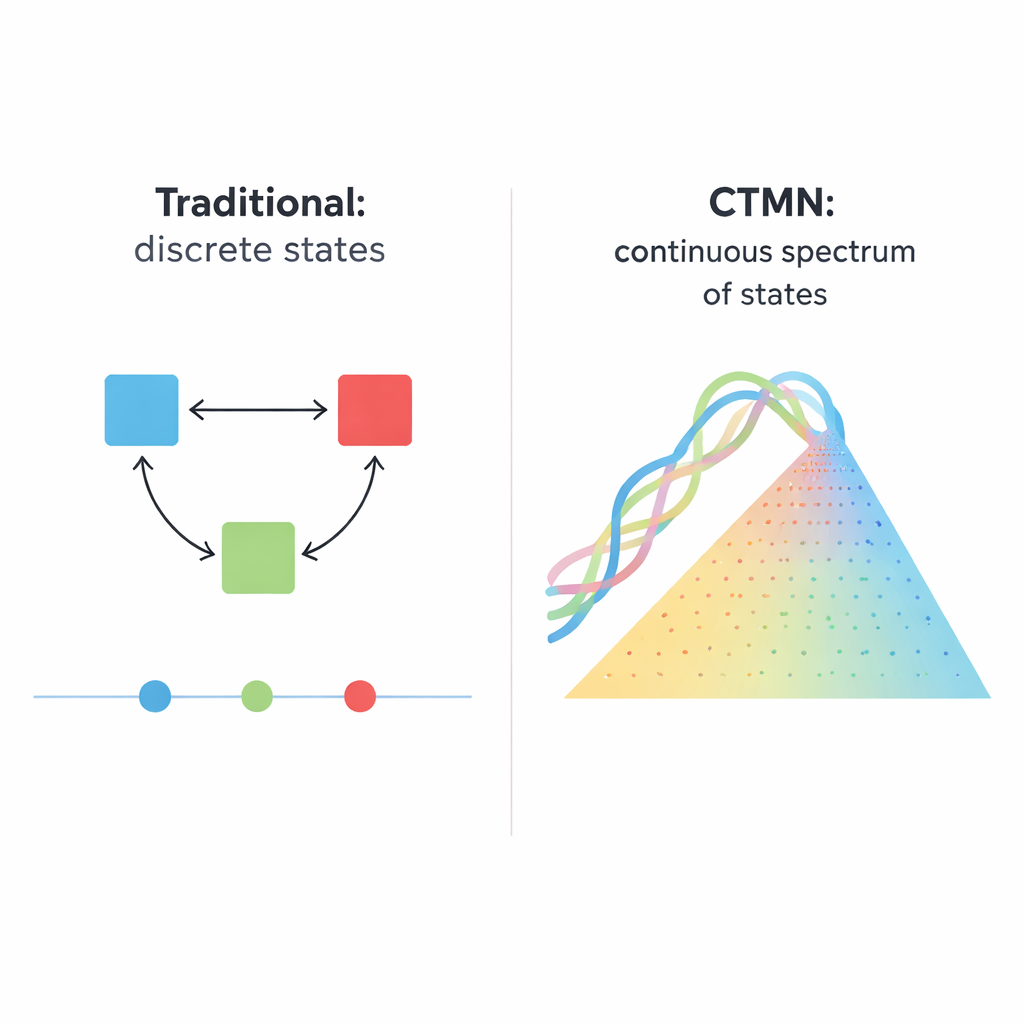
Un nuovo tipo di rete di DNA: continuamente modulabile
Gli autori introducono un principio di progettazione diverso, implementato in quelle che chiamano reti a multistabilità continuamente modulabile (CTMN). Anziché fare affidamento su molti segnali inibitori separati, usano la competizione diretta tra moduli di replicazione del DNA collegati da reazioni di scambio di filamenti reversibili. Ogni modulo è composto da duplex di DNA progettati che possono sia partecipare alla sostituzione di filamenti sia servire da stampi per la polimerasi del DNA, assistita da un enzima nicking che taglia e rigenera segmenti chiave. Il combustibile chimico — i mattoni nucleotidici chiamati dNTP — alimenta la polimerizzazione e il nicking continui, mantenendo il sistema lontano dall’equilibrio. In queste condizioni, i moduli in competizione si “congelano” effettivamente nelle proporzioni relative con cui erano iniziati, producendo non solo due o tre esiti ma un’intera linea continua (o, per più moduli, un piano) di stati di lunga durata.
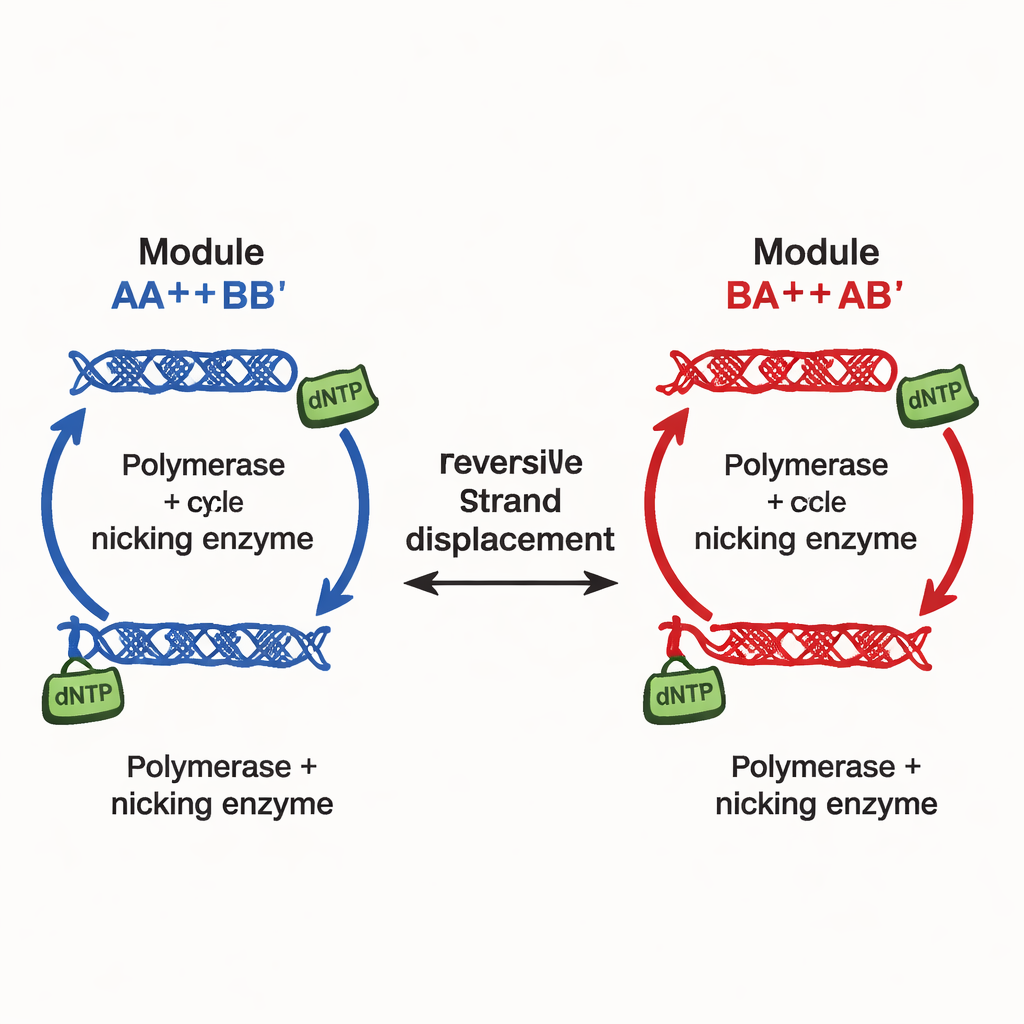
Come il macchinario molecolare fissa la memoria
Nel loro network più semplice a due moduli, CTMN‑1, il gruppo mostra sperimentalmente e tramite un dettagliato modello cinetico che il sistema può stabilizzarsi in una famiglia di miscele stabili che coprono quasi l’intera gamma da “prevalentemente modulo A” a “prevalentemente modulo B”. La polimerizzazione converte i duplex attivi in forme estese temporaneamente escluse dalla competizione di scambio di filamenti; il nicking poi li ripristina, chiudendo un circuito autoregolatorio. Quando entrambi i moduli condividono questo circuito, sopprimono l’interconversione reciproca così fortemente che il sistema rimane bloccato vicino alla composizione iniziale per molte ore, purché sia disponibile il combustibile. L’analisi di stabilità lineare delle equazioni sottostanti rivela un intero manifold — efficacemente un continuum — di stati stazionari, in contrasto con l’unico punto fisso osservato quando gli enzimi o il combustibile vengono rimossi.
Risposte programmabili e memoria molecolare
Poiché lo stato della rete è immagazzinato nelle composizioni del DNA, può essere guidato e letto in modi programmabili. Gli autori progettano brevi “inneschi” di RNA che si legano temporaneamente a specifici filamenti di DNA, sbilanciando la competizione e spostando la rete verso una nuova composizione. Anche dopo che l’RNA viene degradato da un enzima, il nuovo stato persiste, funzionando come una forma di memoria molecolare. Stimoli ripetuti o più intensi spingono il sistema in modo graduale lungo il continuum di stati invece di farlo commutare tra semplici posizioni acceso/spento. Inoltre, i prodotti della replicazione del DNA possono essere personalizzati per agire come segnali per processi a valle: nelle dimostrazioni, diversi stati di CTMN‑1 attivano selettivamente uno dei due catalizzatori a base di DNA o indirizzano la trascrizione di RNA verso uno dei due filamenti messaggeri, senza disturbare la multistabilità sottostante.
Scalare verso “dimmer” molecolari complessi
Per mostrare che questa strategia è scalabile, i ricercatori costruiscono una rete a tre moduli, CTMN‑2, aggiungendo ulteriori duplex di DNA progettati che condividono un dominio di scambio comune ma codificano diversi stampi di replicazione. Ora gli stati stazionari possibili riempiono una regione bidimensionale, come punti attraverso un diagramma di fase triangolare, invece di disporre lungo una semplice linea. Anche in questo caso, gli esperimenti confermano che molte composizioni distinte sono stabili finché sono presenti combustibile ed enzimi, e che tutte collassano in un unico punto di equilibrio quando la fornitura di energia viene rimossa. Poiché aggiungere nuovi moduli richiede solo nuovi costrutti di DNA che si inseriscono nello stesso framework di sostituzione, il cablaggio complessivo non esplode in complessità come nei progetti tradizionali.
Cosa significa per le tecnologie molecolari future
Per un non specialista, il messaggio fondamentale è che gli autori hanno trasformato una rete di replicazione del DNA in un dispositivo di memoria analogico altamente flessibile. Piuttosto che scegliere tra alcune opzioni prestabilite, il loro sistema può mantenere in modo affidabile una delle dozzine di stati sperimentalmente distinguibili, ciascuno definito da quanto di ciascun modulo di DNA è presente, e può convertire impulsi chimici transitori in spostamenti duraturi lungo questo continuum. Poiché i filamenti di DNA di uscita sono programmabili e disaccoppiati dal meccanismo stabilizzante, lo stesso framework potrebbe, in linea di principio, regolare una vasta gamma di reazioni biochimiche a valle o le proprietà dei materiali con controllo fine e graduato. Questo lavoro indica quindi la strada verso dispositivi molecolari che calcolano, memorizzano e si adattano più come sistemi analogici neurali o meccanici che non come semplici interruttori digitali.
Citazione: Zhong, R., Fu, Y., Jiang, S. et al. Continuously tunable multistability in DNA replication networks. Nat Commun 17, 1782 (2026). https://doi.org/10.1038/s41467-026-68488-z
Parole chiave: multistabilità del DNA, memoria molecolare, reti biochimiche sintetiche, sostituzione di filamenti di DNA, calcolo molecolare analogico