Clear Sky Science · it
PTRAMP, CSS e Ripr formano un complesso conservato necessario per l’invasione dei merozoiti delle specie di Plasmodium negli eritrociti
Perché è importante per la lotta alla malaria
I parassiti della malaria devono penetrare nei nostri globuli rossi per causare la malattia. Questo studio svela un piccolo insieme di proteine che formano un “ponte d’imbarco” condiviso utilizzato da diverse specie principali di malaria, incluse quelle che infettano gli esseri umani. Rivelando come questo ponte viene costruito e come talvolta gli anticorpi possono bloccarlo, il lavoro indica nuove strategie per progettare vaccini in grado di proteggere da più tipi di malaria contemporaneamente. 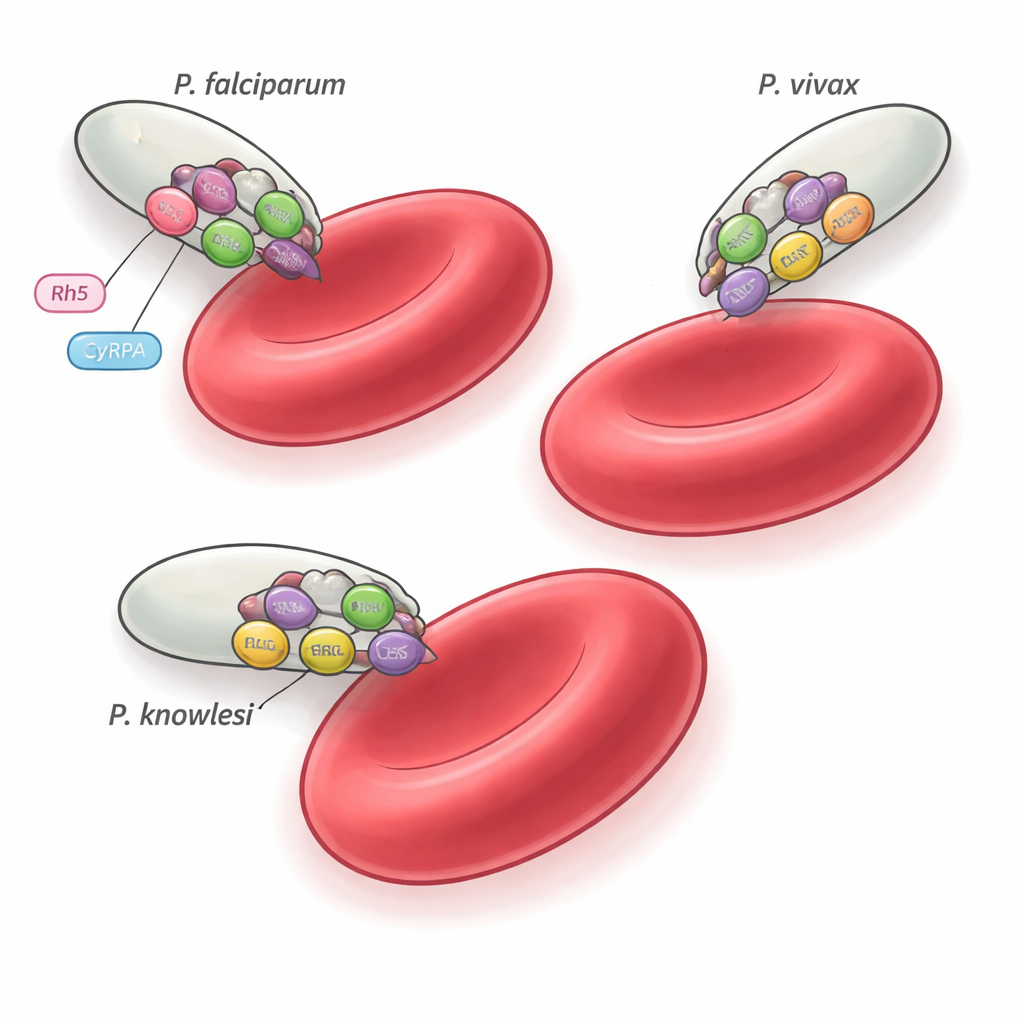
Un kit comune in molte specie di malaria
Esistono più di 200 specie di Plasmodium, ma solo poche, come P. falciparum, P. vivax e P. knowlesi, infettano gli esseri umani. Queste specie occupano rami diversi dell’albero filogenetico del parassita e prediligono tipi diversi di globuli rossi, eppure tutte devono invadere gli eritrociti con precisione estrema. Studi precedenti in P. falciparum hanno identificato un’assemblaggio in cinque parti, il complesso PCRCR, essenziale per l’invasione che si lega a un recettore dei globuli rossi umani chiamato basigin. Un componente di quel complesso, una proteina chiamata Rh5, è unico di P. falciparum e dei suoi parenti stretti, sollevando un quesito: cosa usano le altre specie di malaria al suo posto? Lo studio attuale si concentra su tre proteine companion—PTRAMP, CSS e Ripr—che sono conservate attraverso il genere e verifica se formano una macchina di invasione universale.
Costruire un ponte d’invasione in tre parti
Utilizzando ricerche di sequenze su molti genomi di parassiti, gli autori mostrano che PTRAMP, CSS e Ripr sono presenti in tutte le principali linee di Plasmodium, a differenza di Rh5, che è limitata a un sottogruppo. La previsione strutturale con AlphaFold, combinata con misurazioni biochimiche dettagliate, rivela che PTRAMP e CSS si uniscono per formare una coppia stabile, tenuta insieme da un legame disolfuro specifico tra due cisteine conservate. Questa piattaforma a due proteine poi si fissa all’estremità C-terminale di Ripr, creando un complesso in tre parti PTRAMP–CSS–Ripr (PCR). Esperimenti con proteine di P. falciparum, P. vivax e P. knowlesi mostrano che questo complesso si forma in tutte e tre le specie con alta affinità, e che è sufficiente una piccola regione dell’estremità C-terminale di Ripr per un legame stretto. 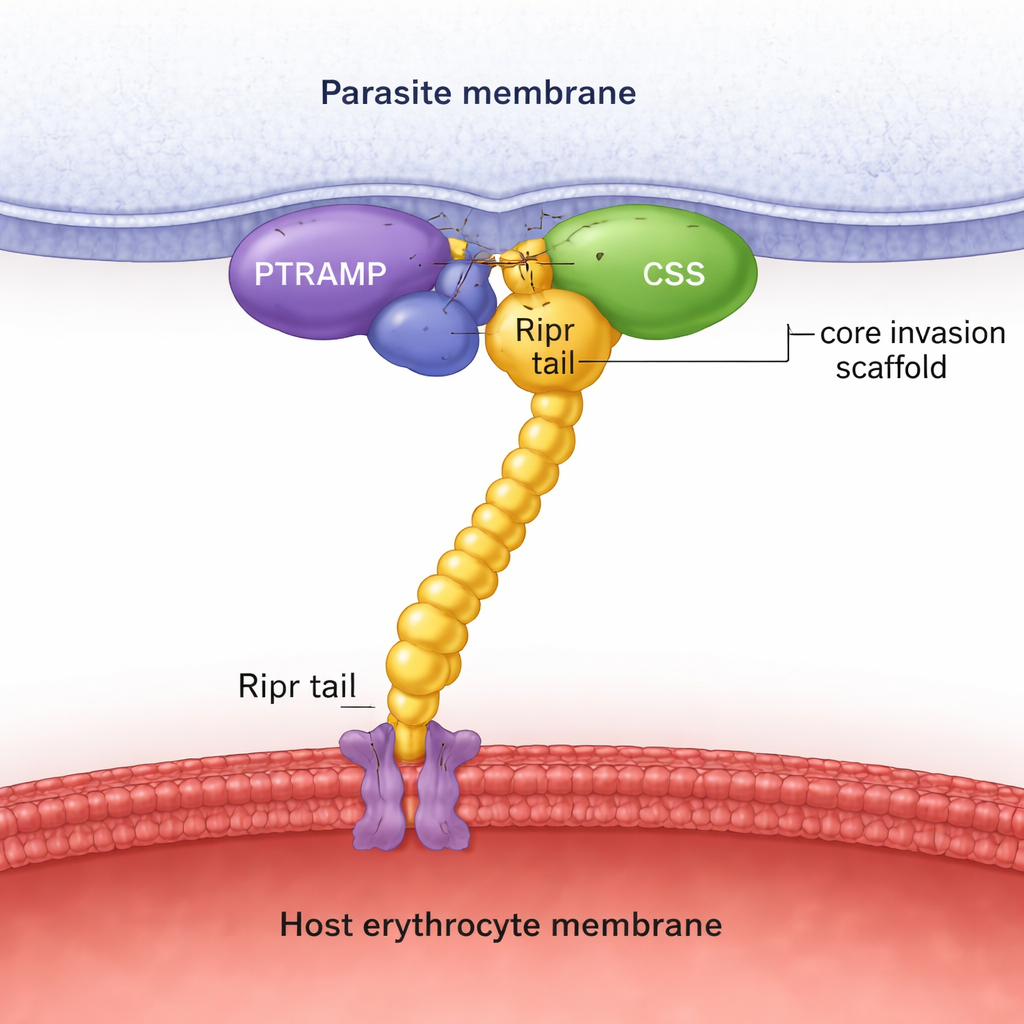
Osservare la struttura a dettaglio atomico
Per andare oltre le predizioni, il team ha risolto strutture cristalline e raccolto immagini mediante crio‑microscopia elettronica. La struttura cristallina della coppia PTRAMP–CSS di P. vivax mostra esattamente come un breve tratto di PTRAMP si snoda attraverso CSS e forma il legame disolfuro chiave. Un’altra struttura cattura un anticorpo potente legato a due domini simili a fattori di crescita di Ripr, mappando un epitopo inibitorio sulla coda di Ripr. L’analisi crio‑EM del complesso PCR di P. knowlesi conferma la forma complessiva predetta da AlphaFold: PTRAMP e CSS si trovano vicino alla membrana del parassita e stringono Ripr, il cui corpo allungato si estende verso la cellula ospite. Questi scatti strutturali insieme sostengono l’idea che il trio PCR formi un’impalcatura rigida che fisicamente copre il divario tra parassita ed eritrocita durante l’invasione.
Anticorpi che riconoscono più di una specie
Poiché queste proteine sono conservate, gli autori si sono chiesti se le infezioni umane generino naturalmente anticorpi che cross‑reagiscono tra specie. Il plasma di pazienti infettati con P. falciparum, P. vivax o P. knowlesi ha mostrato forti risposte anticorpali verso CSS e Ripr di più specie, suggerendo che le persone sviluppano anticorpi contro regioni condivise del complesso PCR. Il team ha quindi prodotto anticorpi monoclonali e nanocorpi che prendono di mira PTRAMP, CSS e Ripr di P. vivax, e ha testato se questi riuscissero a bloccare la crescita del parassita in coltura. Alcuni anticorpi, in particolare uno chiamato 5B3 che si lega alla coda di Ripr, sono stati in grado di inibire l’invasione da parte di P. knowlesi e, a concentrazioni più elevate, di P. falciparum. Sorprendentemente, gli stessi anticorpi non hanno bloccato P. vivax o il parassita di scimmia strettamente correlato P. cynomolgi, anche se potevano legare le proteine di quelle specie.
Un’impalcatura condivisa con componenti specifici per specie
I test funzionali mostrano che il complesso PCR di per sé non si attacca agli eritrociti; invece, probabilmente serve come impalcatura strutturale conservata su cui ogni specie fissa i propri partner leganti il recettore. In P. falciparum, per esempio, il trio PCR collabora con CyRPA e Rh5 per ingaggiare la basigin sugli eritrociti umani. In P. vivax e P. knowlesi, le proteine equivalenti che legano il recettore e gli obiettivi ospite restano sconosciuti, ma lo stesso nucleo PTRAMP–CSS–Ripr sembra organizzare il macchinario d’invasione. Il fatto che alcuni anticorpi possano cross‑reagire ma inibire solo certe specie sottolinea come differenze sottili nell’assemblaggio del complesso e nel timing possano modificare la vulnerabilità all’attacco immunitario.
Cosa significa per i futuri vaccini contro la malaria
Per un non‑specialista, il messaggio principale è che i parassiti della malaria di specie molto diverse condividono una “spina” comune che usano per entrare nei globuli rossi—costituita dalle proteine PTRAMP, CSS e Ripr—anche se collegano quella spina a recettori diversi sulla superficie cellulare. Questa spina conservata è ora mappata strutturalmente e, in alcuni casi, può essere colpita da anticorpi che funzionano attraverso specie diverse. Pur essendo necessario altro lavoro per identificare l’insieme completo dei partner proteici e per migliorare gli anticorpi inibitori, la scoperta di un’impalcatura d’invasione universale apre la strada a progetti di vaccini che potrebbero proteggere contro più tipi di malaria piuttosto che contro uno solo.
Citazione: Seager, B.A., Lim, P.S., Xiao, X. et al. PTRAMP, CSS and Ripr form a conserved complex required for merozoite invasion of Plasmodium species into erythrocytes. Nat Commun 17, 1780 (2026). https://doi.org/10.1038/s41467-026-68486-1
Parole chiave: invasione della malaria, proteine di Plasmodium, ingresso del merozoite, vaccino interspecie, infezione degli eritrociti