Clear Sky Science · it
Criomicroscopia elettronica in tomografia rivela replicazione, gemmazione e maturazione accoppiate nei flavivirus
Come i virus che infettano il cervello dirottano le membrane cellulari
I flavivirus, un vasto gruppo di virus che include gli agenti responsabili della dengue e dell’encefalite trasmessa da zecche, possono invadere il cervello e provocare malattie gravi. Tuttavia, il modo esatto in cui questi minuscoli patogeni si replicano e assemblano nuove particelle virali all’interno delle nostre cellule è rimasto in gran parte nascosto. Questo studio utilizza immagini elettroniche 3D all’avanguardia a temperature criogeniche per osservare i flavivirus trasmessi da zecche al lavoro all’interno di cellule umane e tessuto cerebrale murino, rivelando un accoppiamento inaspettatamente stretto tra copia del genoma, assemblaggio del virus e maturazione del virus.
Fabbriche virali nascoste nelle membrane cellulari
I flavivirus non si limitano a fluttuare nella cellula mentre si replicano. Modificano invece un sistema di membrane cellulari chiamato reticolo endoplasmatico (RE) per formare tasche specializzate note come organelli di replicazione. Queste assomigliano a piccoli rigonfiamenti interni sulla superficie del RE e fungono da camere protette in cui vengono copiati i genomi di RNA virali. Utilizzando la criomicroscopia elettronica in tomografia, una tecnica che produce istantanee 3D di cellule congelate istantaneamente in uno stato vicino al loro ambiente nativo, i ricercatori hanno visualizzato questi rigonfiamenti in cellule polmonari umane infette con un flavivirus trasmesso da zecche correlato al virus dell’encefalite da zecche. Hanno osservato che il RE attorno alle regioni infette si gonfia e diventa pieno di ammassi di questi organelli di replicazione, alcuni dei quali sono vuoti mentre altri sono riempiti da RNA denso e filamentoso.
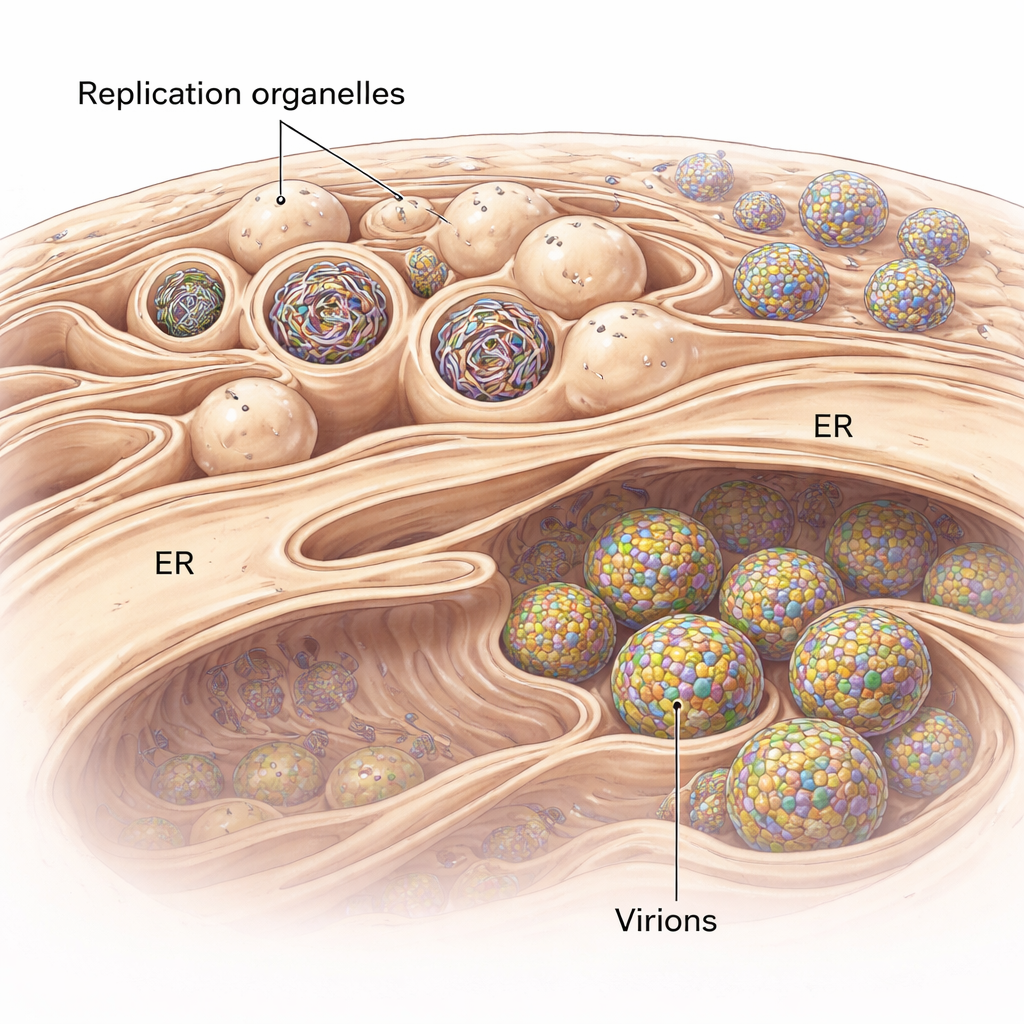
Costruire la bolla virale perfetta
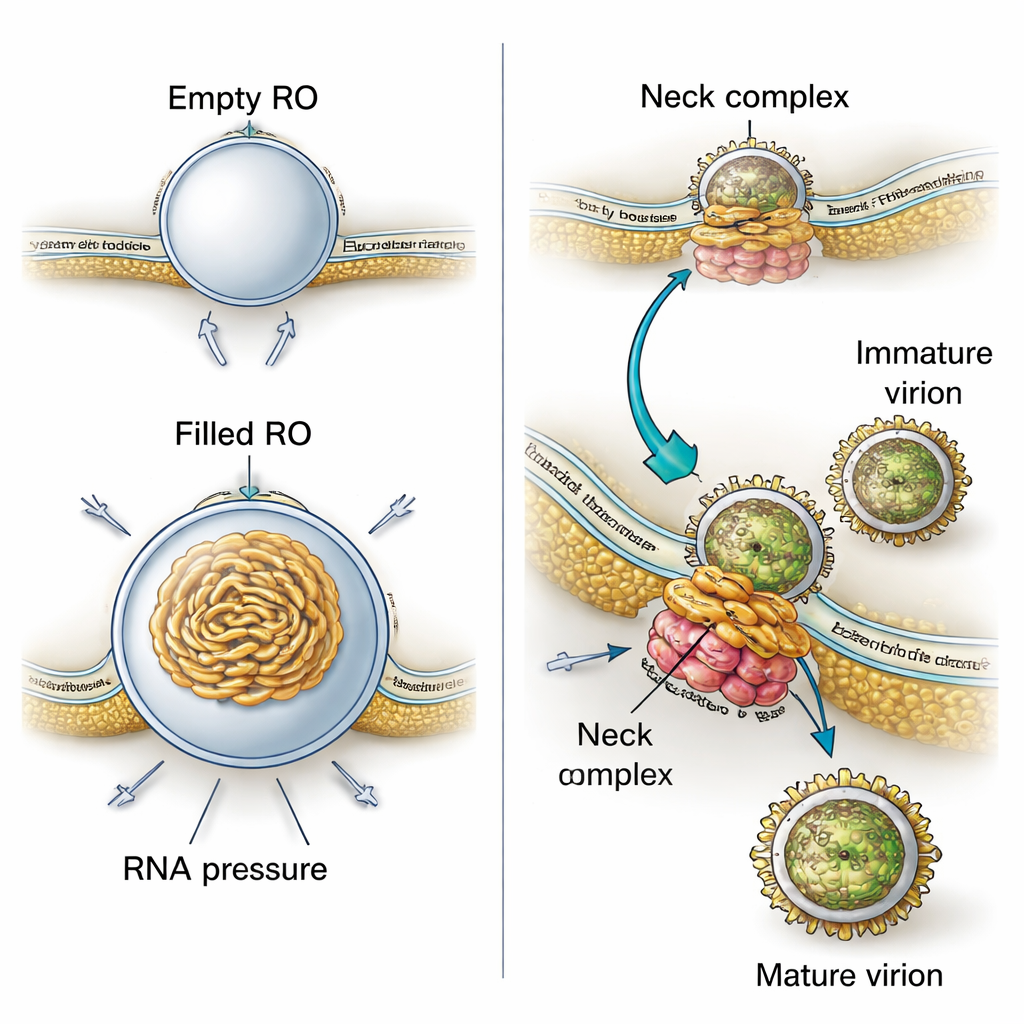
Perché queste tasche di membrana hanno una forma così precisa a gemma? Combinando le loro immagini 3D con modellizzazione fisica, gli autori mostrano che due forze lavorano insieme. Primo, la membrana degli organelli di replicazione è costantemente più spessa del normale RE, suggerendo che proteine virali o lipidi alterati irrigidiscono e curvano la membrana formando una gemma stabile già prima che qualsiasi RNA entri. Secondo, quando l’RNA virale è presente, si avvolge all’interno della tasca e spinge verso l’esterno, aumentando le dimensioni della gemma. I calcoli basati sulle misure indicano che ogni organello pieno contiene probabilmente una pressione corrispondente approssimativamente a una copia del genoma virale in forma a doppio filamento. Ciò significa che il virus sfrutta sia una membrana preformata sia la spinta fisica del proprio materiale genetico per costruire e stabilizzare le sue miniature fabbriche.
Linea di assemblaggio: dalla copia del genoma a nuovi virus
Lo studio rivela anche quanto strettamente la produzione di virus sia collegata a questi siti di replicazione. Nelle loro viste 3D, i ricercatori hanno frequentemente osservato nuove particelle virali che si formavano proprio accanto agli organelli di replicazione, gemmando verso spazi vicini simili al RE. Le particelle immature avevano una superficie spigolosa, mentre quelle più mature apparivano lisce. Misurando le distanze nei tomogrammi si è visto che le particelle immature si trovano più vicine agli organelli di replicazione rispetto a quelle mature, il che implica che, mentre le particelle si spostano solo per una breve distanza attraverso compartimenti membranosi intrecciati, subiscono i cambiamenti strutturali necessari per diventare infettive. Un grande complesso proteico al collo stretto dove ogni gemma di replicazione si connette al citoplasma sembra ancorare l’organello di replicazione a una membrana vicina dove avviene la gemmazione. Questo complesso probabilmente agisce come una cerniera molecolare che coordina la produzione di RNA con l’incapsidamento di quell’RNA in nuove particelle virali.
Rifinire la maturazione con un singolo amminoacido
Per indagare come viene controllata la maturazione del virus, il gruppo ha confrontato due versioni di un virus chimerico che differiscono per un solo amminoacido in un sito riconosciuto da un enzima ospite chiamato furina. Questo enzima taglia una proteina superficiale virale, facilitando la trasformazione delle particelle immature spigolose in particelle mature lisce. In saggi di scissione in provetta e in cellule infette, la variante con un arginina in questa posizione veniva tagliata più rapidamente rispetto alla variante con una glutammina. Quando osservato nelle cellule mediante criomicroscopia elettronica in tomografia, il virus a scissione più rapida produceva una proporzione maggiore di particelle mature vicino agli organelli di replicazione. Nonostante queste differenze microscopiche, entrambe le varianti hanno mostrato pattern simili di crescita e patologia in un modello murino, suggerendo che il virus può tollerare una gamma di efficienze di maturazione pur rimanendo infettivo.
Osservare l’infezione direttamente nel cervello
La maggior parte degli studi strutturali sui virus si basa su linee cellulari, ma questo lavoro si estende anche al tessuto vivente. I ricercatori hanno isolato una struttura cerebrale chiamata plesso coroideo da topi infetti e l’hanno preparata per la criomicroscopia elettronica in tomografia usando congelamento ad alta pressione e fresatura con fascio ionico focalizzato. Anche in questo ambiente complesso hanno osservato gli stessi segni distintivi: ammassi di organelli di replicazione, membrane ispessite e vescicole vicine piene di particelle virali mature. Ciò dimostra che il rimodellamento delle membrane e la sequenza strettamente accoppiata replicazione–assemblaggio–maturazione osservata nelle cellule in coltura operano anche nel cervello, dove questi virus causano malattia.
Perché questi processi nascosti sono importanti
Per i non specialisti, il messaggio centrale è che questi virus che infettano il cervello gestiscono una linea di assemblaggio altamente organizzata all’interno delle nostre cellule. Modellano le membrane cellulari in piccole bolle pressurizzate dove i genomi vengono copiati, collegano direttamente quelle bolle ai siti in cui si formano le nuove particelle e avviano persino i passaggi finali di maturazione a portata di mano del sito di replicazione originale. L’identificazione delle membrane di replicazione ispessite, del complesso proteico che attraversa il collo e dei compartimenti di maturazione strettamente intrecciati non solo spiega come i flavivirus si replicano in modo così efficiente, ma indica anche nuovi bersagli per farmaci antivirali progettati per disturbare le fabbriche nascoste del virus e le sue vie di assemblaggio.
Citazione: Dahmane, S., Schexnaydre, E., Zhang, J. et al. Cryo-electron tomography reveals coupled flavivirus replication, budding and maturation. Nat Commun 17, 828 (2026). https://doi.org/10.1038/s41467-026-68483-4
Parole chiave: flavivirus, criomicroscopia elettronica in tomografia, organelle di replicazione, maturazione del virus, encefalite trasmessa da zecche