Clear Sky Science · it
Approfondimenti spettroeletrochimici su catalizzatori rame-cobalto per la co-elettroreductione di CO2 e nitrito a urea
Trasformare gas di scarto in fertilizzante
L’urea come fertilizzante sostiene l’agricoltura moderna, ma la sua produzione convenzionale richiede molta energia e genera elevate emissioni di carbonio. Questo studio esplora un approccio molto diverso: usare elettricità per trasformare direttamente anidride carbonica (CO2) e rifiuti contenenti azoto (come il nitrito proveniente da scarichi o acque reflue) in urea. Per il lettore non specialista, l’attrattiva è evidente: una via per ottenere un fertilizzante essenziale che potrebbe ridurre le emissioni, impiegare flussi di rifiuti come materia prima e, un giorno, essere alimentata da elettricità rinnovabile.
Perché ripensare la produzione di urea?
Oggi l’urea si ottiene principalmente producendo prima ammoniaca dall’azoto e da idrogeno di origine fossile (processo Haber–Bosch), e poi reagendo l’ammoniaca con CO2 ad alte temperature e pressioni. Questa catena di reazioni è centralizzata, richiede grandi investimenti e genera quasi una tonnellata di CO2 per tonnellata di urea prodotta. Con l’aumento della domanda globale di fertilizzanti, crescono anche i costi ambientali. Un’alternativa è bypassare completamente i combustibili fossili facendo svolgere i passaggi chimici chiave dall’elettricità, idealmente rinnovabile, e sfruttando CO2 e ossidi di azoto (NOx) che oggi sono trattati come rifiuti.
Un nuovo ruolo per rame e cobalto
Gli autori progettano catalizzatori in film sottile depositati co-sputterando rame (Cu) e cobalto (Co) su carta carboniosa, dosando con cura il rapporto Cu:Co. Si concentrano sulla riduzione elettrochimica simultanea di CO2 e nitrito (NO2⁻) in acqua a pH neutro, un ambiente che può favorire la formazione sottile di legami carbonio–azoto (C–N) necessari per l’urea. La composizione che spicca è una miscela 1:1 di Cu e Co, che raggiunge una velocità di produzione di urea di circa 61 millimoli all’ora per grammo di catalizzatore a un potenziale applicato moderato. Microscopia e misure ai raggi X mostrano che i metalli sono intimamente mescolati su scala atomica e rimangono in gran parte metallici durante l’operazione, offrendo una piattaforma robusta in cui sia CO2 sia nitrito possono reagire in modo efficiente. 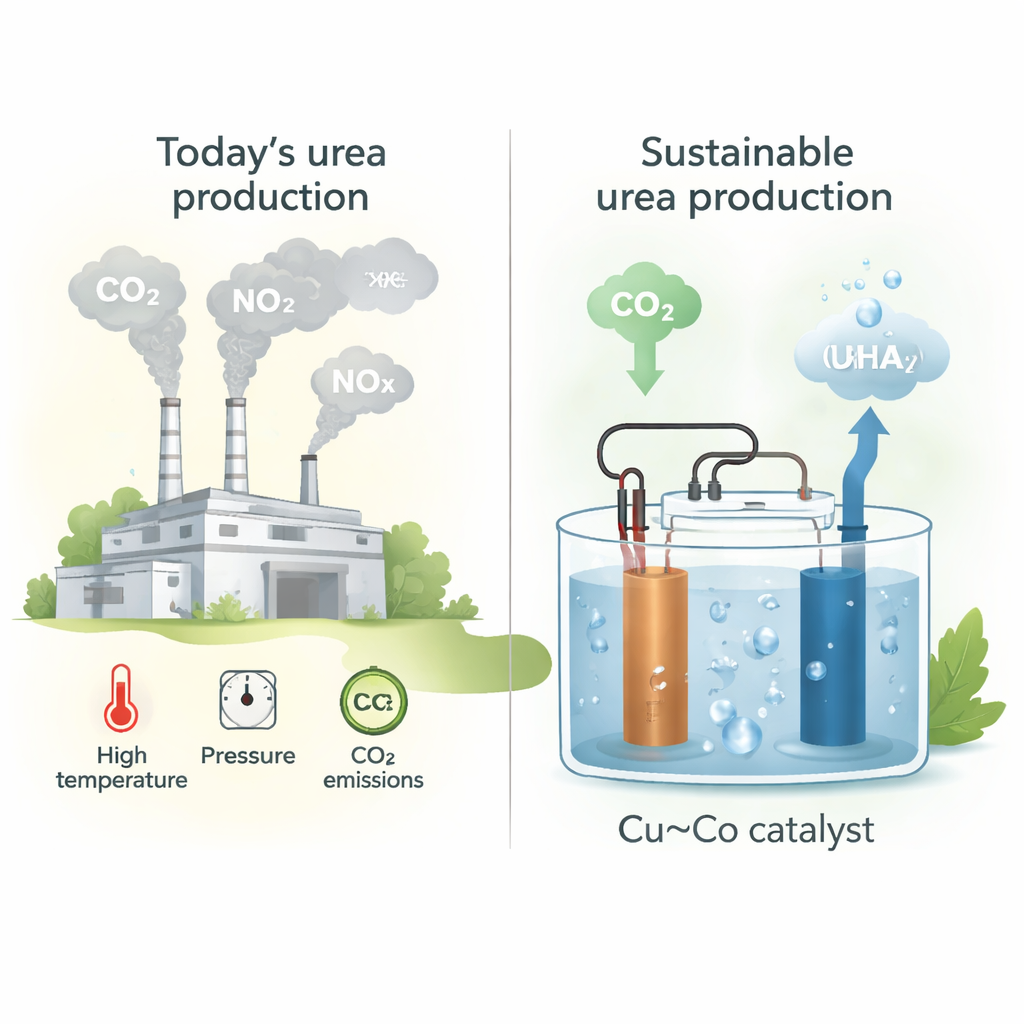
Come il catalizzatore divide e condivide il lavoro
Produrre urea in questo modo è impegnativo perché reazioni più semplici — come la produzione di idrogeno gassoso o la riduzione separata di CO2 o nitrito — competono fortemente. La chiave, osservano i ricercatori, è una divisione del lavoro tra siti di rame e di cobalto che agiscono in tandem. I test elettrochimici mostrano che il rame da solo converte principalmente la CO2 in combustibili e composti a base di carbonio, mentre il cobalto da solo trasforma soprattutto il nitrito in ammoniaca, senza produrre urea in entrambi i casi. Solo quando atomi di Cu e Co sono mescolati strettamente si osserva una produzione significativa di urea. “Istantanee” spettroscopiche acquisite durante la reazione rilevano frammenti legati alla superficie: specie di carbonio derivate da CO2 (*CO e *COOH) che preferiscono il rame, e specie azotate derivate dal nitrito (*NH2 e gruppi correlati) che preferiscono il cobalto. Ai confini tra Cu e Co, questi frammenti possono incontrarsi e accoppiarsi per formare lo scheletro C–N dell’urea.
Trovare le condizioni giuste per costruire legami
Lo studio mostra che la composizione da sola non basta; anche la soluzione circostante e la membrana devono essere ottimizzate. L’urea compare solo in un elettrolita bicarbonato neutro, che mantiene sufficiente CO2 disciolta e fornisce la giusta quantità di protoni (ioni idrogeno) per guidare i passaggi di “trasferimento accoppiato protone-elettrone” senza saturare la superficie con evoluzione di idrogeno. In condizioni fortemente acide o fortemente alcaline, l’urea o non si forma o si decompone rapidamente in prodotti più semplici. Esperimenti con diverse sorgenti di azoto rivelano che il nitrito è particolarmente efficace per la formazione di urea, superando nitrato e idrossilammina. Test prolungati per molte ore indicano che i film Cu–Co sono relativamente stabili, con perdite metalliche modeste e una produzione di urea sostenuta.
Dando un’occhiata sotto il cofano con la teoria
Per capire perché questo catalizzatore tandem funziona così bene, il team ricorre a simulazioni al computer basate sulla teoria del funzionale della densità. Questi calcoli supportano l’idea che il rame favorisca il legame delle specie derivate da CO2, mentre il cobalto attivi meglio il nitrito e stabilizzi frammenti contenenti azoto. Le simulazioni identificano un passaggio particolare come il collo di bottiglia energetico: l’accoppiamento di un frammento *NH2 (dal nitrito) con un frammento *COOH (dalla CO2) per formare un intermedio talvolta indicato come *NH2CO. Una volta che questo pezzo è formato, i passaggi rimanenti verso l’urea sono relativamente facili. L’interfaccia Cu–Co abbassa il costo energetico di questo accoppiamento cruciale rispetto al rame puro o al cobalto puro, spiegando l’incremento sperimentale nella resa di urea per il sistema bimetallico. 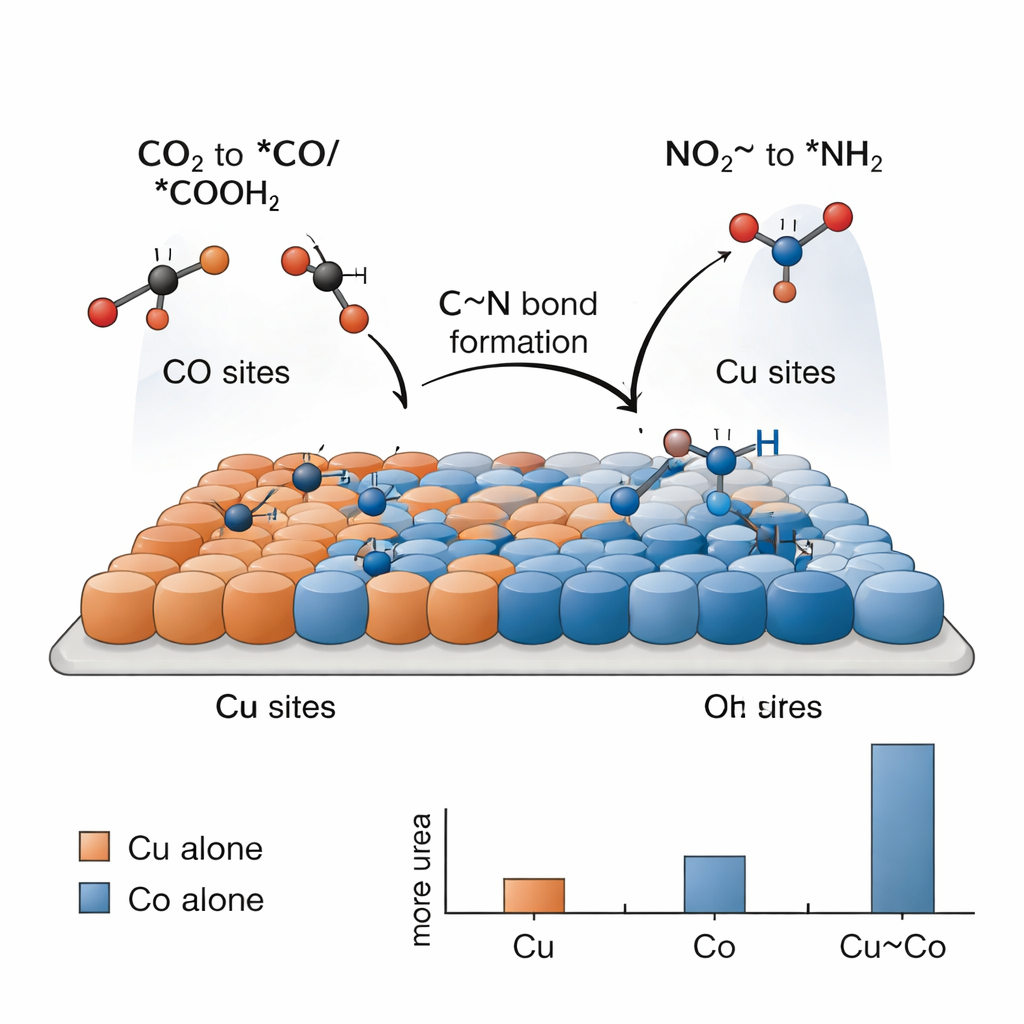
Dall’intuizione di laboratorio a fertilizzanti più verdi
In termini pratici, questo lavoro non sostituisce ancora le gigantesche ureepiante odierne, ma chiarisce come potrebbe essere progettata una futura via elettrochimica. Dimostrando che rame e cobalto possono operare in tandem — uno che fornisce specie di carbonio attivate, l’altro specie di azoto attivate, entrambi sotto condizioni di protoni attentamente controllate — lo studio traccia un percorso realistico verso una produzione di urea più pulita e potenzialmente decentralizzata che utilizzi CO2 e rifiuti azotati come risorse anziché come inquinanti.
Citazione: Ramadhany, P., Trần-Phú, T., Yuwono, J.A. et al. Spectroelectrochemical insight into copper cobalt catalysts for CO2 and nitrite co-electroreduction to urea. Nat Commun 17, 1776 (2026). https://doi.org/10.1038/s41467-026-68481-6
Parole chiave: sintesi elettrochimica dell’urea, catalizzatore rame cobalto, utilizzo della CO2, riduzione del nitrito, accoppiamento C–N