Clear Sky Science · it
Base strutturale per l’inibizione selettiva del trasportatore umano di GABA GAT3
Perché i segnali calmanti del cervello sono importanti
I nostri cervelli dipendono da un delicato equilibrio tra segnali che eccitano e segnali che calmano. Un messaggero chiave del lato calmante è il GABA, una molecola che aiuta a prevenire attività incontrollata collegata a condizioni come epilessia, danno da ictus e malattia di Alzheimer. Questo studio si concentra su una proteina chiamata GAT3, che elimina il GABA dall’intorno delle cellule nervose. Rivelando, a livello atomico, come una nuova molecola si aggancia a GAT3 e lo spegne, i ricercatori forniscono una mappa strutturale per progettare farmaci di nuova generazione in grado di potenziare in modo delicato il sistema frenante naturale del cervello.
Il freno naturale del cervello
Il GABA è il principale neurotrasmettitore inibitorio, o calmante, del sistema nervoso centrale. Dopo che il GABA viene rilasciato dalle terminazioni nervose, deve essere rapidamente rimosso affinché i circuiti cerebrali possano resettarsi. Questa pulizia è svolta da proteine trasportatrici che pompagliano il GABA di nuovo nelle cellule. Due di questi trasportatori predominano nel cervello: GAT1, presente principalmente nei neuroni, e GAT3, presente nelle cellule di supporto chiamate astrociti. Mentre un farmaco che blocca GAT1 (tiagabina) è stato usato per decenni nel trattamento dell’epilessia, medicinali comparabili che prendono di mira GAT3 sono rimasti indietro. Eppure GAT3 è particolarmente interessante perché controlla i livelli di GABA al di fuori delle sinapsi e modella un’inibizione di fondo di lunga durata che può rifinire l’attività cerebrale. 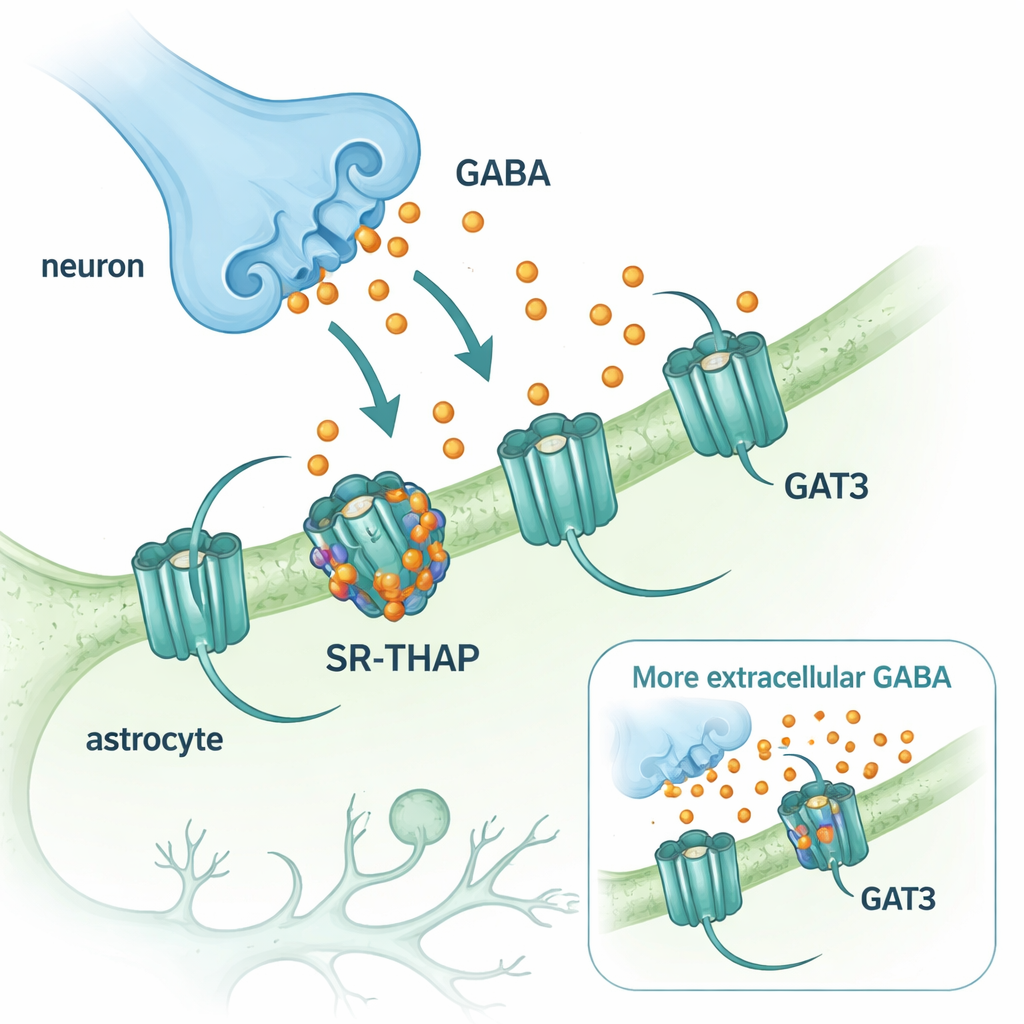
Progettare una serratura molecolare più precisa
I tentativi di inibire GAT3 sono stati ostacolati dalla mancanza di informazioni strutturali dettagliate. Molti composti del passato sono stati creati per tentativi ed errori, spesso producendo varianti ingombranti di molecole note simili al GABA. Uno dei più noti, (S)-SNAP-5114, si è rivelato chimicamente instabile e difficile da usare negli animali vivi. Partendo da un parente più resistente di questo composto, gli autori hanno sviluppato SR-THAP, una nuova piccola molecola progettata per adattarsi a GAT3 in modo più preciso e resistere alla degradazione. Esperimenti in colture cellulari umane hanno mostrato che SR-THAP blocca fortemente GAT3 e lo fa in modo non competitivo: invece di competere semplicemente con il GABA nel sito abituale, cambia il funzionamento del trasportatore, riducendone la capacità massima di trasporto.
Osservare GAT3 a risoluzione quasi atomica
Per capire esattamente come funziona SR-THAP, il gruppo si è rivolto alla criomicroscopia elettronica, una tecnica che immagina proteine congelate istantaneamente con elettroni e ricostruisce la loro forma tridimensionale. Hanno risolto tre versioni del GAT3 umano: legato a SR-THAP, legato al GABA e in uno stato privo di substrato. Tutte e tre rivelano l’architettura tipica vista in trasportatori correlati di neurotrasmettitori: 12 eliche strettamente impacchettate che attraversano la membrana e formano un percorso centrale per il GABA e i suoi ioni compagni, sodio e cloro. Nella struttura legata al GABA, il trasportatore si trova in uno stato «inward-occluded»—il GABA e uno ione sodio sono bloccati al centro, sigillati sia dall’esterno sia dall’interno. Un amminoacido aromatico chiave forma un’interazione specializzata con il gruppo amminico del GABA, contribuendo a spiegare come GAT3 riconosce il suo substrato.
Come SR-THAP blocca il trasportatore in posizione aperta
In netto contrasto, la struttura legata a SR-THAP cattura GAT3 in uno stato «inward-open», con il lato interno della proteina spalancato verso l’interno della cellula. SR-THAP è annidato in profondità in questa cavità interna, infilandosi tra diverse eliche che normalmente si muovono durante il ciclo di trasporto. Occupa tre piccole tasche con differenti caratteristiche chimiche, instaurando una rete di legami a idrogeno e contatti idrofobici. Questo posizionamento effettivamente inceppa il trasportatore in modo che GABA e ioni non possano più completare il loro viaggio. Gli autori mostrano che alcuni specifici amminoacidi che rivestono questa cavità differiscono tra GAT3 e i suoi stretti parenti; la sostituzione di uno di questi residui altera sia l’attività di trasporto sia la potenza di SR-THAP, aiutando a spiegare perché l’inibitore è molto più selettivo per GAT3 rispetto a GAT1 o trasportatori correlati. 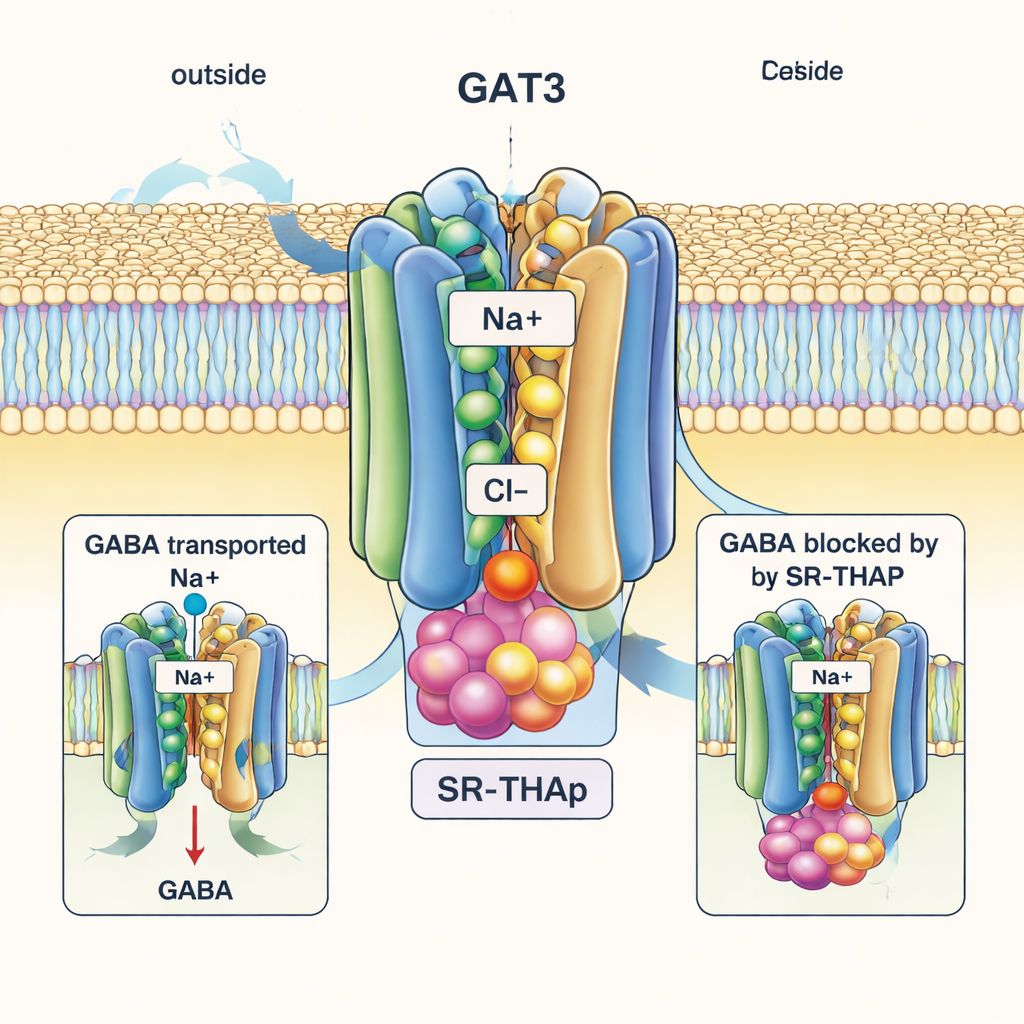
Aprire le porte a nuovi farmaci per epilessia e salute cerebrale
Complessivamente, queste strutture rivelano come GAT3 cicla tra forme diverse per muovere il GABA e come SR-THAP sfrutti una tasca interna meno conservata per bloccare quel ciclo. Per i non specialisti, il messaggio principale è che lo studio fornisce un dettagliato progetto molecolare per spegnere GAT3 in modo altamente selettivo. Compounds di questo tipo potrebbero aumentare i livelli di GABA calmante in modo più raffinato rispetto ai farmaci esistenti, portando potenzialmente a nuovi trattamenti o strumenti di ricerca per epilessia, recupero post-ictus, malattia di Alzheimer e altre condizioni in cui la segnalazione inibitoria è alterata.
Citazione: Mortensen, J.S., Bavo, F., Jensen, M.H. et al. Structural basis for selective inhibition of human GABA transporter GAT3. Nat Commun 17, 1774 (2026). https://doi.org/10.1038/s41467-026-68479-0
Parole chiave: Trasportatore di GABA, GAT3, epilessia, cryo-EM, inibizione del neurotrasmettitore