Clear Sky Science · it
Un meccanismo stocastico guida la veloce traslocazione del substrato nella macchina AAA+ ClpB
Come le macchine cellulari mantengono il movimento delle proteine
All'interno di ogni cellula, minuscole macchine molecolari tirano, spingono e rimodellano costantemente le proteine per evitare che si aggregino e per riparare i danni. Una di queste macchine, chiamata ClpB, aiuta a recuperare proteine aggrovigliate—un compito essenziale per la sopravvivenza cellulare sotto stress. Questo studio pone una domanda semplice ma profonda: come trasforma ClpB il carburante chimico ATP nel lavoro meccanico di tirare una catena proteica attraverso il suo poro centrale, e lo fa con passi ordinati e sincronizzati o in modo più casuale e diffusivo?
Un anello di soccorso proteico in azione
ClpB appartiene a una vasta famiglia di enzimi chiamati macchine AAA+ che si assemblano in strutture ad anello con un tunnel centrale. Molti sono stati riprodotti con dettagli raffinati dalla crio–microscopia elettronica, dando origine al popolare modello «mano dopo mano»: ogni molecola di ATP consumata produrrebbe un piccolo passo preciso, come una squadra che tira una corda a turno. Tuttavia altri esperimenti suggerivano che ClpB potrebbe spostare le proteine molto più rapidamente di quanto il suo lento tasso di consumo di ATP sembrerebbe permettere. Per risolvere questo enigma, gli autori hanno osservato singole molecole di ClpB in tempo reale mentre facevano passare attraverso il loro poro una proteina di prova flessibile, la κ-caseina.
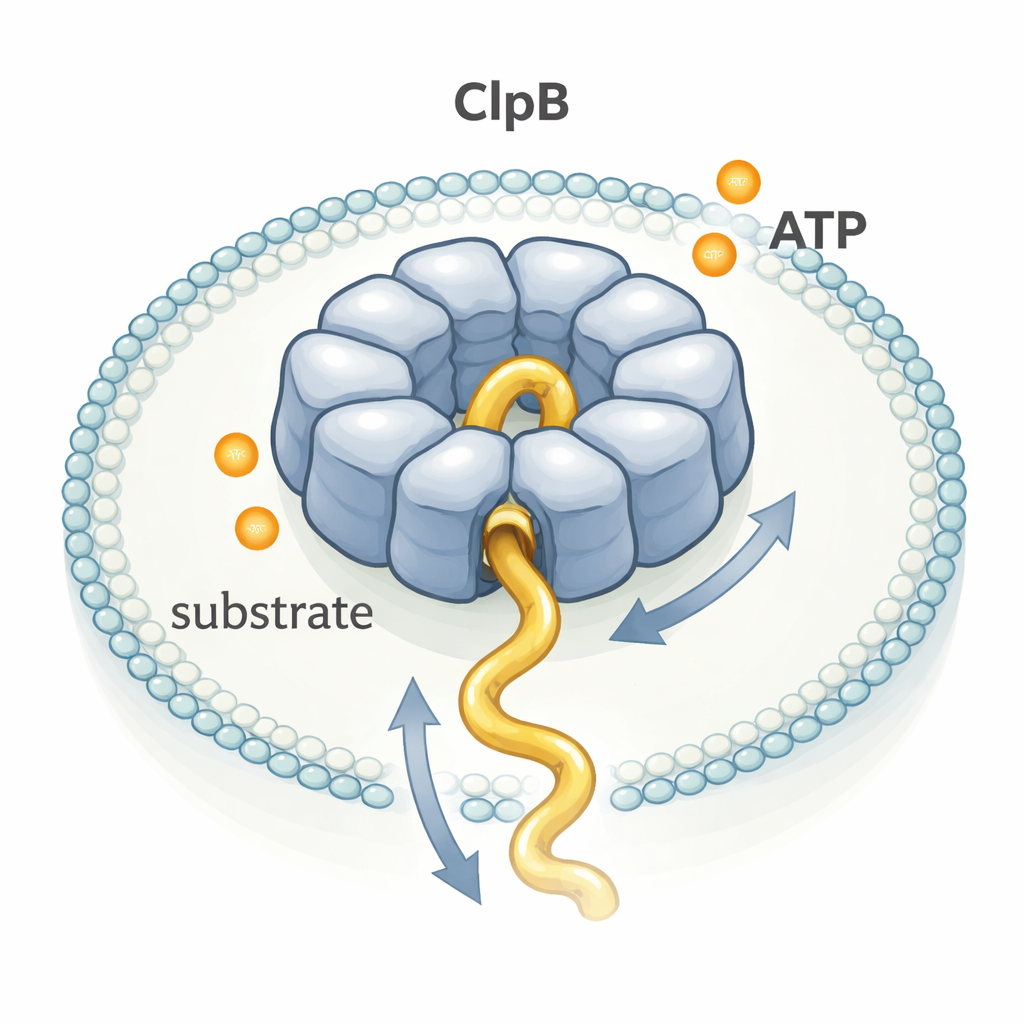
Guardare una molecola alla volta
I ricercatori intrappolarono singoli anelli di ClpB e singole molecole di κ-caseina insieme all'interno di piccole bolle lipidiche attaccate a una superficie di vetro. Aggiunsero coloranti fluorescenti in punti specifici su ClpB e sulla catena proteica, quindi usarono il FRET a singola molecola, una tecnica che segnala cambiamenti di distanza tra i coloranti su scala nanometrica. Quando la κ-caseina scivolava nel poro di ClpB, i coloranti si avvicinavano e il FRET saliva con un breve picco; quando la catena usciva, il segnale calava di nuovo. Misurando la durata e l'ampiezza di migliaia di questi picchi, poterono inferire quanto rapidamente e quanto lontano segmenti della proteina venivano infilati attraverso il poro.
Veloce, poco alimentato e quasi indipendente dalla temperatura
Con sorpresa, gli eventi di traslocazione erano estremamente rapidi: il segmento etichettato della κ-caseina attraversava tipicamente diversi nanometri del poro in circa 1–2 millisecondi—circa mille volte più veloce della media del tempo tra eventi di idrolisi dell'ATP in ClpB. La maggior parte degli eventi era così breve e seguiva una distribuzione ampia a legge di potenza piuttosto che una singola scala temporale caratteristica. Cambiare la temperatura da 10 a 32 °C rallentava a malapena questi movimenti, implicando che la barriera energetica per il moto è minima rispetto a quella di classici motori a «colpo di potenza» come la chinesina. Analogamente, ridurre la concentrazione di ATP diminuiva fortemente la frequenza con cui gli eventi avvenivano, ma aveva quasi nessun effetto sulla durata di ciascun evento. L'ATP, in altre parole, controllava quando ClpB si attivava e con quale frequenza agiva, più che la velocità dei singoli scoppi di infilamento.
Movimento avanti e indietro con una preferenza in avanti
Per verificare se le catene si muovessero sempre in un'unica direzione, il gruppo eseguì esperimenti FRET a tre colori più complessi, marcando con coloranti entrambi i lati del poro e il substrato. Questo permise loro di distinguere se la κ-caseina entrava dalla parte superiore o inferiore dell'anello e se passava completamente attraverso o retrocedeva. Scoprirono sei schemi distinti: infilamenti completi avanti e indietro, visite «parziali» più lunghe in cui la catena esplorava entrambi i lati del poro prima di uscire, e incontri fugaci vicino a un solo lato. Circa tre quarti degli eventi completi andavano in direzione avanti, ma una frazione significativa andava all'indietro, rivelando che ClpB consente una diffusione bidirezionale del substrato con soltanto un modesto bias verso il avanti. Quando l'ATP fu sostituito con un analogo idrolizzato più lentamente, gli eventi divennero rari e molto più lenti, e la preferenza in avanti scomparve praticamente del tutto.
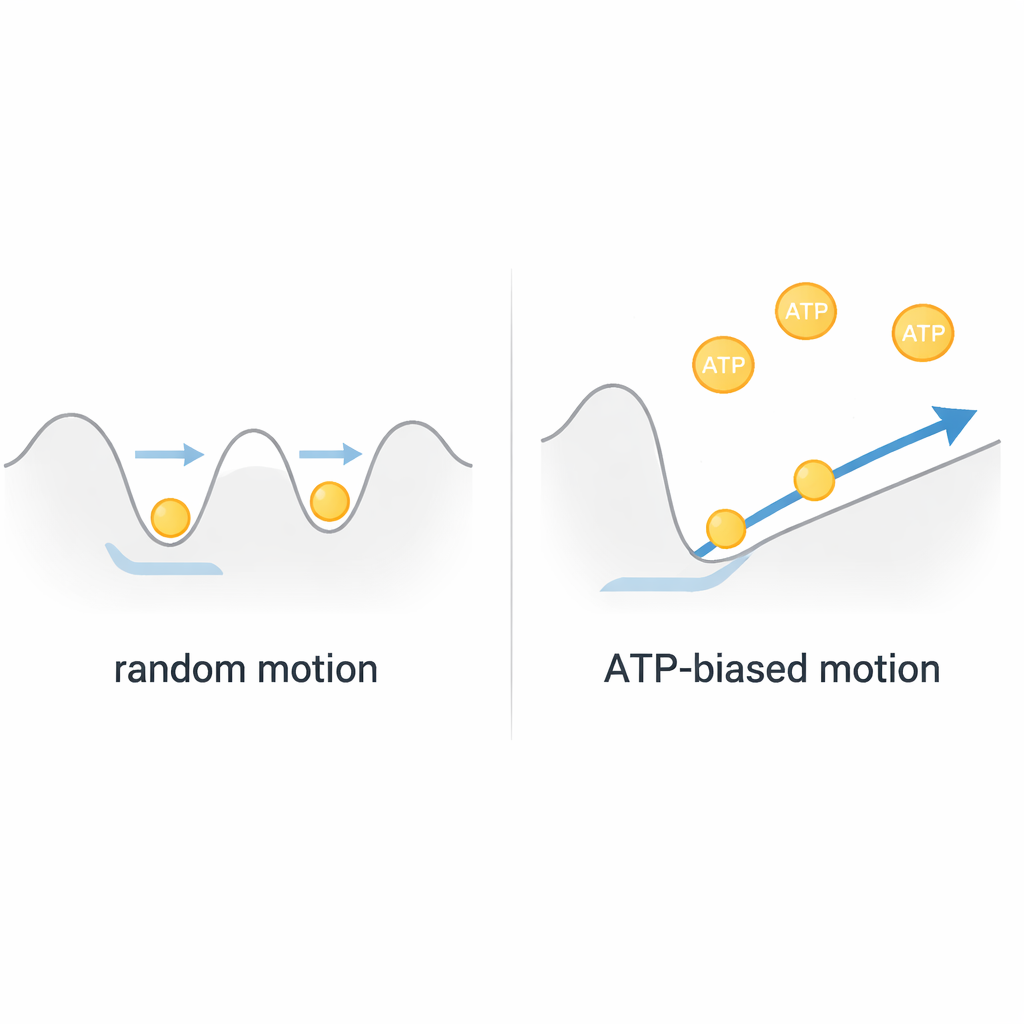
Un motore browniano, non una semplice verricello
Mettendo insieme queste osservazioni, gli autori concludono che ClpB funziona più come un motore browniano che come un verricello rigido azionato dal carburante. La catena proteica vibra termicamente all'interno di un paesaggio energetico poco profondo nel poro, muovendosi avanti e indietro ad alta velocità. L'ATP non fornisce direttamente grandi e discreti colpi di trazione; piuttosto modula la forma di questo paesaggio tramite rapidi movimenti di «sporgenze del poro» interne, favorendo sottilmente lo spostamento in una direzione. Poiché ogni evento di infilamento completo si correla con solo circa uno o due ATP consumati, ClpB ottiene un trasporto straordinariamente efficiente e rapido rettificando il moto casuale invece di contrastarlo. Questa visione riformula il modo in cui pensiamo molte macchine AAA+, suggerendo che i nanomotori biologici spesso sfruttano la casualità invece di eliminarla.
Citazione: Casier, R., Levy, D., Riven, I. et al. A stochastic mechanism drives fast substrate translocation in the AAA+ machine ClpB. Nat Commun 17, 1773 (2026). https://doi.org/10.1038/s41467-026-68478-1
Parole chiave: traslocazione delle proteine, macchina AAA+, motore browniano, chaperone molecolare, FRET a singola molecola