Clear Sky Science · it
Identificazione di PAM non canonici termotolleranti per rilevamenti CRISPR-Cas12a robusti in un unico tubo
Alzare la temperatura dei test del DNA
Test rapidi e accurati per infezioni e variazioni genetiche sono fondamentali per la medicina, ma gli attuali test del DNA spesso richiedono apparecchiature di laboratorio complesse e possono non riconoscere bersagli rari o sottili. Questo studio mostra come eseguire un test basato su CRISPR a una temperatura leggermente più alta sblocchi molti più “manici” utili nel DNA, rendendo la diagnostica in un unico tubo più veloce, più sensibile e capace di distinguere anche differenze di un solo nucleotide nel codice genetico. 
Perché CRISPR ha bisogno di un “codice di avviamento”
Strumenti CRISPR come Cas12a lavorano individuando tratti specifici di DNA, guidati da un breve RNA che funziona come stringa di ricerca. Però possono agganciarsi e iniziare l’attività solo se nelle vicinanze è presente un piccolo tag di quattro lettere, chiamato PAM, con la sequenza giusta—tradizionalmente un set ristretto che inizia con “TTT”. È come avere bisogno del numero civico prima di consegnare una lettera: se il numero giusto manca, il messaggio non arriva. Questa richiesta di PAM limita dove CRISPR può agire, un grave svantaggio quando i medici devono rilevare mutazioni specifiche, marcatori di resistenza ai farmaci o varianti virali che non si trovano accanto a questi tag classici.
Scoprire nuove “porte” a temperature più alte
I ricercatori hanno testato sistematicamente tutte le 256 possibili combinazioni di PAM a quattro lettere per valutare quanto bene potenziassero l’attività di taglio “collaterale” di Cas12a—la sua capacità di tagliare molte molecole di DNA vicine una volta trovato il bersaglio, che è la base del segnale diagnostico CRISPR. A temperatura corporea normale (37 °C), solo poche PAM non standard funzionavano bene quanto quelle classiche. Ma quando hanno aumentato la temperatura di reazione a circa 45 °C, è successo qualcosa di notevole: 82 diverse PAM non canoniche hanno improvvisamente prodotto una forte attività di taglio del segnale, pari a quella dei tag standard. Il gruppo ritiene che il calore aggiuntivo ammorbidisca la struttura locale del DNA e renda il complesso Cas12a più flessibile, abbassando la barriera al riconoscimento di queste PAM precedentemente “deboli”.
Segnale forte, tutela del template
Cas12a ha due modalità di taglio. In modalità “cis” taglia il DNA specifico che gli è stato indicato; in modalità “trans”, una volta attivato, tronca rapidamente qualsiasi filamento porta-segnale nelle vicinanze, illuminando il test. I ricercatori hanno scoperto che a temperature più alte le PAM non canoniche generavano un trans-taglio molto forte—ideale per un segnale brillante e rapido—ma mantenevano relativamente debole il cis-taglio del DNA principale. Questa combinazione è perfetta per test in un unico tubo, dove il DNA deve prima essere amplificato senza essere distrutto. Hanno anche dimostrato che in queste condizioni più calde Cas12a diventa molto più selettivo rispetto agli errori tra l’RNA guida e il bersaglio: anche una singola lettera sbagliata può spegnere il segnale, soprattutto quando si usano PAM non canoniche. 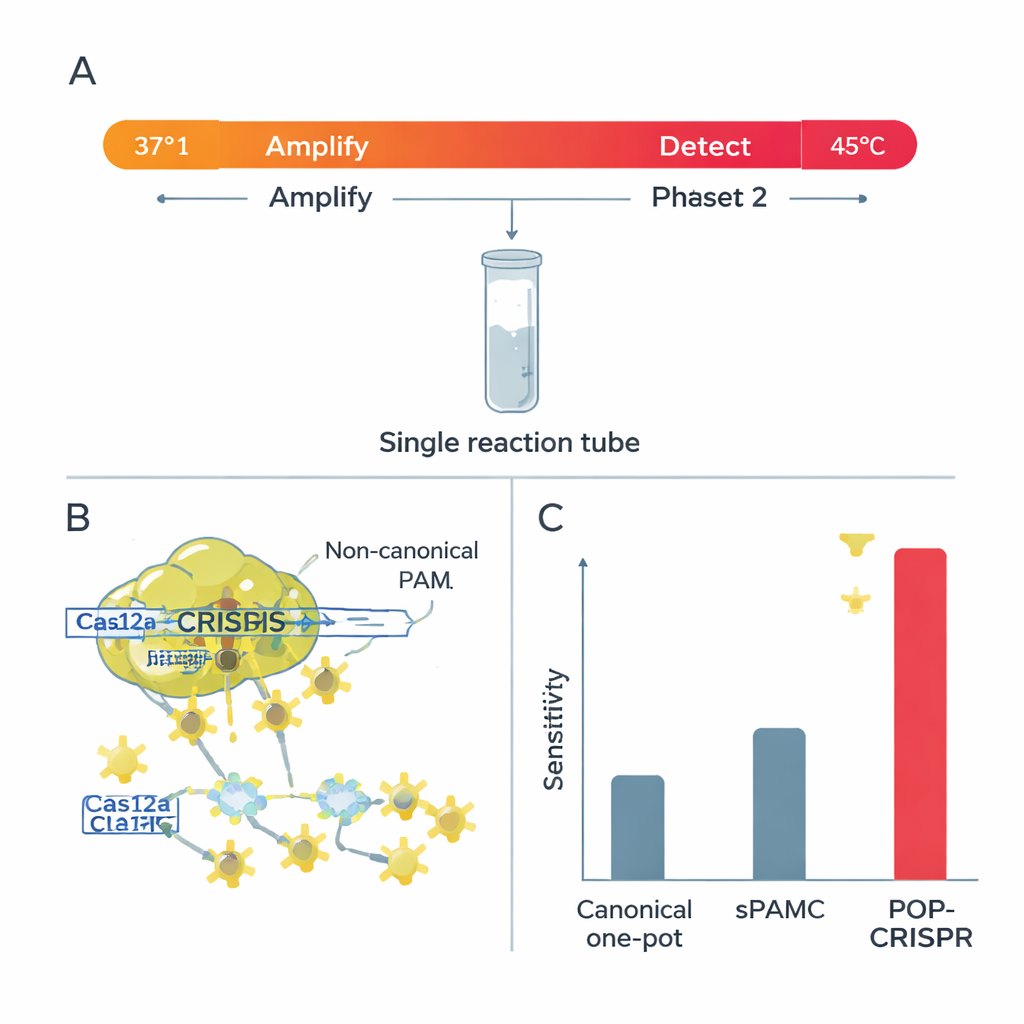
Un test one-pot più intelligente: POP-CRISPR
Sfruttando queste intuizioni, il gruppo ha creato POP-CRISPR, un saggio one-pot “poichilotermico” (a temperatura variabile). La reazione inizia intorno a 37 °C, dove un metodo di amplificazione isoterma moltiplica silenziosamente qualsiasi DNA o RNA bersaglio mentre Cas12a è relativamente inattivo. Dopo circa 10 minuti, la miscela viene riscaldata a circa 45 °C, un punto ottimale in cui Cas12a—ora guidata verso siti PAM non canonici—si attiva con un potente trans-taglio e genera un forte segnale fluorescente. Questo semplice programma a due temperature ha migliorato la sensibilità di rilevamento di circa dieci volte rispetto ai precedenti metodi one-pot CRISPR che utilizzavano anch’essi PAM deboli, e ha chiaramente sovraperformato i formati one-pot con PAM canonici convenzionali.
Dal banco al letto del paziente in pochi minuti
Il sistema POP-CRISPR è stato testato su campioni clinici reali. Ha rilevato con sensibilità il papillomavirus umano (HPV-16) in tamponi vaginali e Mycoplasma pneumoniae in tamponi respiratori, incluse casistiche a bassissima carica virale nella “zona grigia” che mettono in difficoltà i metodi standard. Crucialmente, POP-CRISPR è stato in grado di distinguere ceppi di Mycoplasma resistenti ai farmaci portatori di una singola variazione in un gene ribosomiale, nonostante non ci fosse una PAM classica vicino a quella mutazione—un compito che blocca molti test Cas12a esistenti. Per rendere l’approccio adatto al campo, gli autori hanno abbinato un rapido passaggio di lisi heat-and-Chelex di due minuti (evitando un’estrazione completa del DNA) a un lettore di fluorescenza tascabile controllato da uno smartphone. Insieme, questo flusso di lavoro può trasformare un tampone grezzo in un risultato digitale sì/no in circa 20 minuti.
Cosa significa per il test quotidiano
Aumentando la temperatura di reazione e sfruttando un insieme molto più ampio di “porte” PAM, questo lavoro trasforma Cas12a in un sensore più flessibile e preciso. POP-CRISPR offre un rilevamento degli acidi nucleici più rapido, più sensibile e più specifico in un unico tubo chiuso, ampliando al contempo la gamma di siti genetici che possono essere mirati—incluse mutazioni a singola base legate alla resistenza ai farmaci o al cancro. Per i pazienti, ciò potrebbe tradursi in diagnosi più rapide sul posto e terapie meglio mirate; per ricercatori e sviluppatori di test, offre un nuovo modo potente per progettare diagnostici CRISPR più robusti e discriminanti.
Citazione: Tian, T., Zhang, T., Zhang, W. et al. Identification of thermotolerant non-canonical PAMs for robust one-pot CRISPR-Cas12a detection. Nat Commun 17, 1771 (2026). https://doi.org/10.1038/s41467-026-68476-3
Parole chiave: diagnostica CRISPR, Cas12a, siti PAM, test point-of-care, rilevamento di acidi nucleici