Clear Sky Science · it
Meccanismi strutturali per l’inibizione e l’attivazione del canale potassio umano SK2 attivato dal Ca2+ a bassa conduttanza
Perché i minuscoli canali del potassio contano
Ogni pensiero che fai e ogni battito cardiaco che percepisci dipendono da segnali elettrici nelle tue cellule. Questi segnali sono modellati da pori microscopici, detti canali ionici, che permettono agli atomi carichi di fluire dentro e fuori. Una di queste famiglie, i canali potassio a piccola conduttanza attivati dal calcio (canali SK), contribuisce a controllare come i neuroni sparano e come il cuore mantiene il suo ritmo. Questo studio rivela, a livello atomico, come diversi farmaci e una tossina d’ape possano spegnere o potenziare un protagonista chiave di questa famiglia, il canale umano SK2 — informazioni che potrebbero guidare nuovi trattamenti per patologie che vanno dalla fibrillazione atriale al tremore e ai disturbi della memoria.
Come i canali SK2 agiscono da freni cellulari
I canali SK2 si trovano nella membrana cellulare e funzionano come minuscoli freni sull’attività elettrica. Quando l’interno di una cellula si riempie brevemente di ioni calcio durante un segnale elettrico, una proteina ausiliaria chiamata calmodulina percepisce questo aumento. La calmodulina è attaccata al lato interno di SK2 e, quando lega il calcio, tira una parte del canale come una corda, aprendo un cancello che lascia uscire ioni potassio. Questo flusso verso l’esterno aiuta a silenziare la cellula dopo lo spike, modulando la frequenza con cui i neuroni possono inviare segnali e la regolarità dei battiti cardiaci. Poiché i canali SK1–3 sono diffusi nel cervello e nel cuore, e SK2 è un sottotipo particolarmente importante, comprendere esattamente come si aprono, si chiudono e rispondono ai farmaci è cruciale per progettare terapie mirate.
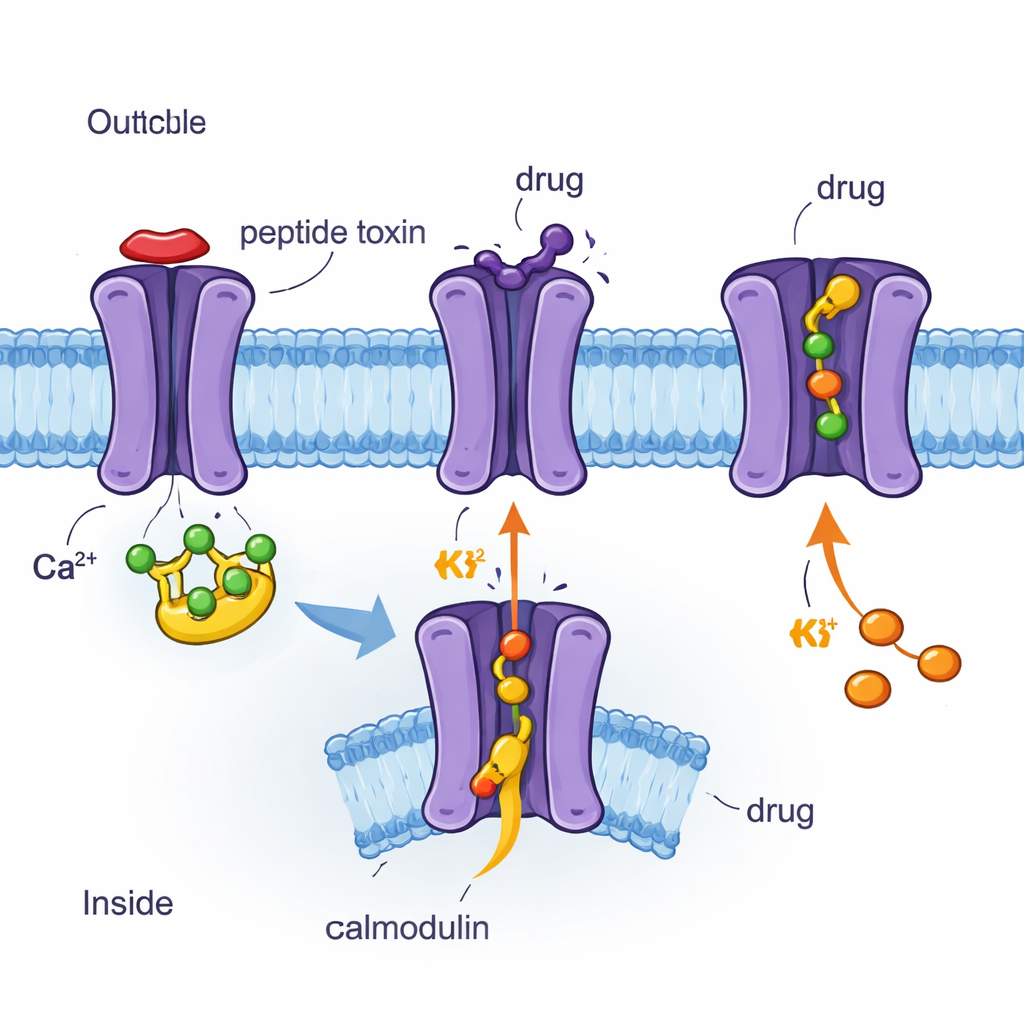
Usare la cryo-EM per vedere canali e farmaci atomo per atomo
Gli autori hanno utilizzato la criomicroscopia elettronica (cryo-EM), una tecnica che fotografa proteine congelate istantaneamente a risoluzione quasi atomica, per determinare quattro strutture tridimensionali del canale umano SK2 legato a calmodulina e a diverse molecole. Queste includevano il peptide del veleno d’ape apamina, il bloccante sintetico UCL1684, l’inibitore clinico AP30663 e l’attivatore clinico CAD-1883. Tutte e quattro le strutture mostrano SK2 come un assemblaggio in quattro parti che attraversa la membrana, con la calmodulina attaccata all’interno. Il confronto di questi istantanee ha rivelato quali parti del canale sono rigide, quali sono flessibili e come si muove la calmodulina quando il canale è nello stato chiuso o aperto. I ricercatori hanno inoltre combinato queste immagini con misure elettriche in cellule, testando come specifiche sostituzioni di amminoacidi alterano la risposta del canale a ciascun composto.
Una tossina d’ape e un farmaco di laboratorio che tappano la bocca esterna
L’apamina, un piccolo peptide proveniente dal veleno d’ape, è da tempo nota come un bloccante estremamente potente e selettivo di SK2 utilizzato nella ricerca. Le nuove strutture mostrano che l’apamina si lega come un tappo alla bocca esterna del poro di SK2. Si annida in un vestibolo a forma di coppa formato da un breve ansa tra due eliche (il collegamento S3–S4) che è ben ordinato in SK2 ma flessuoso in un canale correlato, SK4, spiegando perché SK4 è insensibile all’apamina. Residui positivamente carichi chiave sull’apamina raggiungono tra quattro catene laterali aromatiche del canale, stabilendo forti interazioni elettrostatiche e di stacking che sigillano completamente il percorso per il potassio. UCL1684, un composto bis-quinolinio sintetico, occupa sostanzialmente lo stesso tasca esterna e blocca anch’esso l’uscita degli ioni, ma la sua dimensione minore le permette di sedersi più in profondità, imitando la posizione delle fondamentali cariche positive dell’apamina. La mutazione dei residui del canale che modellano questo vestibolo riduce drasticamente la sensibilità all’apamina e, in misura minore, a UCL1684, confermando che questo ansa esterna sagomata è un determinante principale dell’azione della tossina e del farmaco.
Un tappo centrale e una cuneo interno che regolano l’attività
Al contrario, il candidato clinico AP30663 si lega all’interno della cavità centrale di SK2, proprio sotto il filtro di selettività che sceglie gli ioni potassio. Lì agisce come un tappo fisico, incuneandosi tra specifiche catene laterali che rivestono il poro. Le modifiche a questi residui di rivestimento indeboliscono la capacità di AP30663 di inibire SK2, e i confronti di sequenza spiegano perché i suoi analoghi stretti possono distinguere SK1–3 da SK4. CAD-1883, un modulatore positivo sviluppato per i disturbi del movimento, utilizza invece un’altra strategia. Si infila in una tasca all’interfaccia tra il lobo N della calmodulina e un breve collegamento (S4–S5) che accoppia il movimento della calmodulina al cancello del canale. Rafforzando i contatti in questa tasca, CAD-1883 sostanzialmente incolla calmodulina e SK2 in una configurazione che tira il cancello interno aprendolo e allargando il poro. I confronti strutturali mostrano che questo stato legato a CAD-1883 somiglia a un canale completamente aperto, sebbene il filtro di selettività possa adottare una forma inattivata dopo un’apertura prolungata.
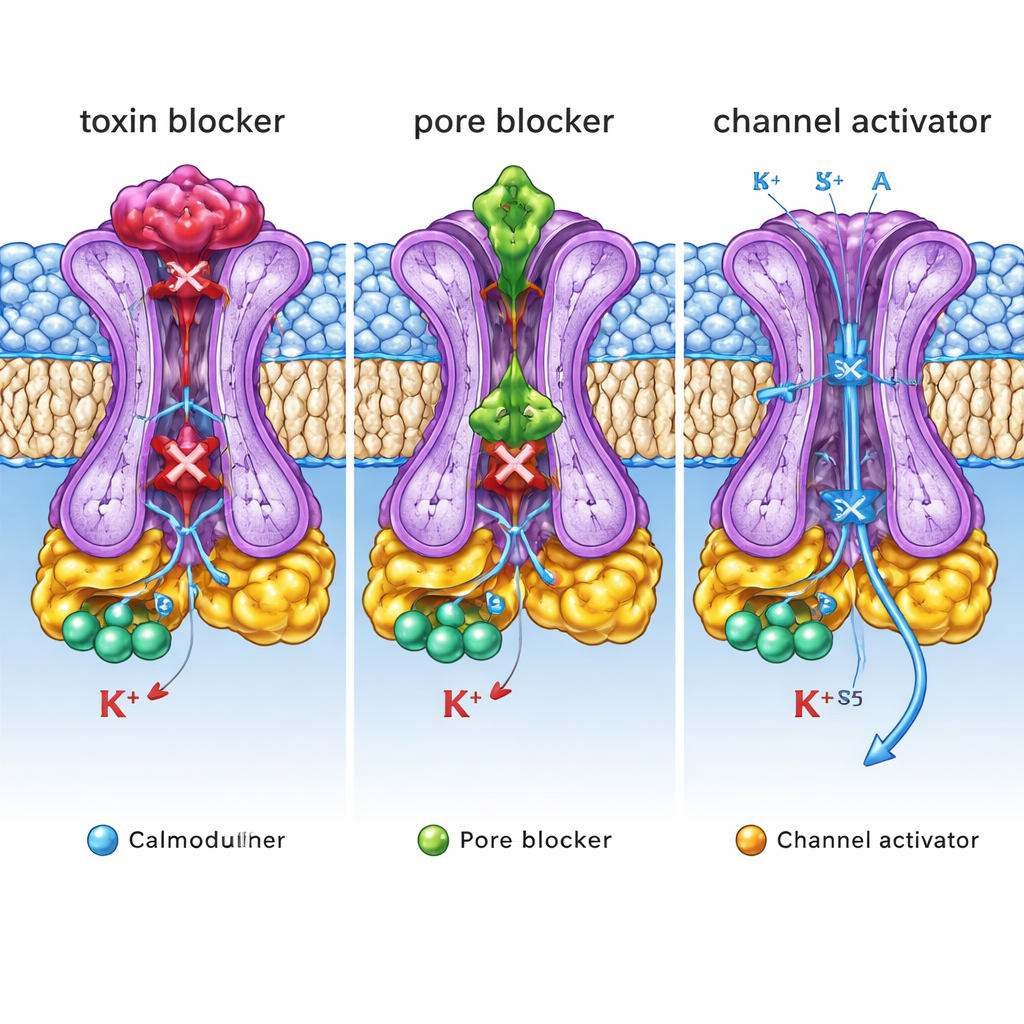
Cosa significano queste mappe strutturali per la medicina
Nel complesso, queste strutture rivelano tre distinti “manopole di controllo” su un singolo canale SK2: un coperchio esterno dove si posizionano tossine e alcuni bloccanti, una cavità interna del poro dove altri inibitori ostruiscono il flusso, e una tasca laterale dove gli attivatori stabilizzano l’apertura. Per un non specialista, il messaggio chiave è che lo stesso canale ionico può essere regolato in senso inibitorio o attivatorio da farmaci che agiscono su maniglie strutturali molto diverse. Mappando queste maniglie con precisione atomica e collegandole a effetti funzionali, questo lavoro fornisce un progetto dettagliato per la progettazione di molecole di nuova generazione che attenuino o potenzino selettivamente l’attività di SK2. Farmaci su misura di questo tipo potrebbero un giorno contribuire a normalizzare ritmi cerebrali anomali, alleviare i tremori o correggere battiti cardiaci irregolari con minori effetti collaterali.
Citazione: Ma, B., Wu, D., Cao, E. et al. Structural mechanisms for inhibition and activation of human small-conductance Ca2+-activated potassium channel SK2. Nat Commun 17, 1770 (2026). https://doi.org/10.1038/s41467-026-68475-4
Parole chiave: Canali potassio SK2, canali attivati dal calcio, strutture cryo-EM, modulatori di canali ionici, fibrillazione atriale e tremore