Clear Sky Science · it
Sistemi di editing delle basi divisi mediati da eterodimeri a coiled-coil permettono sostituzioni nucleotidiche flessibili e robuste
Riparare il DNA con meno effetti collaterali
Molte malattie sono causate da piccoli errori nel nostro DNA—sbagli di una singola lettera che possono avere conseguenze potenzialmente letali. Gli scienziati dispongono di strumenti potenti, chiamati editor delle basi, che possono correggere questi errori senza tagliare il DNA, ma questi strumenti sono ingombranti e difficili da veicolare in modo sicuro nell’organismo. Questo articolo presenta un nuovo modo di dividere gli editor delle basi in componenti più piccoli e intelligenti che mantengono l’efficacia — o la superano — rispetto all’originale, aprendo nuove strade per trattamenti di malattie genetiche nel fegato, nei muscoli e oltre.
Perché la dimensione è un problema per gli strumenti di correzione genetica
Gli editor delle basi combinano componenti del sistema CRISPR con enzimi capaci di scambiare una lettera del DNA con un’altra, ad esempio trasformando una A in G o una C in T. Queste sostituzioni precise sono promettenti per trattare condizioni come ipercolesterolemia o distrofia muscolare. Tuttavia, un vettore di consegna leader per la terapia genica, il virus adeno-associato (AAV), può trasportare solo circa 4,7 mila basi di DNA, mentre gli editor standard sono più grandi. Lavori precedenti hanno provato a dividere questi editor usando speciali “forbici” proteiche chiamate inteine, o riducendoli con enzimi compatti, ma questi approcci spesso riducevano l’efficienza, aumentavano la complessità di progettazione o limitavano i siti genomici in cui gli strumenti potevano agire.
Usare il velcro molecolare per ricostruire l’editor
Per risolvere il problema, i ricercatori hanno progettato un editor delle basi “diviso” tenuto insieme da piccole cerniere proteiche conosciute come eterodimeri a coiled-coil—come un pezzo di velcro molecolare. Hanno separato l’editor delle basi in due parti: una contenente la Cas9 nickasi che riconosce il DNA e l’altra contenente l’enzima di editing. Brevi peptidi a coiled-coil su ciascuna metà si riconoscono e si assemblano quando entrambe le metà raggiungono lo stesso tratto di DNA. Questo genera editor a coiled-coil (CC‑BE), comprese versioni che editano C (CC‑CBE), A (CC‑ABE) e varianti più complesse che possono effettuare diversi tipi di cambiamenti di lettera. 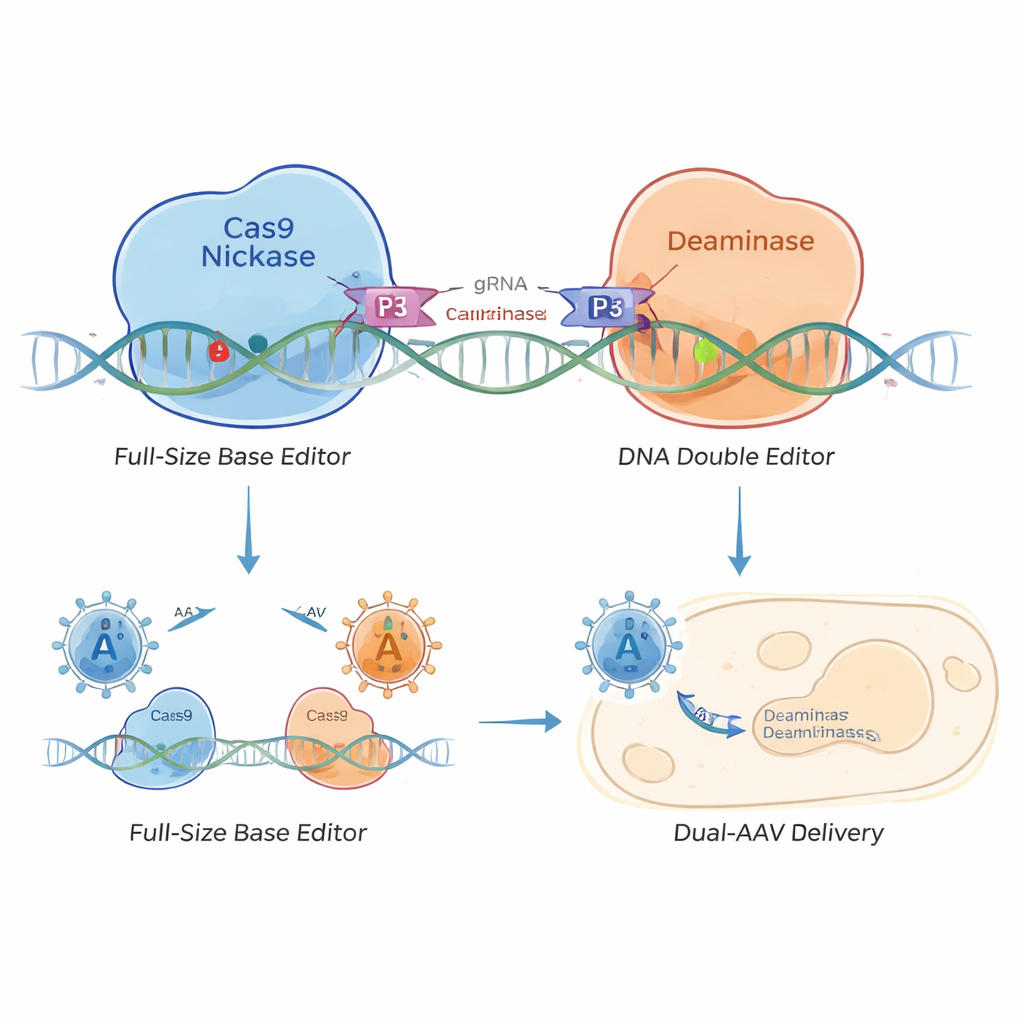
Editing flessibile, potente e preciso
Il team ha testato i CC‑BE in diversi tipi cellulari, incluse cellule umane e cellule primarie suine, e con diverse forme di Cas9 che riconoscono una gamma più ampia di sequenze di DNA. Le versioni CC‑CBE non solo hanno funzionato in modo affidabile su molti siti, ma hanno anche mostrato una “finestra di editing” più ampia, cioè la capacità di modificare lettere bersaglio su un tratto di DNA più esteso, offrendo agli scienziati maggiore flessibilità nella scelta degli RNA guida. Le versioni CC‑ABE hanno raggiunto efficienze simili ai migliori editor adenina esistenti, spesso producendo meno sottoprodotti fuori bersaglio. I ricercatori hanno inoltre adattato la strategia del coiled‑coil a design di editor più recenti—come il compatto TadCBE e il preciso ABE9—trovando ancora una volta che dividere gli strumenti con coppie a coiled‑coil ne preservava o migliorava le prestazioni.
Dalle colture cellulari ai topi viventi
In modo cruciale, gli autori hanno dimostrato che questi editor divisi funzionano all’interno di organismi viventi usando una consegna duale con AAV, dove ogni particella virale porta metà dell’editor. Nei topi, un CC‑ABE mirato al gene Pcsk9 nel fegato ha ottenuto modifiche da A a G a tassi fino a circa il 70%, riducendo drasticamente la proteina Pcsk9 e il colesterolo LDL nel sangue senza segni di danno epatico. 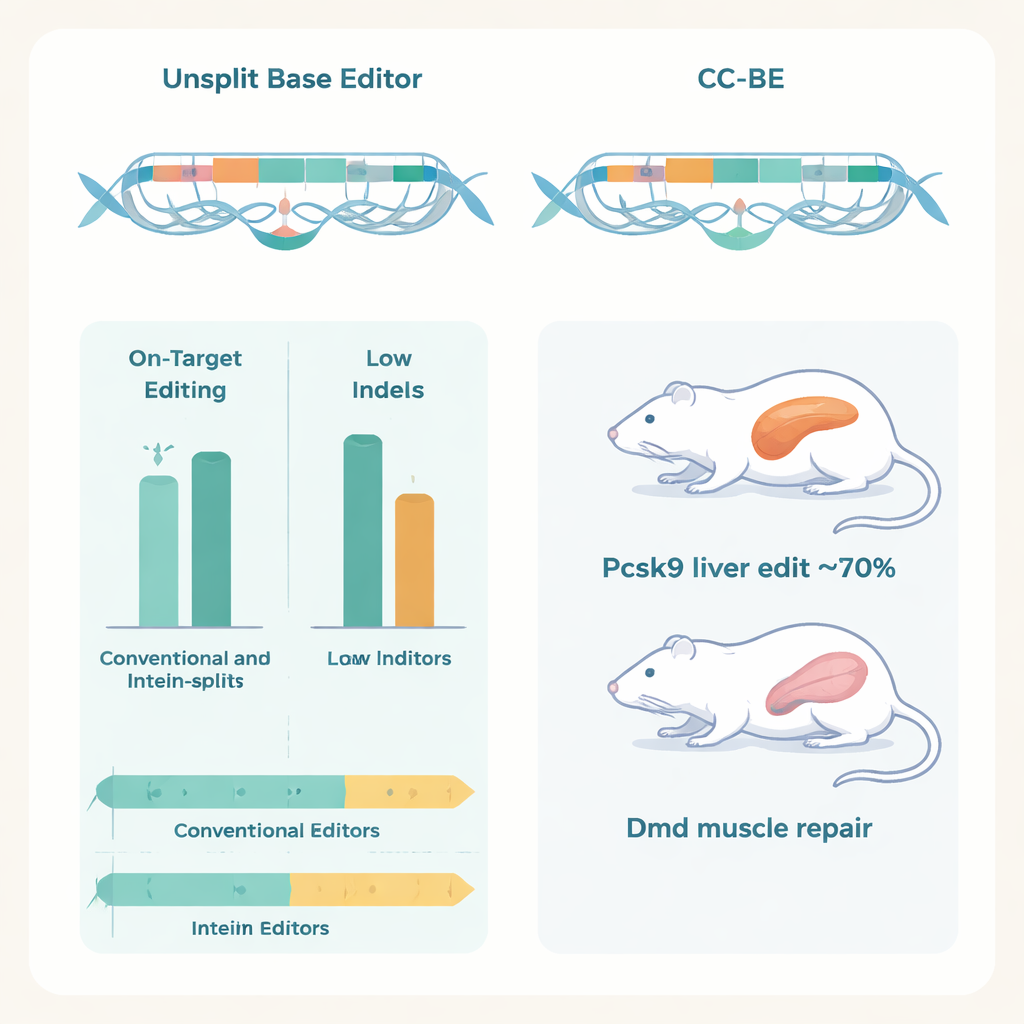
Una nuova strada verso la riparazione pratica del DNA
In sostanza, questo studio presenta un trucco di ingegneria semplice ma potente: usare piccoli “ganci” a coiled‑coil per dividere grandi editor delle basi in moduli delle dimensioni compatibili con AAV che si riuniscono solo dove serve. Per i non esperti, il messaggio è che gli scienziati possono ora imballare strumenti di riparazione del DNA altamente efficaci in vettori virali clinicamente collaudati senza sacrificare precisione o potenza. Questo approccio a coiled‑coil potrebbe semplificare la progettazione di trattamenti per un’ampia gamma di malattie genetiche causate da singole lettere in organi come fegato, cuore e muscolo, avvicinando la correzione genetica di precisione a terapie reali.
Citazione: Mu, S., Li, Q., Chen, M. et al. Coiled-coil heterodimer-mediated split base editing systems enable flexible and robust nucleotide substitutions. Nat Commun 17, 1765 (2026). https://doi.org/10.1038/s41467-026-68469-2
Parole chiave: editing delle basi, terapia genica, CRISPR, consegna con AAV, malattia genetica