Clear Sky Science · it
Imprinting dipendente da H3K27me3 e regolazione trascrizionale negli embrioni di topo precoci richiede la restrizione dell’attività di PRC2 mediata da EZHIP
Perché i piccoli embrioni necessitano di un timing genetico accurato
Ogni mammifero inizia la vita come una singola cellula che porta un set di cromosomi dalla madre e uno dal padre. Sebbene questi due pacchetti genetici contengano quasi le stesse lettere del DNA, arrivano avvolti in tag chimici differenti che aiutano a decidere quali geni si accendono o si spengono. Questo studio esplora come uno di questi sistemi di marcatura venga mantenuto in equilibrio durante i primi giorni dopo la fecondazione nei topi, e perché disturbare quell’equilibrio può deviare lo sviluppo normale.
Due genitori, due genomi impacchettati diversamente
Nei mammiferi, certi geni si comportano diversamente a seconda che provengano dalla madre o dal padre, un fenomeno chiamato imprinting genomico. L’imprinting classico si basa su marchi chimici sul DNA stesso, ma negli ultimi anni gli scienziati hanno scoperto un secondo tipo, più transitorio, dipendente da una modifica delle proteine istoniche chiamata H3K27me3. Questi istoni agiscono come rocchetti attorno a cui il DNA è avvolto, e H3K27me3 tende a spegnere i geni nelle vicinanze. Negli embrioni normali di topo, il genoma materno porta più di questo marchio rispetto a quello paterno subito dopo la fecondazione, contribuendo a silenziare copie geniche materne specifiche permettendo invece alle copie paterne di funzionare.
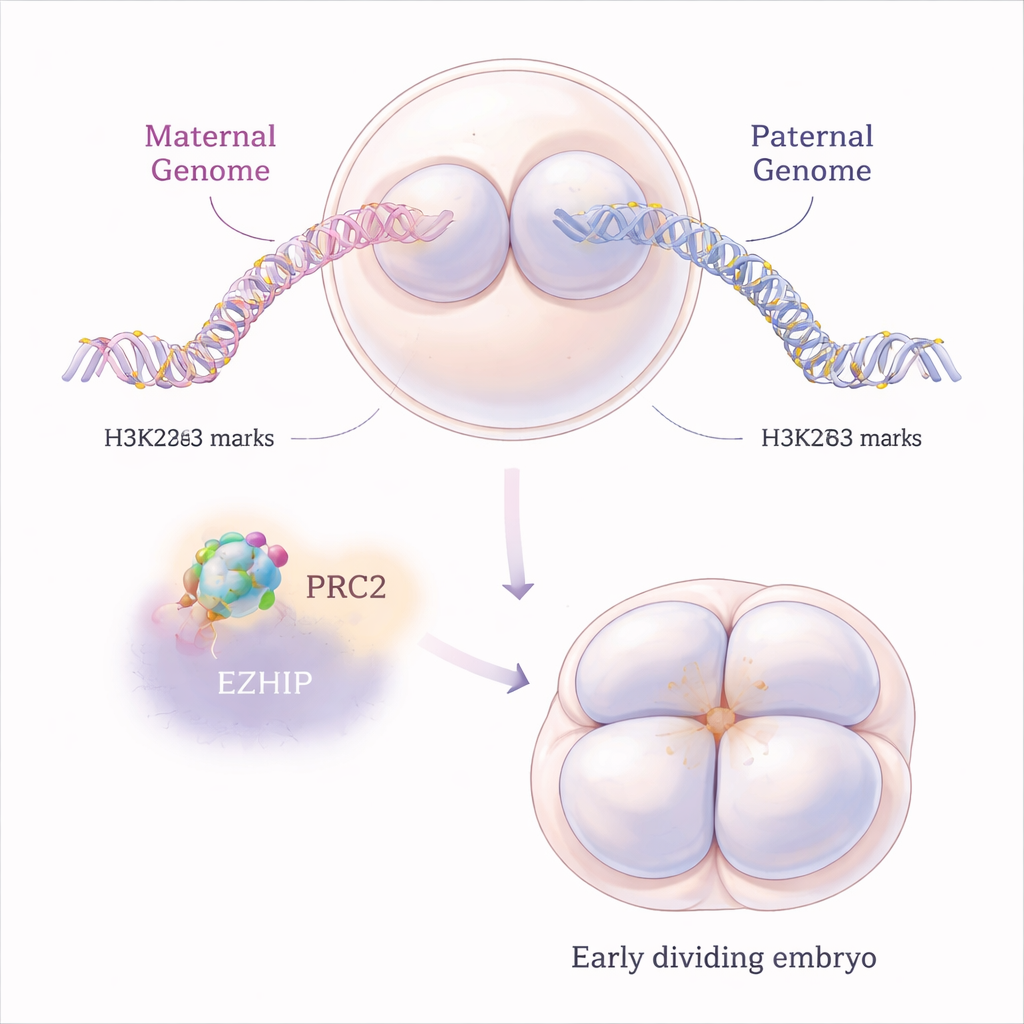
Un freno molecolare su un potente repressore
H3K27me3 viene depositato sulla cromatina da una grande macchina proteica chiamata PRC2. Gli autori si sono concentrati su EZHIP, una proteina meno nota che si lega a PRC2 e ne rallenta l’attività. Le cellule uovo di topo producono molto RNA di Ezhip, e la proteina EZHIP risultante persiste negli embrioni per le prime divisioni cellulari. Studiando topi le cui madri mancavano di Ezhip, i ricercatori hanno indagato cosa accade quando questo freno naturale viene rimosso. Hanno osservato che, senza EZHIP, ovuli ed embrioni precoci accumulano marchi H3K27me3 aggiuntivi, ma in modo sorprendentemente “appiattito”: invece di domini netti e ben definiti, il marchio repressivo si è diffuso più ampiamente confondendo i pattern normali e interessando sia i cromosomi materni sia quelli paterni.
Quando un eccesso di repressione rompe l’imprinting
Utilizzando metodi sensibili di mappatura del genoma, il gruppo ha mostrato che l’asimmetria usuale tra i paesaggi di H3K27me3 materni e paterni è in gran parte persa negli embrioni che si sviluppano da ovuli privi di Ezhip. Molte regioni che normalmente mantengono H3K27me3 su una sola copia parentale ora lo acquisivano su entrambe, o avevano i loro pattern sfumati. Questo cambiamento ha avuto conseguenze importanti per i geni imprintati che sono normalmente controllati da H3K27me3 piuttosto che dalla metilazione del DNA. Negli embrioni di controllo, questi geni tendono a essere espressi prevalentemente dall’allele paterno. Negli embrioni privi di EZHIP materno, però, gli stessi geni venivano spesso attivati da entrambe le copie parentali e i livelli complessivi di RNA per molti di essi aumentavano invece di essere doppiamente silenziati.
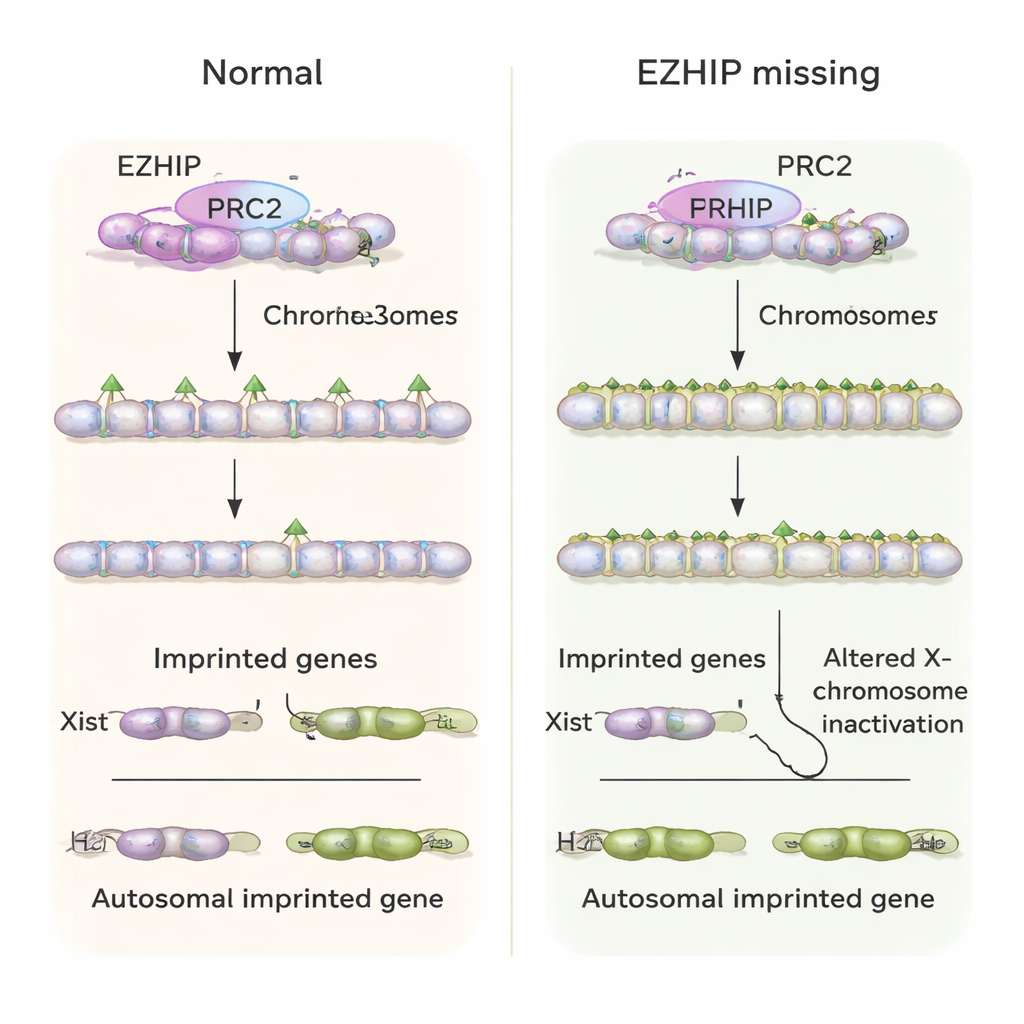
Controllo del cromosoma X alterato e salute dell’embrione
Un gene imprintato chiave dipendente da H3K27me3 è Xist, un lungo RNA che ricopre e inattiva un cromosoma X nelle cellule femminili per bilanciare il dosaggio genico con i maschi. Normalmente, negli embrioni di topo precoci Xist è espresso solo dall’X paterno nelle femmine, e per nulla nei maschi. In assenza di EZHIP materno, gli autori hanno osservato che gli embrioni femminili spesso esprimevano Xist da entrambi gli X, mentre gli embrioni maschili “inappropriatamente” attivavano Xist dal loro singolo X. Questo ha portato a schemi anomali di inattivazione dei geni legati all’X. A livello dell’animale intero, i topi nati da madri prive di Ezhip erano meno numerosi, e gli embrioni mostravano crescita alterata e problemi nei tessuti extraembrionali che supportano la placenta, coerenti con uno stress dello sviluppo di lunga durata causato dal fallimento precoce dell’imprinting.
Troppo di una cosa buona può essere dannoso
Per un non specialista potrebbe sembrare intuitivo che più di un marchio di silenziamento come H3K27me3 significhi semplicemente che più geni vengano spenti. Invece, questo lavoro mostra che sovraccaricare il genoma con tali marchi in uno schema errato può in realtà compromettere la loro capacità di funzionare come interruttori precisi. Rimuovendo EZHIP, i ricercatori hanno scatenato PRC2, causando una diffusione così ampia di H3K27me3 che i segnali di imprinting sono stati sfumati e regolatori critici come Xist sono stati controllati in modo errato. Lo studio evidenzia che gli embrioni precoci dipendono non solo dall’avere le molecole giuste, ma anche dal mantenere le loro attività finemente calibrate affinché i genomi materno e paterno vengano letti nel giusto equilibrio.
Citazione: Diop, S., Richart, L., Petitalot, A. et al. H3K27me3-dependent imprinting and transcriptional regulation in early mouse embryos requires EZHIP-mediated restriction of PRC2 activity. Nat Commun 17, 1758 (2026). https://doi.org/10.1038/s41467-026-68467-4
Parole chiave: epigenetica, imprinting genomico, sviluppo embrionale precoce, inattivazione del cromosoma X, Polycomb PRC2