Clear Sky Science · it
Screening CRISPR in vivo identifica membri del complesso SAGA come regolatori chiave dell'ematopoiesi
Perché mantenere l'equilibrio della produzione del sangue è importante
Ogni giorno il corpo produce silenziosamente centinaia di miliardi di nuove cellule del sangue che trasportano ossigeno, combattono le infezioni e fermano il sanguinamento. Questa produzione continua dipende da rare cellule «madri» nel midollo osseo, chiamate cellule staminali ematopoietiche. Quando il meccanismo che le controlla si guasta, le persone possono sviluppare anemia, immunodeficienza o tumori come la leucemia. Questo studio pone una domanda semplice ma potente: tra le migliaia di geni del nostro genoma, quali sono davvero essenziali per mantenere la produzione di cellule del sangue sana ed equilibrata?
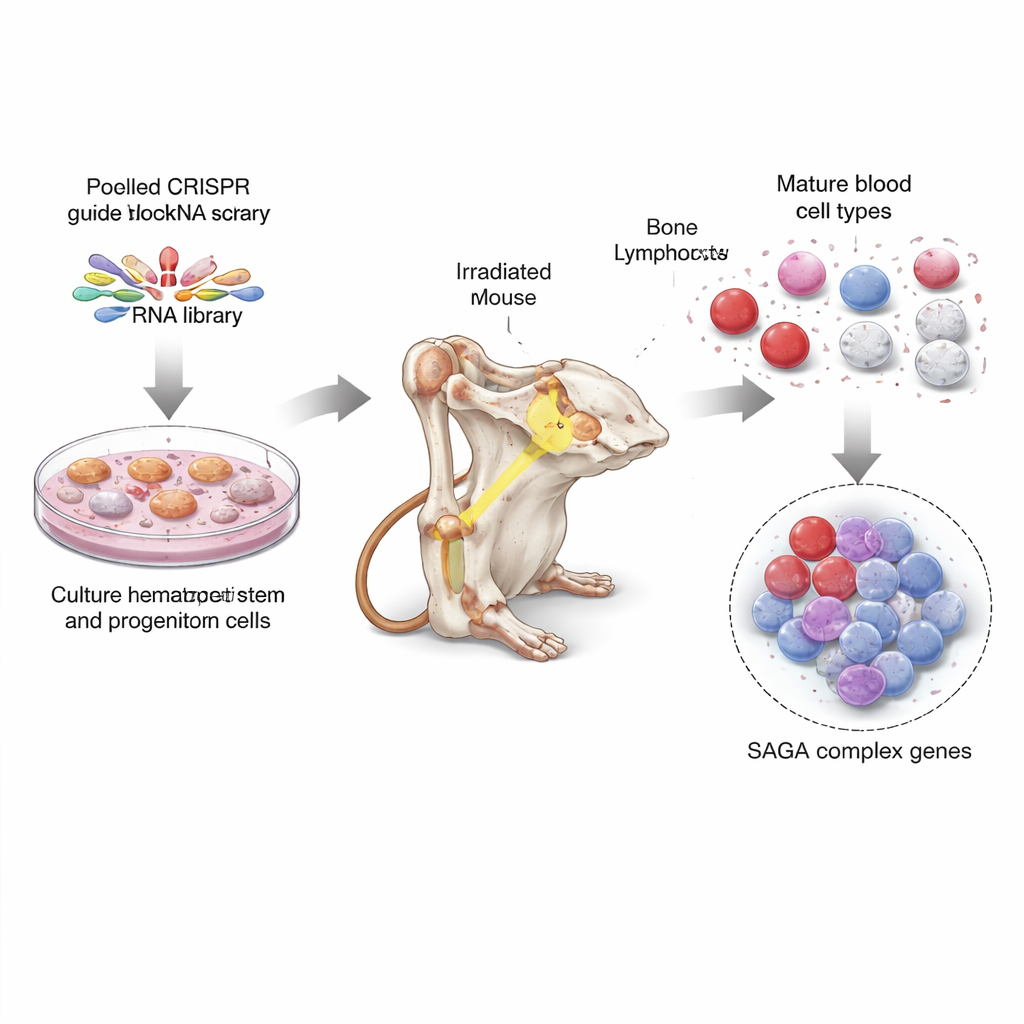
Una caccia al tesoro a livello genomico nelle cellule staminali del topo
Per affrontare il problema, i ricercatori hanno usato CRISPR, lo strumento di editing genico spesso paragonato a forbici molecolari, per spegnere quasi ogni gene del genoma del topo, con dieci guide per gene. Hanno prima coltivato grandi quantità di cellule staminali e progenitrici del midollo osseo in condizioni di cultura speciali, quindi hanno infettato queste cellule con pool di guide CRISPR in modo che ogni cellula portasse l'ablazione di un gene diverso. Successivamente hanno trapiantato queste cellule miste ed editate in dozzine di topi irradiati, permettendo alle cellule editate di ricostruire i sistemi ematopoietici degli animali. Alcuni mesi dopo, hanno purificato vari tipi di cellule del sangue mature e cellule con caratteristiche staminali dal midollo osseo e hanno letto quali guide CRISPR erano sovra- o sotto‑rappresentate. Questo ha rivelato quali perdite di geni favorivano cellule immature e quali supportavano la produzione di cellule del sangue completamente formate.
Un centro di controllo nascosto chiamato SAGA entra in evidenza
Tra i numerosi regolatori noti della formazione del sangue, è emerso un set sorprendente di hit: diversi pezzi strutturali di un grande assemblaggio proteico chiamato complesso SAGA, inclusi geni denominati Tada2b, Taf5l e Tada1. SAGA non produce direttamente cellule del sangue; piuttosto aiuta ad attivare o disattivare altri geni marcando chimicamente le proteine che impacchettano il DNA, gli istoni. Quando il team ha disattivato individualmente questi componenti di SAGA e trapiantato le cellule editate nei topi, ha osservato un modello coerente. Le cellule immature del midollo osseo si accumulavano, ma la loro capacità di maturare in globuli bianchi circolanti, globuli rossi e alcuni tipi di cellule immunitarie era fortemente ridotta. In sostanza, le cellule staminali e progenitrici restavano bloccate in un collo di bottiglia, incapaci di completare il percorso verso cellule del sangue pienamente funzionali.
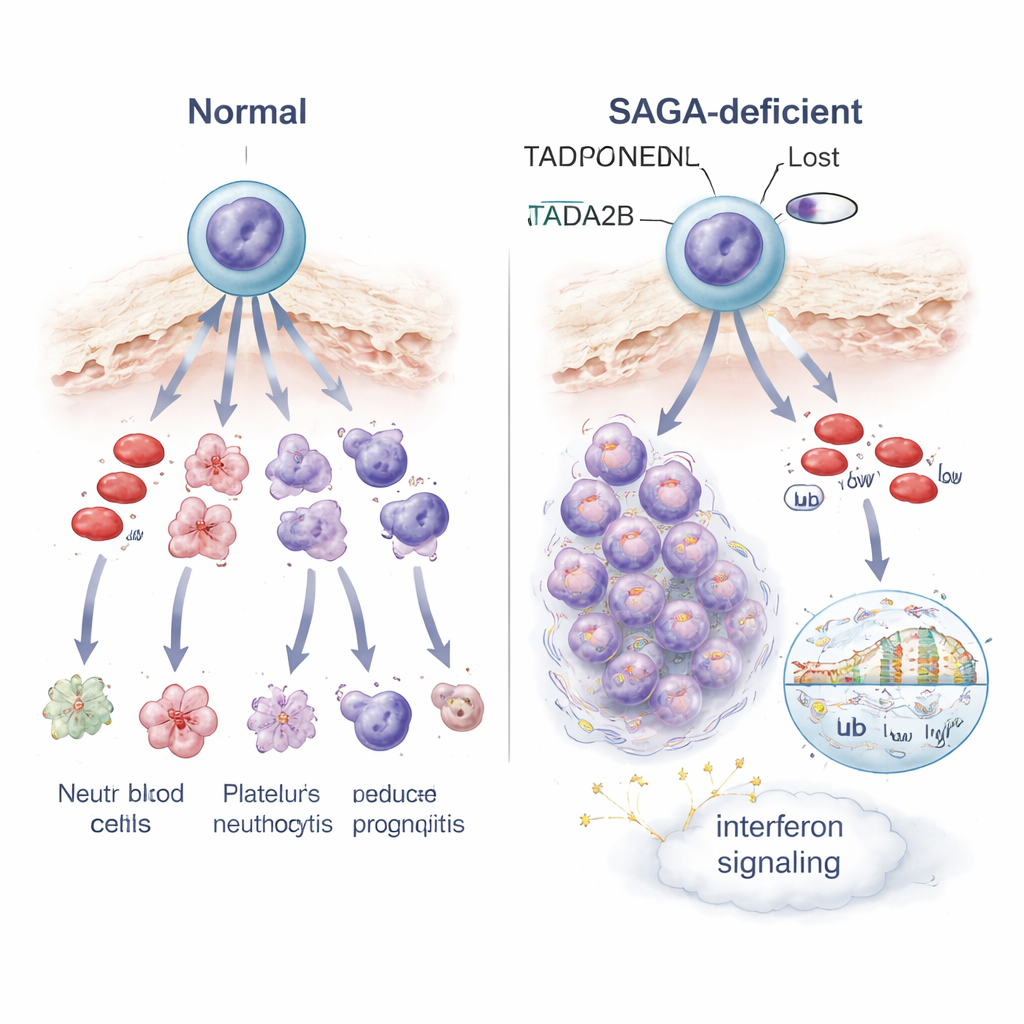
Come il controllo genico alterato cambia il destino cellulare e i segnali di stress
Per capire cosa andasse storto dentro queste cellule bloccate, gli scienziati hanno profilato l'attività genica una cellula alla volta e in popolazioni. La perdita di Tada2b o Taf5l ha riorganizzato l'attività di molti geni nelle cellule staminali, con due temi evidenti. Primo, i geni coinvolti nella segnalazione dell'interferone—normalmente parte della difesa antivirale dell'organismo—venivano attivati, indicando un allarme o uno stato di stress interno. Secondo, i mitocondri delle cellule, le piccole centrali energetiche che alimentano il lavoro cellulare, diventavano meno attivi, e le cellule alterate si mostravano più sensibili a un farmaco che prende di mira la produzione di energia mitocondriale. A livello dell'impacchettamento del DNA, le cellule prive di Tada2b presentavano livelli ridotti di una modifica istonica associata a cromatina aperta e attiva, e cambiamenti in un'altra modifica legata a come i geni vengono letti. Questi spostamenti nella chimica della cromatina spiegano probabilmente perché molti geni, inclusi quelli che guidano la corretta maturazione ematica, vengono disregolati.
Dai meccanismi di base ai modelli di malattia
Il gruppo ha poi verificato se modulare l'attività di SAGA verso l'alto o verso il basso potesse invertire questi effetti. Forzare le cellule a produrre Tada2b in eccesso ha ridotto l'attività dei geni legati all'interferone e ha diminuito la proporzione di cellule con caratteristiche staminali, l'immagine speculare del knockout. Trattare cellule staminali normali con un farmaco che inibisce le subunità enzimatiche chiave di SAGA ha riprodotto gran parte della firma dovuta alla perdita di Tada2b, rafforzando l'idea che l'attività modificatrice della cromatina di SAGA sia centrale per il suo ruolo. Infine, i ricercatori si sono rivolti a un modello cellulare umano della sindrome mielodisplastica, un disturbo pre-leucemico in cui la produzione di sangue vacilla e i percorsi dell'interferone sono spesso elevati. Quando hanno eliminato componenti di SAGA in queste cellule umane e le hanno trapiantate in topi immunodeficienti, le cellule editate hanno acquisito un vantaggio di crescita e hanno nuovamente attivato programmi genici correlati all'interferone e alla linea mieloide, suggerendo che questo hub regolatorio plasma anche il comportamento della malattia.
Cosa significa per la salute del sangue e le terapie future
Per un lettore non specialista, il messaggio chiave è che questo studio rivela un potente centro di controllo—il complesso SAGA—che aiuta le cellule staminali ematopoietiche a decidere quando restare immature, quando maturare e come evitare risposte di stress dannose. Quando parti chiave di SAGA mancano, le cellule staminali si accumulano ma non riescono a produrre sufficienti cellule del sangue funzionanti, mentre aumentano segnali di stress simili a quelli antivirali e i mitocondri si indeboliscono. Queste scoperte non solo approfondiscono la nostra comprensione di come la produzione di sangue sana venga mantenuta nel corso della vita, ma suggeriscono anche che cambiamenti sottili nell'attività di SAGA potrebbero contribuire a problemi ematici legati all'invecchiamento e a disordini come la sindrome mielodisplastica. A lungo termine, mappare questo circuito di controllo potrebbe aiutare gli scienziati a progettare terapie che spingano le cellule staminali difettose verso una produzione di sangue equilibrata e resistente.
Citazione: Shankar, A., Olender, L., Hsu, I. et al. In vivo CRISPR screening identifies SAGA complex members as key regulators of hematopoiesis. Nat Commun 17, 1756 (2026). https://doi.org/10.1038/s41467-026-68465-6
Parole chiave: cellule staminali ematopoietiche, screening CRISPR, complesso SAGA, segnalazione dell'interferone, sindrome mielodisplastica