Clear Sky Science · it
Inferire l’architettura della cromatina in un singolo locus tramite localizzazione probabilistica del DNA in situ
Come la forma 3D del DNA controlla quando i geni si attivano
Il nostro DNA viene spesso immaginato come una scala dritta, ma all’interno delle cellule si piega in anse e avvolgimenti complessi. Queste forme contano: contribuiscono a decidere quali geni si attivano, quando e dove. Questo studio presenta un nuovo modo di osservare i minuscoli arrangiamenti 3D del DNA attorno a un singolo gene all’interno di embrioni di moscerino della frutta in sviluppo, rivelando come sottili variazioni nel ripiegamento del DNA possano modificare i modelli di attività genica che definiscono il piano corporeo.
Osservare il controllo genico in un embrione in sviluppo
Durante lo sviluppo embrionale, migliaia di geni devono accendersi e spegnersi nei momenti giusti. Molte di queste decisioni sono prese da brevi tratti di DNA chiamati enhancer, che possono trovarsi a decine di migliaia di basi di distanza dai geni che controllano. Per funzionare, gli enhancer devono avvicinarsi fisicamente al gene bersaglio nello spazio 3D, formando anse che mettono in contatto siti distanti. Ma queste anse sono piccole, dinamiche e difficili da osservare. Gli autori si sono concentrati su un singolo gene, brinker (brk), nel moscerino Drosophila. Questo gene contribuisce a modellare l’embrione precoce, attivandosi in una striscia lungo il lato dell’uovo. Tre elementi di controllo vicini—due enhancer (E1 ed E2) e un elemento promotore-prossimale (PPE) accanto al gene—cooperano per produrre questo preciso motivo.
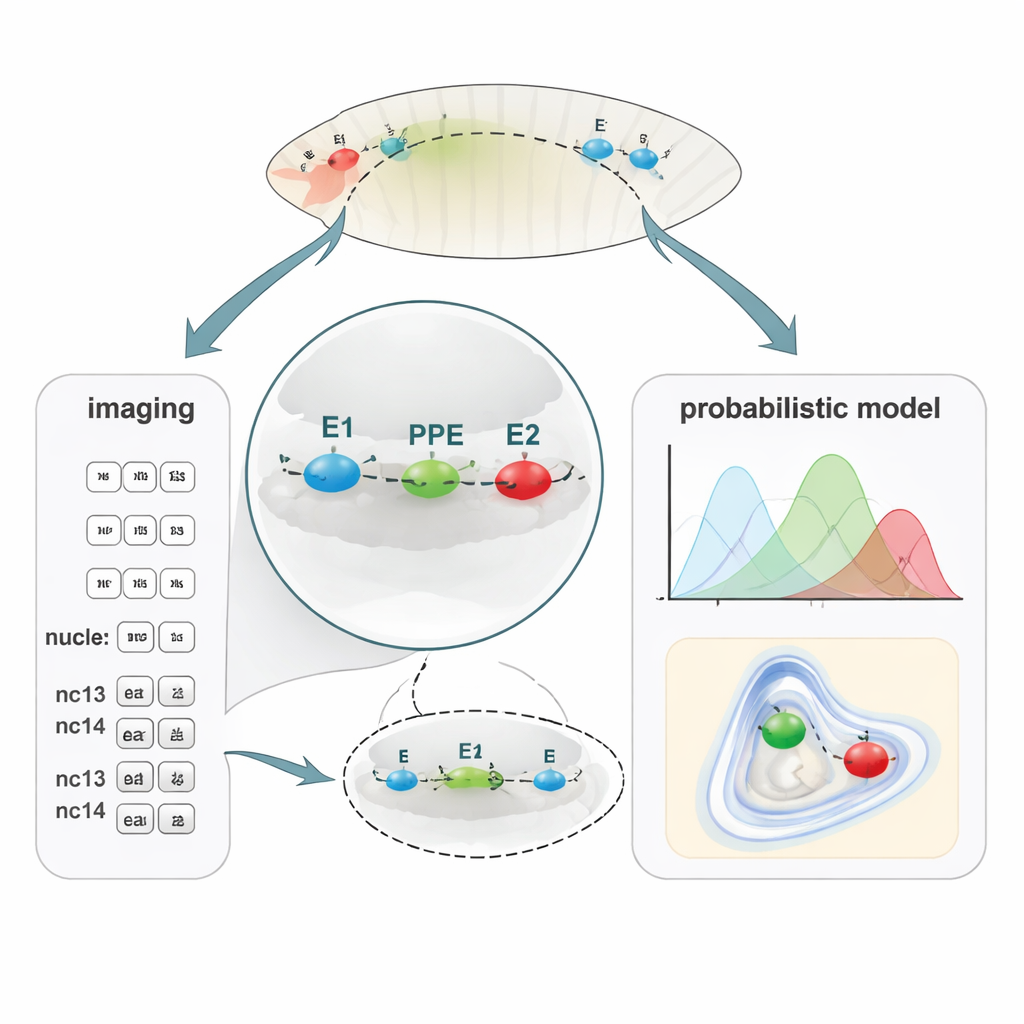
Un nuovo modo per mappare distanze di DNA minime
Per collegare il ripiegamento del DNA all’attività genica, il team ha sviluppato PLOTTED (Probabilistic Localization of Oligopaint Tagged Target Element Distances). Per prima cosa hanno usato un metodo di marcatura del DNA chiamato Oligopaint FISH per attaccare tre coloranti fluorescenti diversi alle regioni E1, PPE ed E2 in embrioni fissati. Con un microscopio confocale a super-risoluzione hanno misurato le distanze 3D fra questi tre punti colorati in decine di migliaia di nuclei attraverso embrioni in cicli nucleari successivi, da poco prima dell’inizio dell’attività genica (pre-nc13) fino a stadi successivi (nc13 e nc14). Hanno poi inserito tutte queste distanze in una pipeline computazionale personalizzata che filtra misurazioni rumorose e costruisce mappe di probabilità che mostrano dove è più probabile che ciascun elemento si trovi rispetto agli altri. Invece di produrre un’unica “ansa” statica, PLOTTED genera un paesaggio di probabili forme della cromatina a ogni stadio dello sviluppo.
Quando il DNA si compatta, il gene si risveglia
Negli embrioni normali, i ricercatori hanno osservato che, quando l’embrione raggiunge il ciclo nucleare 13, entrambi gli enhancer si avvicinano al PPE: il quartiere locale di DNA attorno al gene brk diventa più compatto. Dopo questo punto, le distanze fra i tre elementi rimangono relativamente stabili. In modo significativo, questo timing corrisponde all’inizio dell’espressione di brk, suggerendo che l’irrigidirsi della configurazione del DNA aiuta a permettere l’attivazione del gene. PLOTTED ha inoltre rivelato che questa disposizione compatta appare più frequentemente nelle regioni dell’embrione dove brk è attivo, mentre configurazioni più aperte dominano dove il gene è represso, rafforzando il legame tra architettura 3D e trascrizione.
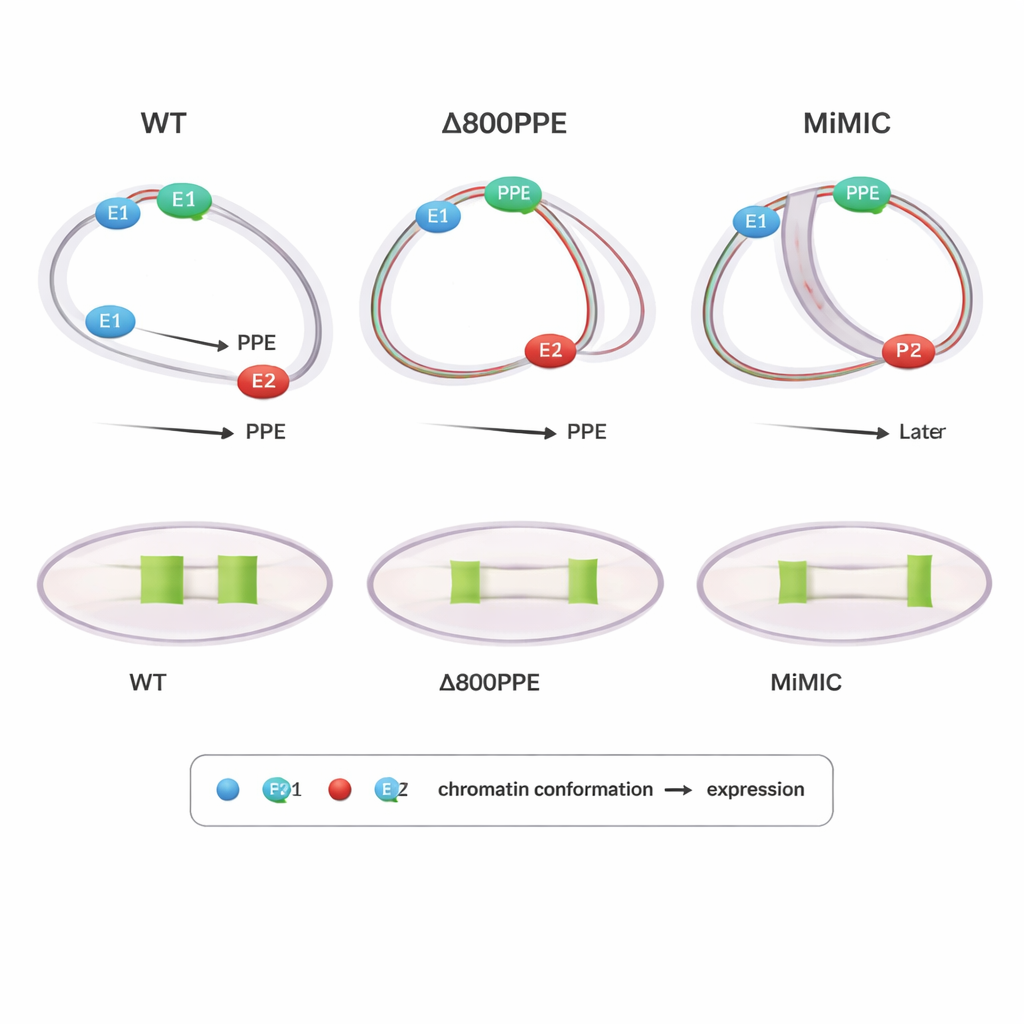
Le mutazioni mostrano perché tempo e posizione sono importanti
Per indagare causa ed effetto, gli autori hanno esaminato moscerini portatori di modifiche ingegnerizzate al locus brk. In un mutante sono stati rimossi 800 paia di basi del PPE, indebolendo questo elemento centrale; in un altro è stato inserito un cassette di 7,3 kilobasi (MiMIC) tra E1 e il PPE, spingendoli di fatto più lontano e aggiungendo un promotore extra. Entrambi i mutanti mostravano un’espressione di brk ritardata o ridotta. PLOTTED ha spiegato il perché: nella linea con delezione del PPE, la compattazione delle distanze tra il PPE e entrambi gli enhancer si verificava più tardi del normale, e negli stadi tardivi il PPE restava troppo vicino a E1, impedendo a E2 di guidare il modello di espressione ampio osservato nel tipo selvatico. Nella linea MiMIC, il PPE si associava troppo presto e con forza a E2 e solo più tardi si avvicinava a E1, perturbando di nuovo il normale passaggio di consegne tra enhancer. Questi risultati suggeriscono che non è importante solo se gli elementi si riuniscono, ma anche quando e con quale partner sono più vicini, per ottenere un output genico corretto.
Il ripiegamento del DNA varia attraverso l’embrione
Poiché PLOTTED preserva l’informazione spaziale all’interno di embrioni integri, il team ha potuto anche chiedersi se l’architettura del DNA differisca in varie regioni corporee. Confrontando le zone laterali dove brk è attivo con le zone ventrali dove è represso, hanno constatato che i tre elementi stanno più vicini nelle regioni attive e si distanziano maggiormente nei domini repressi. Lungo l’asse testa-coda hanno osservato che le distanze E1–PPE cambiano in modo differente nella parte anteriore rispetto a quella posteriore dell’embrione, suggerendo che segnali regionali modulano l’architettura della cromatina per rifinire i modelli di espressione genica. Queste osservazioni supportano l’idea che l’organizzazione 3D del DNA regolatorio sia dipendente dal contesto, tracciando sia il tempo sia la posizione nell’organismo in sviluppo.
Perché è importante oltre i moscerini
In termini semplici, questo studio mostra che il modo in cui il DNA si ripiega attorno a un singolo gene è strettamente legato a quando e dove quel gene si attiva. Il nuovo metodo PLOTTED offre un modo pratico per mappare questi minuscoli quartieri del DNA in tessuti integri usando microscopi ampiamente disponibili e chimica accessibile, combinati con un potente modello probabilistico. Sebbene dimostrato in embrioni di mosca, l’approccio è applicabile a molti organismi e modelli di malattia. Con la crescente evidenza che una cromatina mal ripiegata è alla base di disturbi dello sviluppo e tumori, strumenti come PLOTTED aiuteranno a rivelare come piccoli spostamenti nel layout 3D di enhancer e geni possano propagarsi in grandi cambiamenti nel destino cellulare e nella salute.
Citazione: Le, M.T., McGehee, J., Dunipace, L. et al. Inferring chromatin architecture at a single locus through probabilistic in situ DNA localization. Nat Commun 17, 1752 (2026). https://doi.org/10.1038/s41467-026-68460-x
Parole chiave: architettura della cromatina, interazioni enhancer-promotore, embriogenesi di Drosophila, regolazione genica, imaging a super-risoluzione