Clear Sky Science · it
DKK1 derivato dalle cellule della cresta neurale e NEDD4 modulano il segnale Wnt nel secondo campo cardiaco per orchestrare lo sviluppo del tratto di efflusso
Perché contano i piccoli costruttori del cuore
Il cuore dell'embrione precoce inizia come un semplice tubo, ma deve rapidamente rimodellarsi in un organo complesso che pompa il sangue sia al corpo sia ai polmoni. Passi falsi, anche sottili, in questo processo di costruzione possono causare gravi difetti alla nascita, incluse condizioni che richiedono interventi chirurgici subito dopo la nascita. Questo studio svela come due popolazioni cellulari si parlino mentre modellano la principale via di uscita del cuore e rivela un errore molecolare che può contribuire alle cardiopatie congenite sia nei topi che negli esseri umani.
Due squadre che costruiscono la rampa di uscita del cuore
La porzione del cuore che convoglia il sangue fuori dai ventricoli — il tratto di efflusso — si forma da una regione chiamata secondo campo cardiaco. Le cellule qui devono rimanere abbastanza plastiche come “progenitori” per essere aggiunte al tratto di efflusso in crescita e poi trasformarsi in muscolo maturo al momento giusto. Accanto a loro transitano le cellule della cresta neurale, una popolazione migrante che aiuta a costruire le grandi arterie e le valvole. Studi precedenti suggerivano che queste cellule della cresta neurale influenzino in qualche modo il secondo campo cardiaco, ma il meccanismo di questo dialogo era ignoto. 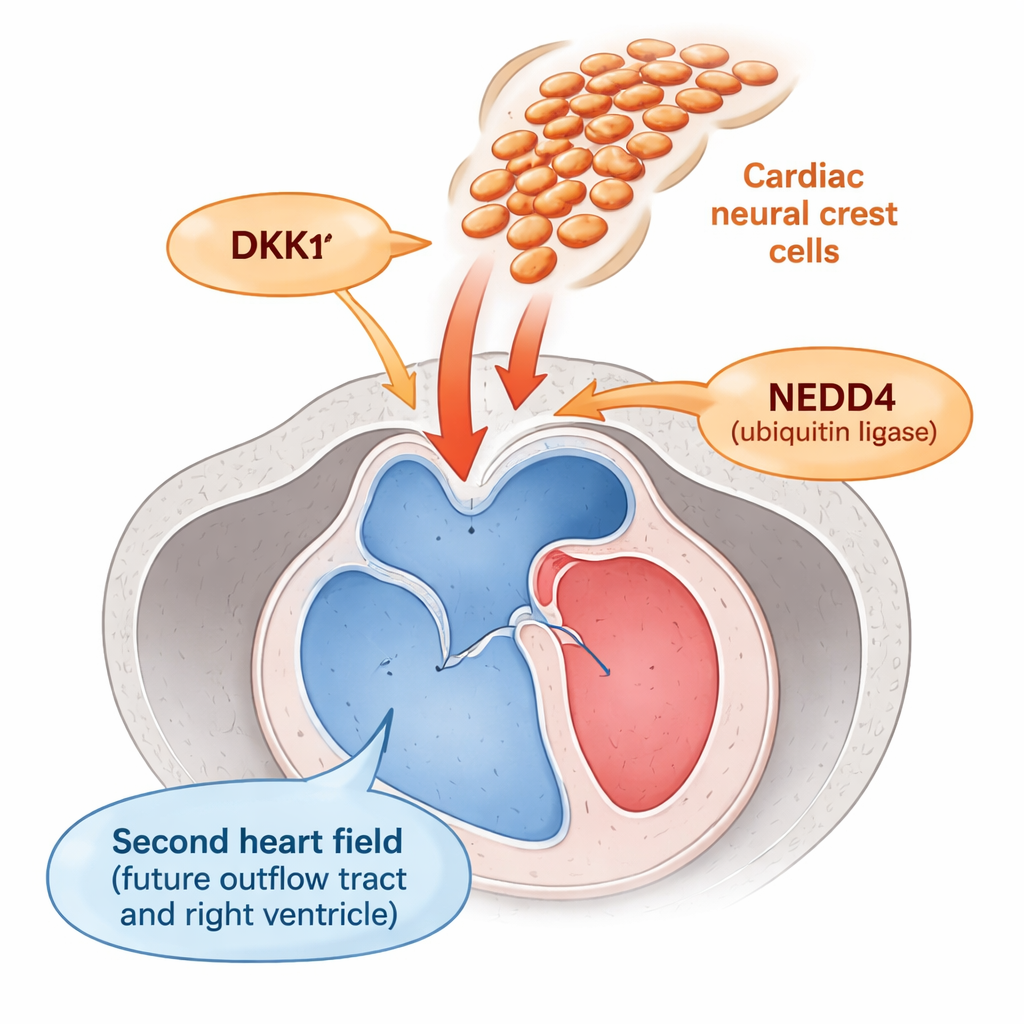
Un dimmer molecolare per i segnali di crescita
Gli autori hanno scoperto che le cellule della cresta neurale funzionano come un dimmer per un segnale di crescita chiave chiamato Wnt, che mantiene i progenitori in divisione e ritarda la loro maturazione. Hanno trovato che le cellule della cresta neurale sono una fonte principale di DKK1, una piccola proteina secreta che spegne la segnalazione Wnt nelle cellule vicine. DKK1 è normalmente regolata da NEDD4, una proteina che marca DKK1 per la degradazione. Negli embrioni di topo privi di Nedd4 specificamente nelle cellule della cresta neurale, DKK1 si accumulava a livelli anormalmente elevati. Questo eccesso di DKK1 riduceva l'attività Wnt nel vicino secondo campo cardiaco, come mostrato dalla diminuzione della beta‑catenina nucleare — un marcatore standard della segnalazione Wnt — e da livelli più bassi di diversi geni sensibili a Wnt.
Quando il timing è sbagliato, la geometria del cuore fallisce
Troppa DKK1 e troppo poco Wnt hanno avuto una conseguenza evidente: le cellule del secondo campo cardiaco hanno iniziato a trasformarsi in muscolo cardiaco troppo presto. Marker del muscolo maturo comparivano precocemente in questa zona di progenitori, e c'erano meno cellule indifferenziate disponibili per estendere il tratto di efflusso. Seguendo le cellule in divisione nel tempo, il gruppo ha mostrato che meno cellule del secondo campo cardiaco venivano aggiunte al tratto di efflusso nei mutanti. Di conseguenza, il tratto di efflusso era più corto e ruotato in modo errato, causando un disallineamento tra le grandi arterie e i ventricoli. Questi errori strutturali somigliavano a difetti conotruncali umani come il doppio sbocco del ventricolo destro e malformazioni correlate osservate nei topi completamente privi di Nedd4.
Dimostrare il ruolo del segnale e un legame con la malattia umana
Per confermare che l'alterazione della segnalazione Wnt fosse la causa di questi problemi, i ricercatori hanno modulato la via con farmaci in topo gravide. Bloccare Wnt in embrioni altrimenti sani li ha indirizzati verso la stessa differenziazione prematura e i difetti di rotazione osservati nella perdita di Nedd4, mentre ridurre la dose genica di Dkk1 sullo sfondo Nedd4‑deficiente ha parzialmente ripristinato dimensione e rotazione del tratto di efflusso. Infine, il team ha identificato un bambino con Tetralogia di Fallot che portava una rara variazione ereditata in NEDD4 che indeboliva la sua capacità di marcare DKK1 per la degradazione. Topi ingegnerizzati per portare la stessa variante di Nedd4 hanno sviluppato difetti della parete e del setto cardiaco sul lato destro, supportando l'idea che un controllo difettoso NEDD4–DKK1 possa contribuire alle cardiopatie congenite umane. 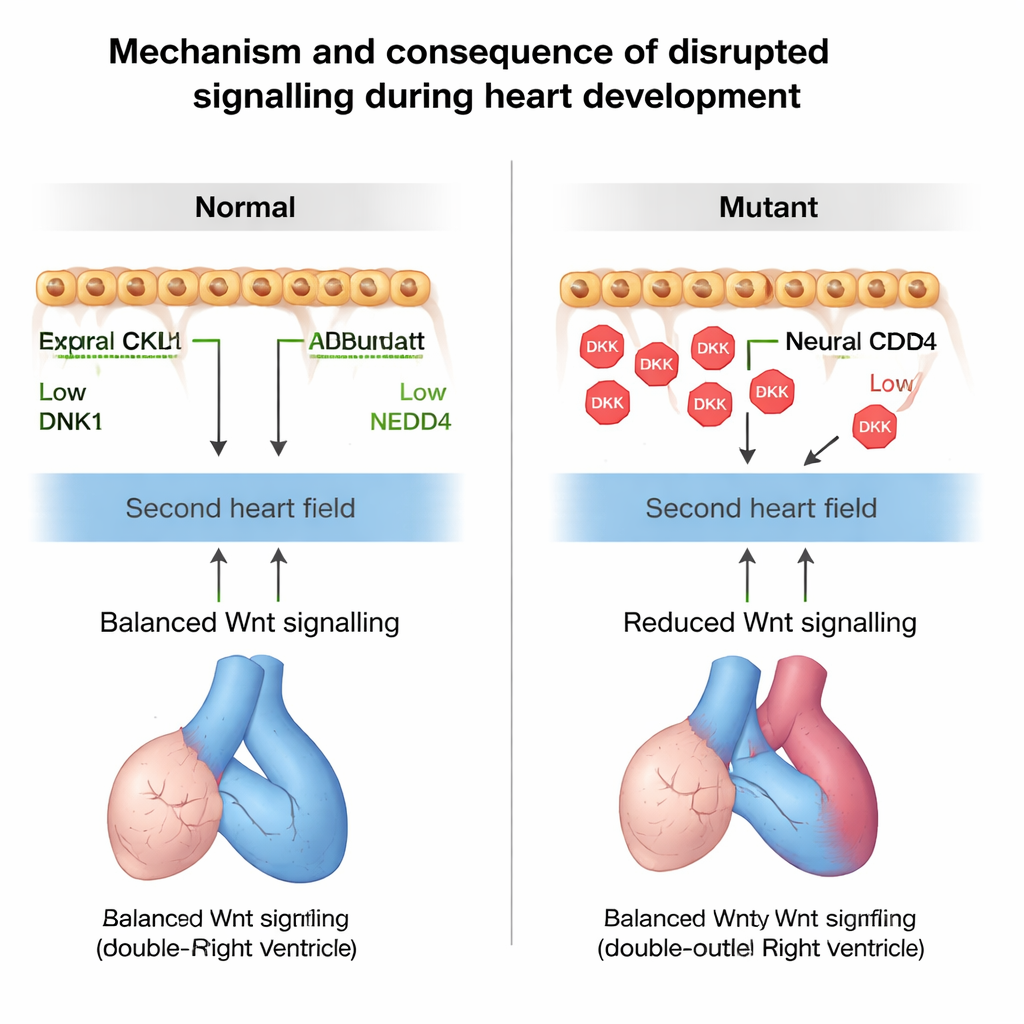
Cosa significa per la comprensione dei difetti cardiaci
Per i non specialisti, il messaggio chiave è che la “rampa di uscita” del cuore dipende dal timing preciso di quando i suoi mattoni smettono di moltiplicarsi e cominciano a diventare muscolo. Questo timing è controllato non solo dall'interno del tessuto cardiaco, ma anche dalle cellule della cresta neurale vicine che modulano finemente un segnale di crescita tramite la coppia NEDD4–DKK1. Quando questo dimmer molecolare resta troppo basso, il tratto di efflusso è sottosviluppato e disallineato, portando a gravi difetti congeniti. Mappando questa via e collegandola a una variante genetica umana, lo studio offre nuovi indizi su come insorgano alcune cardiopatie congenite e indica possibili bersagli molecolari per futuri strumenti diagnostici o interventi.
Citazione: Wiszniak, S., Alankarage, D., Lohraseb, I. et al. Neural crest cell-derived DKK1 and NEDD4 modulate Wnt signalling in the second heart field to orchestrate outflow tract development. Nat Commun 17, 1751 (2026). https://doi.org/10.1038/s41467-026-68459-4
Parole chiave: cardiopatia congenita, sviluppo del cuore, cellule della cresta neurale, segnalazione Wnt, tratto di efflusso cardiaco