Clear Sky Science · it
Varianti funzionali in 1p36.23 conferiscono rischio di schizofrenia modulando RERE
Perché piccoli cambiamenti nel DNA contano per la salute mentale
La schizofrenia è una grave malattia mentale che altera il modo in cui le persone pensano, provano emozioni e si relazionano agli altri. È fortemente ereditaria, ma la maggior parte delle modifiche genetiche coinvolte sono piccole variazioni sparse nel DNA. Questo studio si concentra su una di queste regioni del genoma e mostra, passo dopo passo, come due sottili varianti del DNA possano modificare lo sviluppo e la comunicazione delle cellule cerebrali in modi che potrebbero aumentare il rischio di sviluppare la schizofrenia. 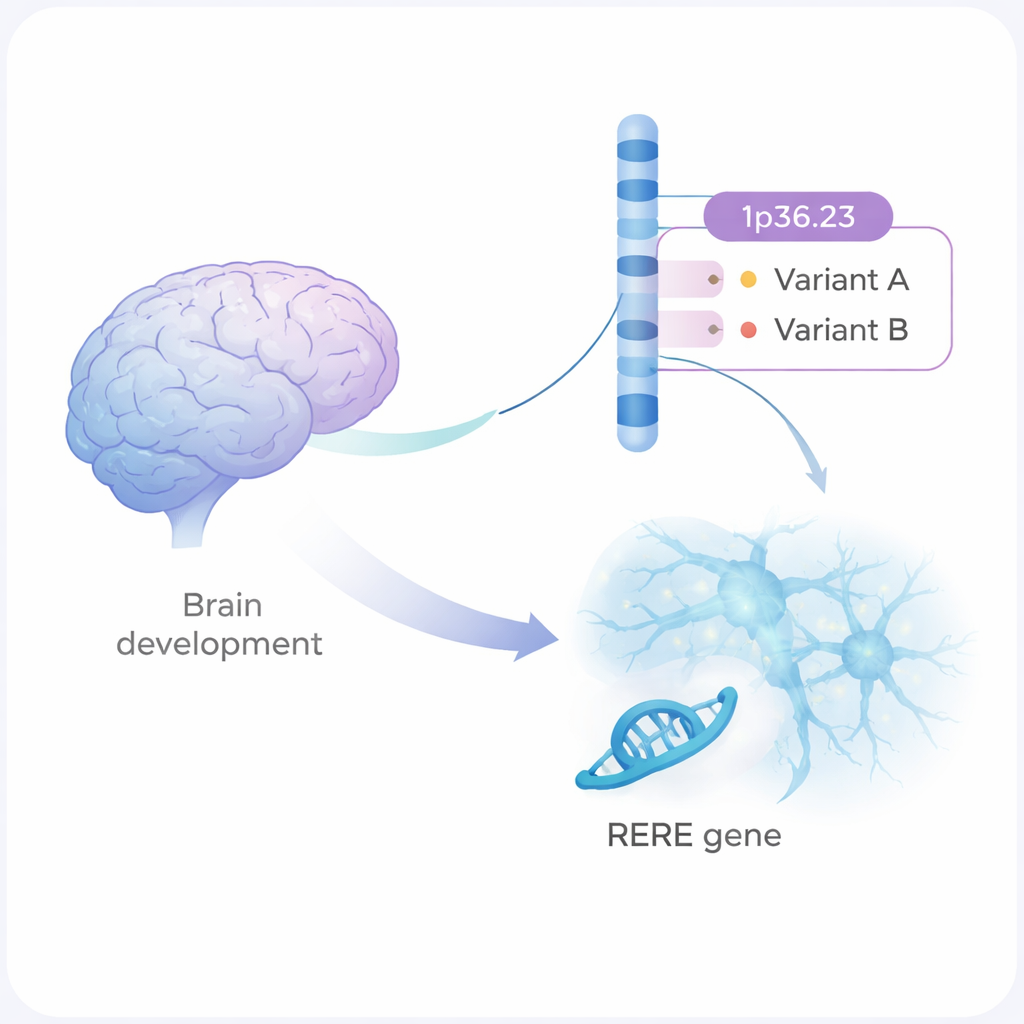
Un punto caldo genetico sul cromosoma 1
Grandi studi genetici hanno segnalato più di 300 regioni del genoma umano collegate alla schizofrenia. Una di queste è un tratto di DNA sul cromosoma 1, chiamato 1p36.23. Fino ad ora, gli scienziati non sapevano quali esatte varianti in questa regione, o quale gene, fossero responsabili. Gli autori hanno combinato genetica statistica ed esperimenti di laboratorio e hanno individuato due varianti del DNA, denominate rs159961 e rs301792, situate all’interno di un gene chiamato RERE. Queste varianti non alterano la proteina RERE in sé; si trovano invece in zone regolatorie «interruttore» all’interno del gene che controllano quanto intensamente RERE viene attivato.
Come le varianti di rischio aumentano il volume di RERE
Il gruppo ha innanzitutto verificato se queste due varianti agiscono effettivamente come interruttori funzionali. Usando saggi reporter—test in cui un frammento di DNA attiva un gene che produce luce—hanno dimostrato che le versioni associate alla schizofrenia di rs159961 e rs301792 si comportano come potenziatori (enhancer) più forti nelle cellule nervose, ma non in tipi cellulari non correlati. Test biochimici di legame hanno rivelato il perché: la forma di rischio di una variante indebolisce l’adesione di REST, una proteina che normalmente attenua l’attività genica, mentre la forma di rischio dell’altra rafforza il legame di POLR2A, un componente centrale della macchina di trascrizione. Insieme, questi spostamenti nel legame proteico aumentano l’attività dei segmenti enhancer e spingono verso l’alto l’espressione di RERE.
Dall’eccesso di RERE a un alterato sviluppo delle cellule cerebrali
Successivamente, i ricercatori hanno chiesto cosa comporti un aumento di RERE nel cervello. Hanno riscontrato che persone decedute con schizofrenia mostravano livelli più alti di RERE nel tessuto cerebrale rispetto a individui non affetti. Per modellare questo effetto, hanno innalzato artificialmente i livelli di RERE nelle cellule staminali neurali di topo—le cellule immature che danno origine a neuroni e glia. Quando RERE era sovraespresso, queste cellule staminali si dividevano meno, rimanevano bloccate in una fase tardiva del ciclo cellulare e producevano meno neuroni maturi, lasciando in gran parte inalterati altri tipi cellulari. Anche nei neuroni in coltura, un eccesso di RERE rimodellava i loro pattern di diramazione e riduceva il numero e il tipo di piccole protrusioni chiamate spine dendritiche, dove si formano le sinapsi. Questi cambiamenti sono coerenti con prove di lunga data che la schizofrenia coinvolge uno sviluppo cerebrale disturbato e perdita di spine.
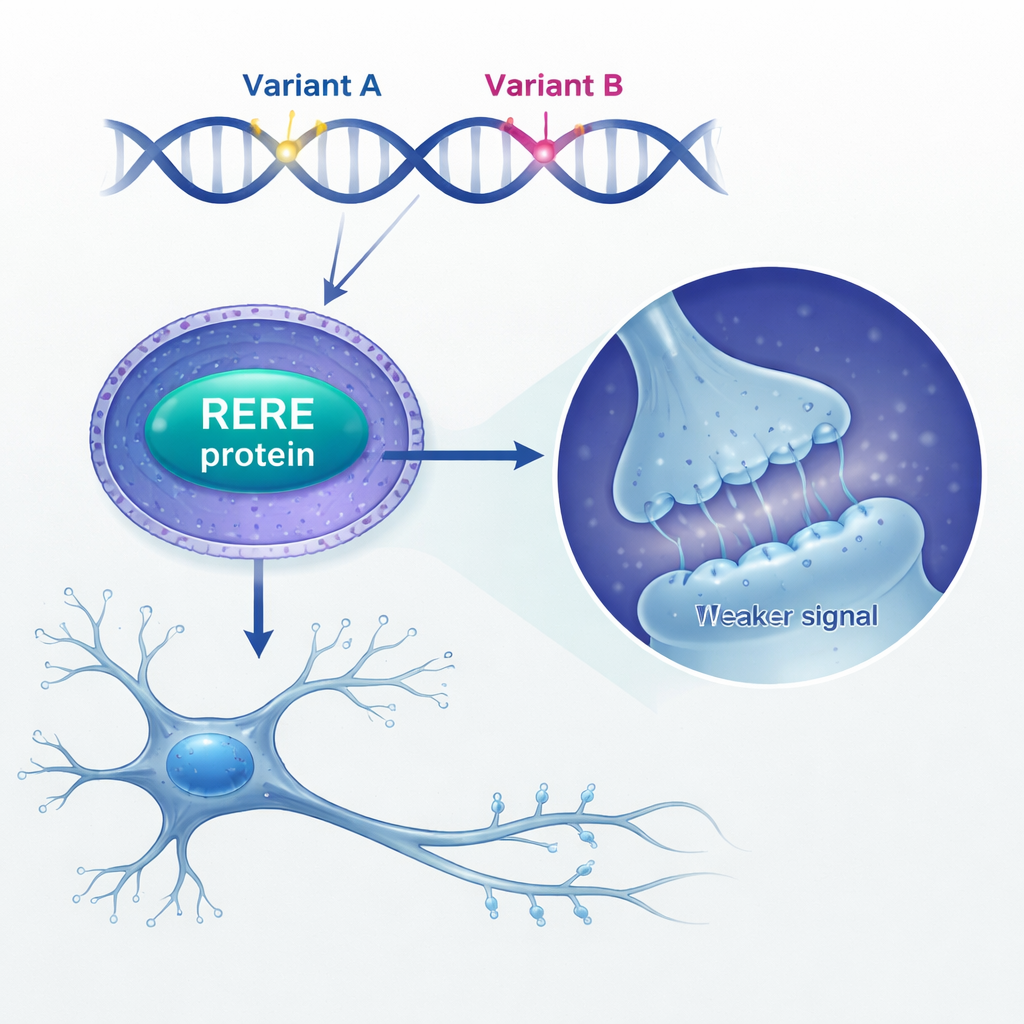
Interrompere la «conversazione» glutamatergica del cervello
Analizzando più da vicino l’attività genica, il team ha trovato che la sovraespressione di RERE disturbava reti di geni coinvolti nella crescita dei dendriti e in principali sistemi di segnalazione chimica, in particolare la via del glutammato. Un bersaglio chiave è emerso: il gene GRIN2A, che codifica una subunità cruciale (GluN2A) dei recettori glutammatergici di tipo NMDA, da tempo implicati nella schizofrenia. Gli autori hanno mostrato che RERE si associa con altre due proteine nucleari, RARB e RXRA, per legarsi direttamente al promotore di GRIN2A e attenuarne l’attività. Nei neuroni con eccesso di RERE, i livelli di GluN2A diminuivano e le registrazioni elettrofisiologiche rivelavano correnti sinaptiche mediate da recettori NMDA più deboli, anche se la frequenza degli eventi sinaptici non cambiava. In altre parole, il «volume» dei singoli segnali eccitatori veniva abbassato.
Collegare le varianti del DNA alla funzione cerebrale
Intrecciando genetica, biologia molecolare, colture cellulari ed elettrofisiologia, questo lavoro delinea una catena causale chiara: le varianti del DNA di rischio in 1p36.23 aumentano elementi regolatori all’interno del gene RERE, portando a una maggiore espressione di RERE nelle cellule cerebrali. L’eccesso di RERE a sua volta compromette la crescita e la maturazione dei neuroni, altera la forma e il numero delle spine sinaptiche e indebolisce la segnalazione a base di glutammato attraverso i recettori NMDA—in particolare quelli contenenti GluN2A. Per il lettore non specialista, il messaggio principale è che cambiamenti molto piccoli nel DNA possono spostare leggermente l’attività di un singolo gene e, su molti neuroni e nel corso di molti anni, questo può deviare lo sviluppo e la comunicazione cerebrale in modi che contribuiscono alla schizofrenia.
Citazione: Liu, Y., Wang, J., Yang, H. et al. Functional variants at 1p36.23 confer risk of schizophrenia through modulating RERE. Nat Commun 17, 1742 (2026). https://doi.org/10.1038/s41467-026-68449-6
Parole chiave: genetica della schizofrenia, gene RERE, neurosviluppo, segnalazione del glutammato, funzione sinaptica