Clear Sky Science · it
Polarizzazione del CO2 indotta da campo elettrico e blocco protone bioispirato sbloccano la riduzione del CO2 in acido forte senza cationi metallici
Trasformare un gas problematico in un ingrediente utile per i carburanti
Il diossido di carbonio (CO2) è il principale gas serra che guida il cambiamento climatico, ma è anche una potenziale materia prima per produrre carburanti e sostanze chimiche usando elettricità rinnovabile. Uno dei maggiori ostacoli è che il CO2 è molto poco reattivo, specialmente in liquidi molto acidi dove si forma invece idrogeno indesiderato. Questo studio mostra come un nanomateriale d'oro sagomato in modo intelligente, rivestito da un coating bioispirato, possa superare questi ostacoli e trasformare il CO2 in monossido di carbonio (CO) in modo efficiente in condizioni acide estreme, senza fare affidamento su sali metallici disciolti che normalmente causano intasamenti e sprechi.

Perché lavorare in acido forte conta
La maggior parte dei dispositivi che convertono elettricamente il CO2 operano in liquidi neutri o alcalini. In questi ambienti, però, il CO2 tende a reagire con il liquido formando carbonati e bicarbonati, sprecando gran parte del gas e accorciando la vita utile del dispositivo per l'accumulo di solidi. Eseguire la reazione in acido forte potrebbe evitare queste perdite e sfruttare meglio ogni molecola di CO2. Il problema è che in ambiente acido gli ioni idrogeno carichi positivamente sono ovunque e si combinano con facilità formando idrogeno, competendo con il CO2 per gli elettroni sulla superficie dell'elettrodo. Allo stesso tempo, le molecole neutre di CO2 non aderiscono facilmente alle superfici metalliche. Gli autori hanno progettato un catalizzatore e un ambiente circostante che potessero sia attrarre sia attivare il CO2, e contemporaneamente tenere i protoni a distanza, il tutto in una soluzione acida priva di cationi metallici.
Triangoli d'oro appuntiti che sovralimentano il CO2
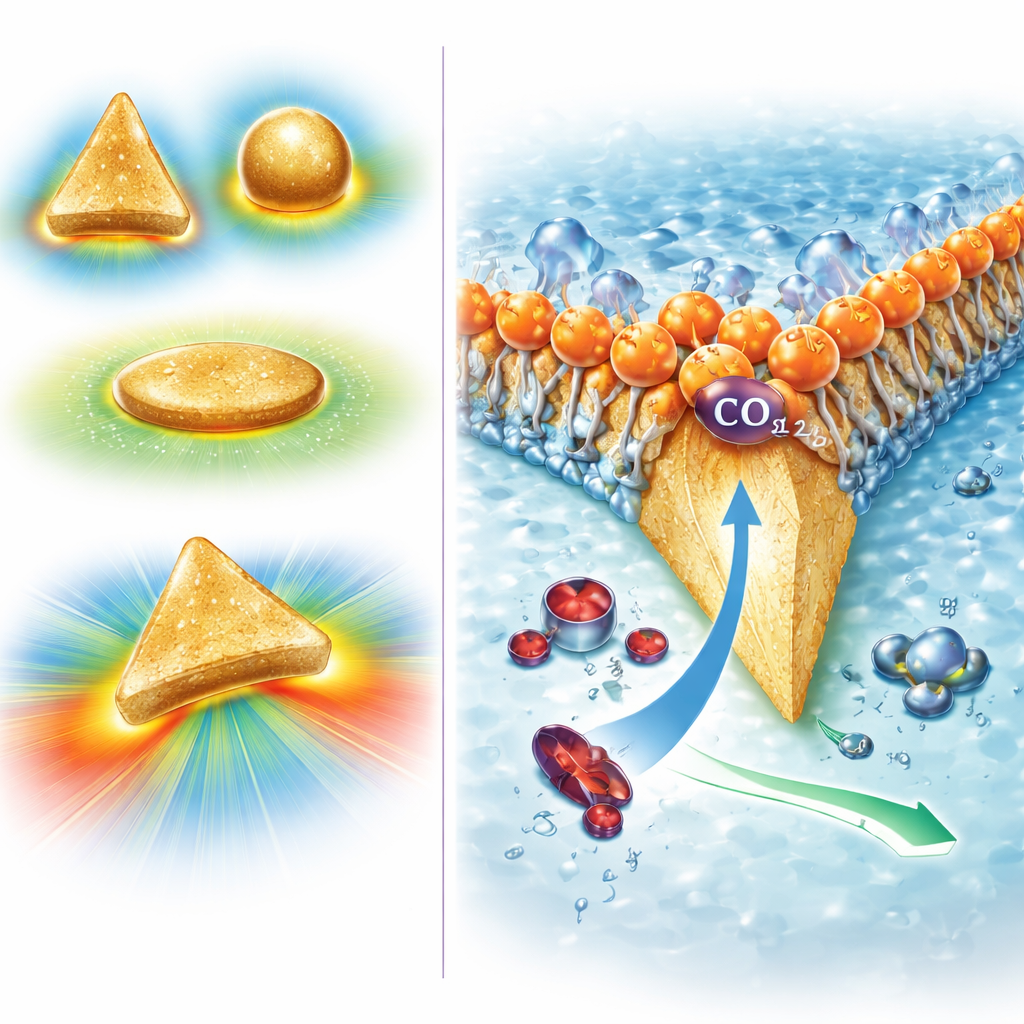
Il team ha creato piccoli triangoli d'oro piatti larghi solo circa 70 nanometri, con angoli molto acuti. Simulazioni al computer hanno mostrato che quando viene applicata una tensione, la carica elettrica si concentra su queste punte affilate, producendo campi elettrici locali estremamente intensi—circa dieci volte più forti che su particelle più arrotondate. Questi campi intensi distorcono la nuvola elettronica delle molecole di CO2 vicine, trasformandole da specie non polari e simmetriche in specie polarizzate con un dipolo misurabile. Tale distorsione allunga e piega leggermente i legami carbonio–ossigeno, rendendo le molecole più facili da legare e trasformare sulla superficie d'oro. Calcoli ed esperimenti insieme indicano che questo effetto di campo rende l'adsorbimento del CO2 praticamente spontaneo e abbassa la barriera energetica per il passo iniziale chiave della sua conversione in CO, così la reazione procede più velocemente e a costo energetico minore.
Un rivestimento bioispirato che blocca i protoni
Per risolvere il secondo problema—la formazione eccessiva di idrogeno—i ricercatori si sono ispirati alle acquaporine, proteine nelle membrane cellulari di alcuni microrganismi acidofili. Le acquaporine permettono il passaggio di molecole d'acqua neutre bloccando i protoni tramite cariche positive posizionate con precisione. Imitando questa idea, gli autori hanno rivestito i loro nanotriangoli d'oro con uno strato di un tensioattivo carico positivamente chiamato CTAC. Questo strato forma un guscio morbido e ordinato i cui gruppi testa carichi respingono i protoni in arrivo ma non ostacolano il CO2 neutro. Gli esperimenti hanno mostrato che quando questo rivestimento cationico è presente, quasi tutta la corrente elettrica va nella produzione di CO anziché di idrogeno, mentre l'oro nudo o rivestito diversamente produce molta più H2. I modelli al computer hanno confermato che lo strato carico rallenta il trasporto dei protoni, innalza il pH locale immediatamente accanto al catalizzatore e quindi sopprime la reazione collaterale.
Una prestazione che dura
Quando i triangoli appuntiti con cappuccio di CTAC sono stati testati in un elettrolizzatore a flusso a pH 1, hanno prodotto CO con quasi il 100% di selettività su un'ampia gamma di tensioni e hanno continuato a funzionare per almeno 100 ore a elevata densità di corrente. L'efficienza energetica ha raggiunto circa il 60%, valore competitivo o superiore a molti sistemi che fanno affidamento su sali metallici in ambienti meno acidi. I confronti con forme d'oro più lisce e con versioni a "punte arrotondate" dei triangoli hanno dimostrato che sia la forma bidimensionale triangolare sia, in modo cruciale, gli angoli acuti sono necessari per raggiungere queste prestazioni. Il lavoro dimostra una vera sinergia: i campi elettrici amplificati dalla geometria attirano e attivano il CO2, mentre il rivestimento carico bioispirato modella la chimica locale per tenere lontani i protoni.
Cosa significa per i dispositivi energetici puliti del futuro
Per i non specialisti, il messaggio principale è che questa ricerca offre una nuova ricetta per trasformare il CO2 in una materia prima utile in condizioni che prima sembravano sfavorevoli. Prendendo in prestito idee dalla biologia e sfruttando la fisica delle punte appuntite, gli autori mostrano che è possibile eseguire la conversione del CO2 in acido forte senza ioni metallici aggiunti, evitando l'accumulo di sali e migliorando l'utilizzo del CO2. Se scalati e integrati con energia rinnovabile, tali catalizzatori potrebbero contribuire a trasformare il CO2 da prodotto di scarto a mattonella per carburanti e chimici a impatto neutro di carbonio, rendendo nel contempo i dispositivi elettrochimici più robusti e facili da gestire.
Citazione: Chen, L., Guo, Z., Huang, HZ. et al. Electric-field-driven CO2 polarization and bioinspired proton blocking unlock CO2 reduction in strong acid without metal cations. Nat Commun 17, 1734 (2026). https://doi.org/10.1038/s41467-026-68435-y
Parole chiave: elettroreazione del CO2, elettrolizzatore acido, nanocatalizzatore d'oro, potenziamento del campo elettrico, blocco dei protoni