Clear Sky Science · it
Miglior knockout genico in vivo con alta specificità usando sgRNA Cas12a multiplex
Modificare i geni in modo più affidabile
L'editing genico promette nuovi modi per studiare la biologia, curare le malattie e persino controllare gli insetti nocivi, ma negli organismi viventi spesso funziona meno perfettamente di quanto suggeriscano i titoli. Molte cellule sfuggono all'editing o vengono alterate solo parzialmente, il che può offuscare i risultati sperimentali e limitarne l'uso pratico. Questo studio descrive un nuovo metodo basato su CRISPR nelle mosche della frutta che rende i knockout genici più completi e più precisi, offrendo un modello per un editing del genoma più affidabile in organismi complessi.
Perché il CRISPR standard spesso non basta
Gli strumenti CRISPR tradizionali come Cas9 tagliano il DNA in un punto scelto usando una singola o poche guide RNA. Negli animali viventi questo approccio affronta diversi ostacoli. Alcune guide funzionano semplicemente male; alcuni siti bersaglio sono difficili da raggiungere per l'enzima; e la macchina di riparazione cellulare spesso “sistema” la rottura con piccole modifiche che lasciano il gene ancora funzionante. Il risultato è un mosaico: cellule vicine nello stesso tessuto possono portare mutazioni differenti, o nessuna. Quella disomogeneità rende difficile capire cosa succede quando un gene è realmente spento e rappresenta una sfida per applicazioni come la terapia genica o i gene drive che devono agire efficacemente nella maggior parte delle cellule.
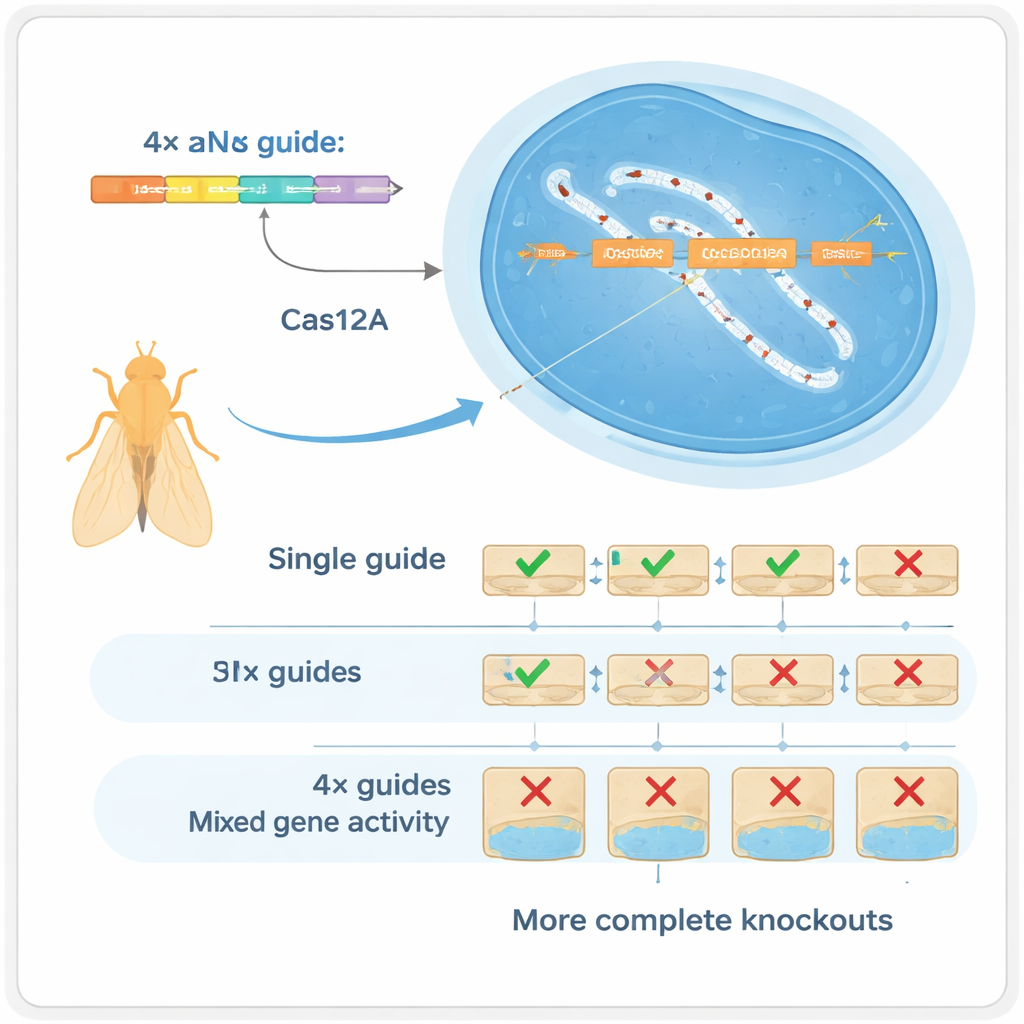
Quattro guide sono meglio di una
Gli autori si sono rivolti a un altro enzima CRISPR, Cas12a, che può processare array compatti di guide molto più facilmente rispetto a Cas9. Hanno costruito un toolkit per Drosophila in cui ogni gene è bersagliato da un insieme di quattro guide RNA, tutte codificate su un singolo piccolo frammento di DNA che può essere prodotto in massa. In test attentamente controllati hanno mostrato che usare quattro guide per gene ristruttura drasticamente i tipi di modifiche del DNA prodotti: invece di piccole inserzioni o delezioni a un singolo sito, il sistema crea frequentemente delezioni più ampie tra siti di taglio che distruggono quasi sempre la funzione genica. Questo “multiplexing” funziona in due modi: se una guida fallisce, le altre possono ancora svolgere il lavoro (ridondanza), e quando più guide tagliano contemporaneamente possono rimuovere porzioni maggiori del gene (sinergia).
Alta efficienza senza danni collaterali aggiuntivi
Creare più rotture nel DNA solleva ovvie questioni di sicurezza. Potrebbero tagli multipli in una regione cancellare accidentalmente geni vicini? Le guide potrebbero sbagliare bersaglio altrove nel genoma più frequentemente? Per rispondere a ciò, i ricercatori hanno misurato la morte cellulare, analizzato gli effetti sui geni adiacenti e ideato un saggio intelligente per visualizzare eventi di riparazione cromosomica chiamato perdita di eterozigosi su ampi tratti di DNA. Hanno scoperto che raggruppare quattro tagli all'interno di un singolo gene è ben tollerato: non aumentava la morte cellulare rispetto agli approcci convenzionali con Cas9 e raramente disturbava i geni vicini a meno che una guida non finisse estremamente vicino a un elemento regolatorio. Schermi su larga scala usando più di 2.000 guide su un terzo del genoma della mosca hanno mostrato che oltre il 99% degli array di guide era attivo sul bersaglio previsto, mentre l'attività off-target riproducibile era inferiore all'1%, indicando una specificità molto alta anche in un contesto multiplex.
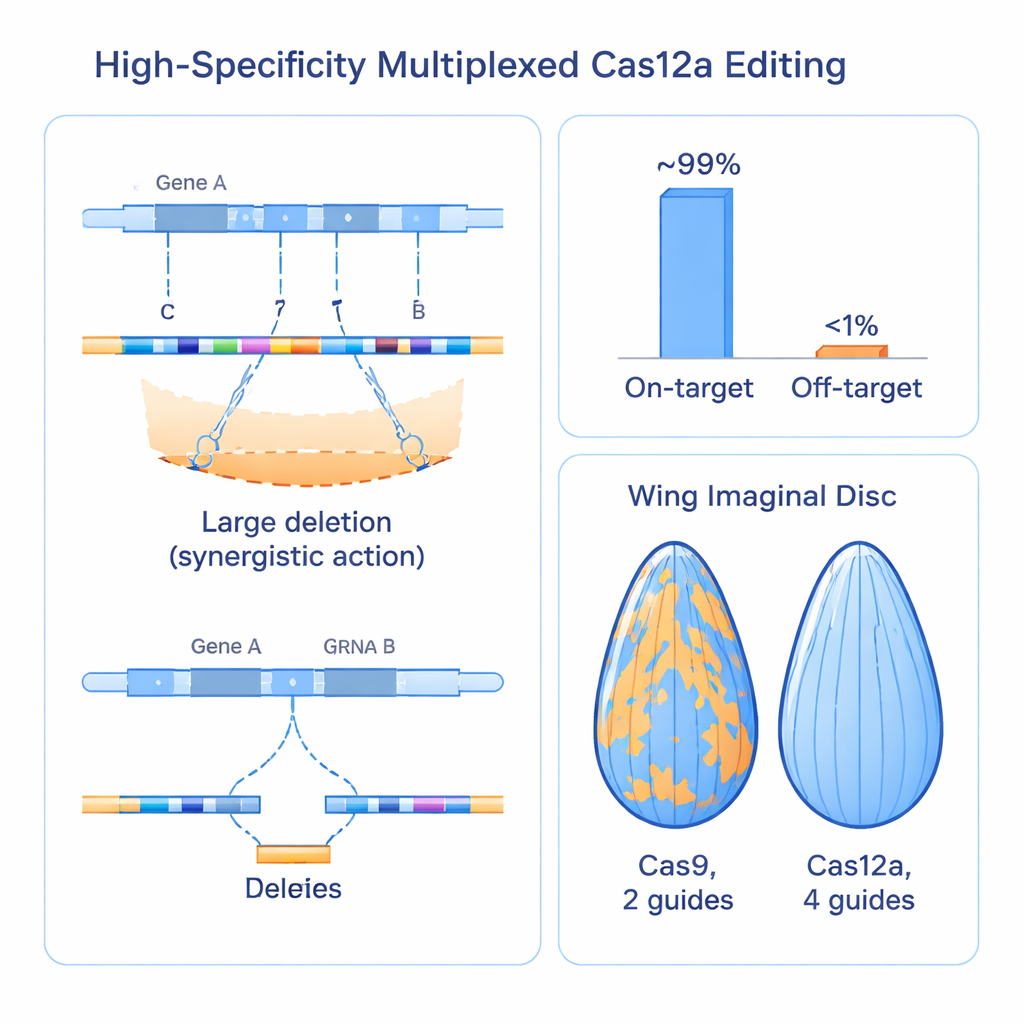
Sorpassare i sistemi Cas9 consolidati nei tessuti reali
Per valutare se questi miglioramenti molecolari si traducono in biologia più chiara, il gruppo ha confrontato il loro sistema Cas12a a quattro guide direttamente con risorse basate su Cas9 ampiamente usate, bersagliando più di 100 geni nella mosca. In tessuti come occhio, intestino e ala in sviluppo, l'approccio Cas12a ha prodotto effetti di perdita di funzione più forti e più uniformi rispetto a Cas9, che spesso lasciava evidenti chiazze di tessuto non modificato e normale. Quando hanno usato la dimensione dell'ala come misura quantitativa, il nuovo sistema ha generato costantemente difetti di crescita maggiori e più riproducibili per regolatori noti, rivelando che alcuni geni precedentemente classificati come deboli o non essenziali erano in realtà sfuggiti perché gli strumenti più vecchi non li inattivavano a sufficienza. La maggiore potenza del metodo ha persino svelato un ruolo essenziale precedentemente sconosciuto per un gene chiamato trade embargo nello sviluppo e nella sopravvivenza dell'ala.
Cosa significa per il futuro dell'editing genico
In termini semplici, questo lavoro mostra come trasformare il CRISPR da un bisturi talvolta impreciso in un interruttore più netto per spegnere i geni negli animali viventi. Combinando Cas12a con quattro guide per gene, gli autori ottengono knockout quasi completi con effetti indesiderati molto bassi, il tutto in un formato pratico da scalare su centinaia di geni. Sebbene sviluppata nelle mosche della frutta, le basi del metodo — usare più guide per ridondanza e sinergia e controllare con cura gli effetti cromosomici collaterali — sono ampiamente applicabili. Questa strategia potrebbe migliorare la ricerca di base, affinare gli screen genetici e orientare progetti più sicuri per future applicazioni mediche ed ecologiche dell'editing genico.
Citazione: Port, F., Buhmann, M.A., Zhou, J. et al. Improved in vivo gene knockout with high specificity using multiplexed Cas12a sgRNAs. Nat Commun 17, 877 (2026). https://doi.org/10.1038/s41467-026-68434-z
Parole chiave: CRISPR, Cas12a, knockout genico, Drosophila, specificità dell'editing del genoma