Clear Sky Science · it
Uso dinamico degli alleli dei geni legati all’X attenua i fenotipi delle malattie neuroevolutive negli organoidi cerebrali
Come il cromosoma X “silenzioso” aiuta a proteggere il cervello
Ogni cellula di una donna contiene due cromosomi X, ma per decenni i manuali di biologia hanno descritto uno di essi come in gran parte spento—come un libro di riserva tenuto chiuso su uno scaffale. Questo studio mostra che, soprattutto nel cervello in sviluppo, quell’X “silente” è più simile a una biblioteca di riserva dinamica. Può essere richiamato quando necessario e questa flessibilità aggiuntiva potrebbe contribuire a spiegare perché molti disturbi dello sviluppo cerebrale colpiscono più gravemente i maschi rispetto alle femmine.
Un sistema di riserva nascosto sul cromosoma X
Nelle femmine dei mammiferi, un cromosoma X in ciascuna cellula viene spento precocemente durante lo sviluppo per evitare una doppia dose di geni legati all’X. Tuttavia, gli scienziati sanno da tempo che alcuni geni possono sfuggire a questo spegnimento. Il nuovo lavoro pone una domanda più profonda: questa fuga è fissa o può cambiare durante lo sviluppo cellulare? Usando cellule staminali umane e tessuti cerebrali in miniatura detti organoidi, i ricercatori hanno tracciato quale copia di ciascun gene legato all’X—materna o paterna—veniva utilizzata mentre le cellule maturavano da staminali a neuroni. Hanno scoperto che molti geni sul cosiddetto X inattivo si accendono e si spengono in modo specifico per fase e tipo cellulare, invece di seguire una semplice regola on/off.
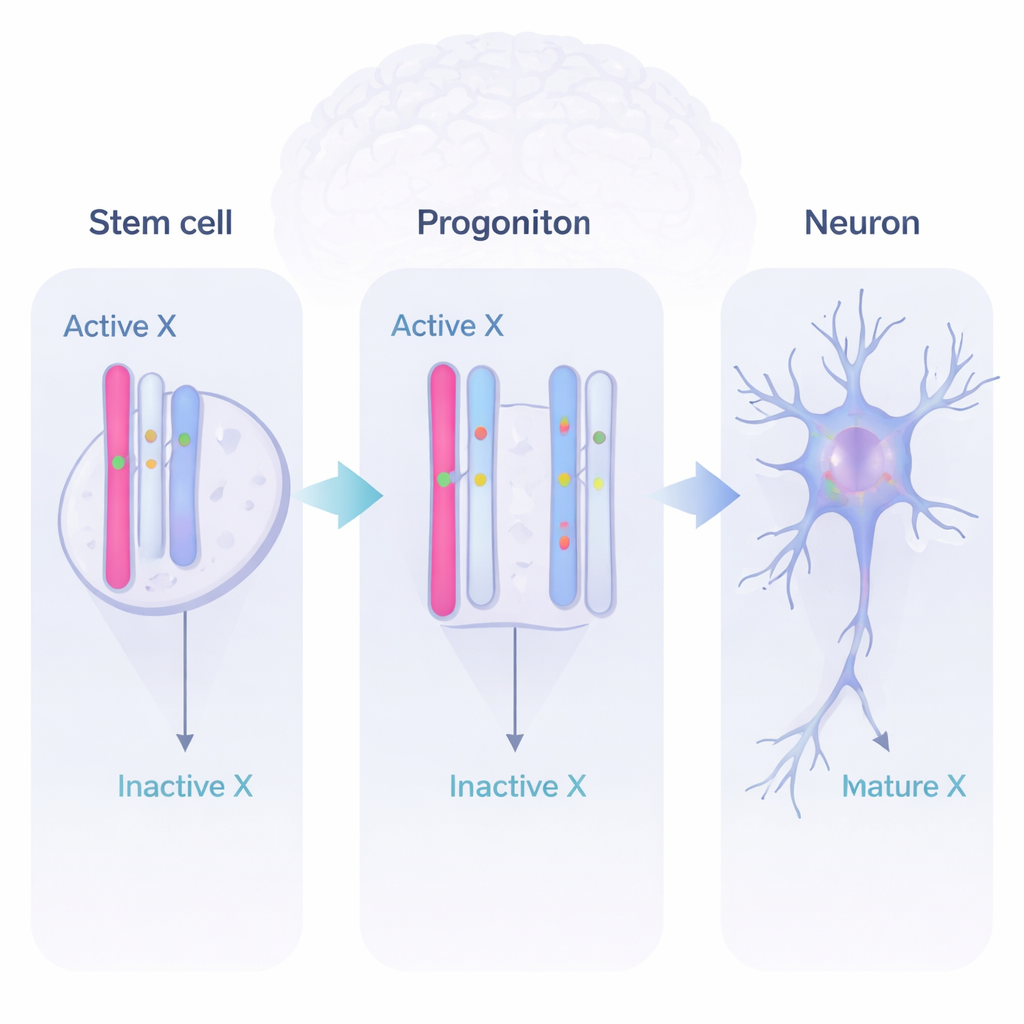
Uso dinamico dei geni durante lo sviluppo cerebrale
Leggendo l’RNA (i messaggi prodotti dai geni) e distinguendo tra le due copie parentali, il team ha identificato tre comportamenti principali. Alcuni geni restavano perlopiù spenti sull’X inattivo, come previsto. Altri erano “fuggitivi completi”, attivi da entrambe le copie dell’X in tutte le fasi. Più intrigante, un gruppo consistente di geni era dinamico. Questi geni erano silenti sull’X inattivo nelle cellule staminali, si accendevano da entrambi i cromosomi X nelle cellule progenitrici neurali e nei neuroni precoci, e poi alcuni si spegnevano di nuovo in fasi successive. Questo dimostra che l’X inattivo non è un cimitero statico di geni ma un serbatoio flessibile su cui il cervello in sviluppo può attingere quando è utile un’attività genica aggiuntiva.
Modelli conservati e legami con i disturbi cerebrali
Confrontando i dati umani con studi sul topo e con le marcature chimiche del DNA provenienti da tessuto cerebrale fetale, i ricercatori hanno rilevato che questa fuga dinamica dall’inattivazione dell’X è osservata in altri mammiferi ed è legata agli stati della cromatina—caratteristiche del confezionamento del DNA che controllano quanto facilmente i geni possono essere attivati. I geni che si riattivavano tendevano a raggrupparsi in specifiche regioni del cromosoma X e presentavano firme epigenetiche di DNA attivo specifiche del tessuto cerebrale femminile. Importante per la medicina, questi geni dinamicamente riattivati erano insolitamente ricchi di geni conosciuti per aumentare il rischio di disturbi neuroevolutivi come il ritardo intellettivo e le condizioni dello spettro autistico, suggerendo che questa flessibilità si è evoluta come meccanismo protettivo.
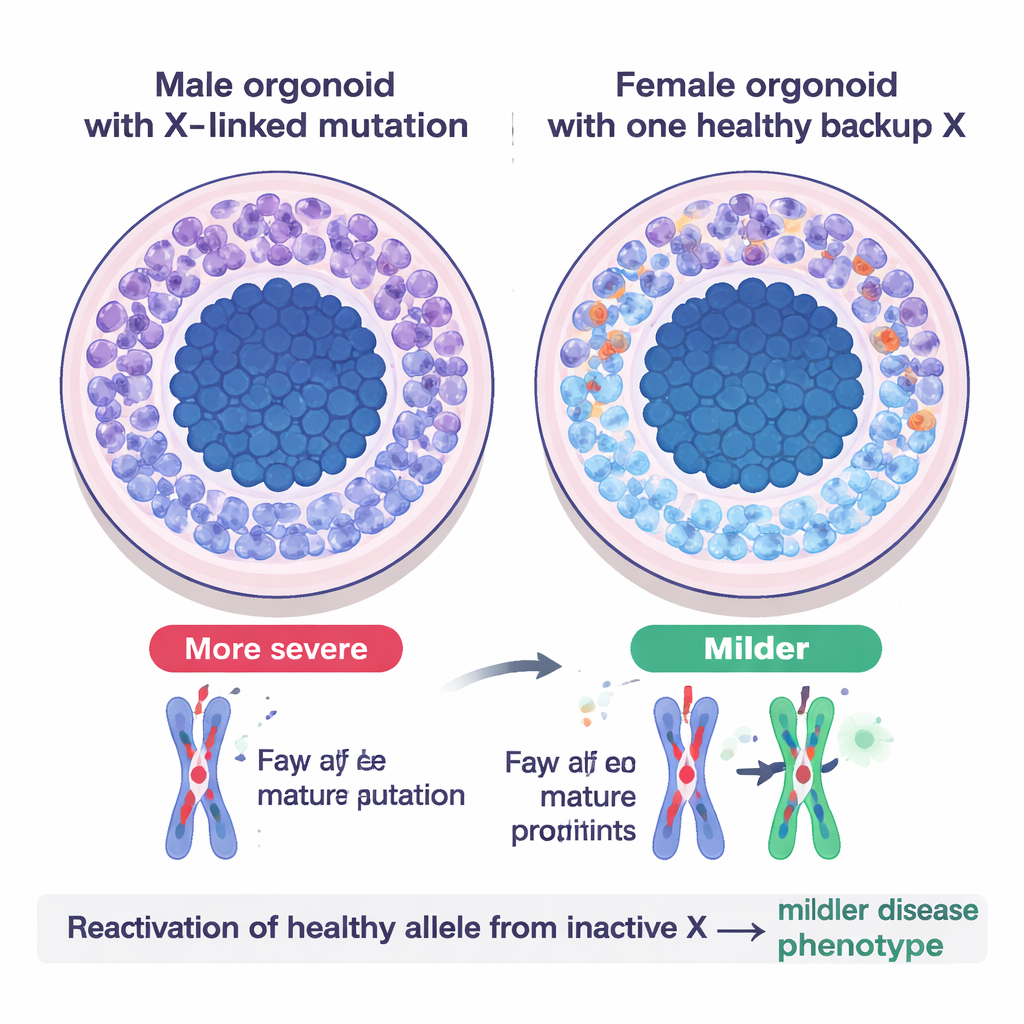
Un test nel mondo reale: la sindrome di Opitz BBB/G
Per capire come questo sistema di riserva si manifesta nella malattia, il gruppo ha modellato la sindrome di Opitz BBB/G, una rara condizione legata all’X che interessa le strutture mediane del cervello e spesso causa ritardo dello sviluppo. Il disturbo è dovuto a mutazioni dannose in un gene chiamato MID1 sul cromosoma X. Negli organoidi cerebrali coltivati da cellule di pazienti maschi—che hanno una sola copia dell’X—i neuroni erano scarsi e le cellule staminali neurali restavano a lungo in uno stato di divisione, richiamando l’ipoplasia cerebrale osservata nei pazienti. Gli organoidi femminili con la stessa mutazione sull’X attivo, ma con una copia sana sull’X inattivo, apparivano decisamente più sani: producevano più neuroni e presentavano difetti più lievi. Quando gli scienziati hanno modificato linee femminili in modo che entrambe le copie dell’X portassero la mutazione, gli organoidi hanno sviluppato problemi gravi, simili a quelli maschili, confermando che l’allele sano precedentemente inattivo si era riattivato e stava contribuendo a compensare.
Cosa significa questo per le differenze di sesso nelle malattie cerebrali
Lo studio rivela che il secondo cromosoma X “silente” nelle femmine non è mero zavorra genetica. Durante finestre critiche dello sviluppo cerebrale, geni selezionati su questo X inattivo si accendono in tipi cellulari specifici, ampliando il pool di copie geniche funzionanti. Per geni come MID1, cruciali per la costruzione del cervello, questa riattivazione dinamica può attenuare l’impatto di mutazioni dannose e produrre sintomi più lievi e più variabili nelle femmine. In altre parole, il cervello femminile possiede un sistema di riserva interno che può essere modulato nel tempo, contribuendo a spiegare perché molti disturbi neuroevolutivi legati all’X sono meno frequenti o meno severi nelle ragazze rispetto ai ragazzi.
Citazione: Bertin, M., Todorov, H., Frank, S. et al. Dynamic allele usage of X-linked genes ameliorates neurodevelopmental disease phenotypes in brain organoids. Nat Commun 17, 599 (2026). https://doi.org/10.1038/s41467-026-68428-x
Parole chiave: inattivazione del cromosoma X, organoidi cerebrali, disturbi neuroevolutivi, dosaggio genico, differenze di sesso nelle malattie