Clear Sky Science · it
Shigella flexneri elude l’immunità cellulo-autonoma mediata dai setpina tramite ADP-riboxanazione delle proteine
Come alcuni batteri intestinali sfuggono al nostro sistema di sicurezza interno
La diarrea grave causata dai batteri Shigella resta un problema importante a livello mondiale, in particolare per i bambini piccoli. Le nostre cellule non sono indifese: possiedono strumenti integrati che possono intrappolare e distruggere i microbi invasori. Questo studio rivela come Shigella flexneri, una delle principali cause di dissenteria, utilizzi astuzie molecolari per smantellare uno di questi strumenti, facilitando la diffusione del batterio da cellula a cellula nell’intestino.
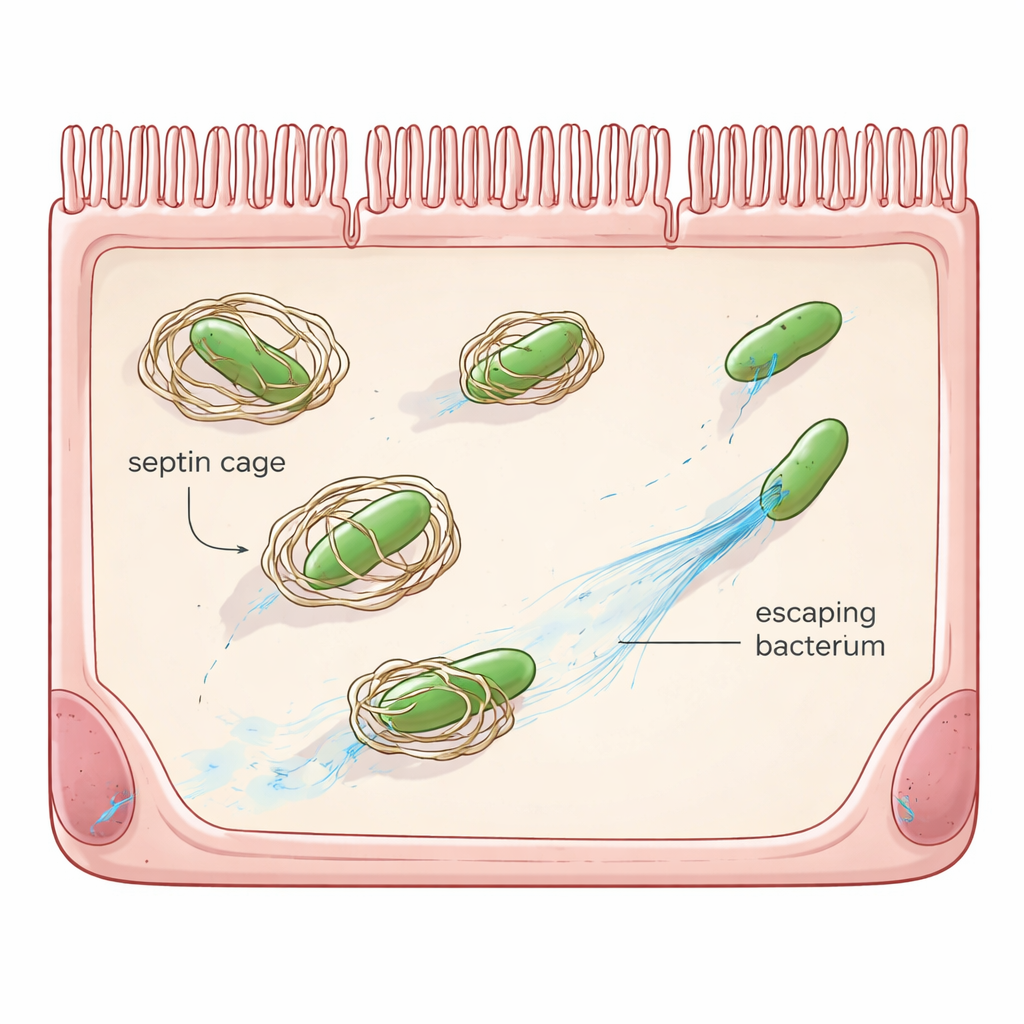
La difesa “fai-da-te” della cellula
Oltre ai globuli bianchi e agli anticorpi, molte cellule ordinarie possiedono sistemi di sicurezza d’emergenza propri, noti come immunità cellulo-autonoma. Uno di questi sistemi si basa sui setpina, una famiglia di proteine impalcatura che formano anelli e strutture a gabbia. Quando Shigella entra in una cellula e sfugge nel citoplasma gelatiniforme, i setpina possono assemblarsi attorno al batterio, bloccarne la mobilità e segnalarlo per la distruzione tramite i percorsi di riciclo cellulare. Lavori precedenti avevano mostrato che Shigella dispone già di un contromisura, una proteina chiamata OspG, che contrassegna i setpina per la degradazione. Tuttavia, anche quando OspG manca, la maggior parte dei batteri evita comunque di essere incastrata, suggerendo che Shigella possieda ulteriori espedienti.
Smaskerare un secondo sabotatore batterico
Gli autori hanno rivolto la loro attenzione a un altro gruppo di proteine di Shigella, note come famiglia OspC. Utilizzando un approccio globale di mappatura delle proteine in cellule umane, hanno cercato proteine ospiti che risultassero chimicamente modificate in presenza delle proteine OspC. Oltre a bersagli noti coinvolti nella sintesi proteica, hanno trovato che diversi setpina, in particolare uno chiamato SEPT9, venivano costantemente segnati. Test biochimici dettagliati hanno mostrato che tre proteine OspC possono direttamente attaccare un piccolo gruppo ricco di energia, derivato dalla molecola NAD, su molti siti dei setpina. Questa modifica chimica, chiamata ADP-riboxanazione, è una variante speciale e irreversibile di una modifica proteica più comune.
Spezzare l’impalcatura proteica dall’interno
Per capire come questo marcatore chimico indebolisca le difese della cellula, il team ha esaminato più da vicino SEPT9. I setpina normalmente formano catene ordinate di otto unità, che poi si allineano in filamenti e infine in gabbie complete attorno ai batteri. I ricercatori hanno scoperto che una posizione particolare in SEPT9, un amminoacido chiamato arginina 561, è il sito principale dell’ADP-riboxanazione durante l’infezione. Lavori strutturali ed esperimenti di ricostituzione con proteine purificate hanno mostrato che questo sito si trova su una superficie di contatto critica dove due unità di SEPT9 si bloccano a vicenda. Quando quell’arginina è chimicamente modificata — o sostituita con un residuo che imita la carica negativa aggiunta — le catene ottameriche si disintegrano in frammenti più piccoli e non possono più costruire filamenti stabili.
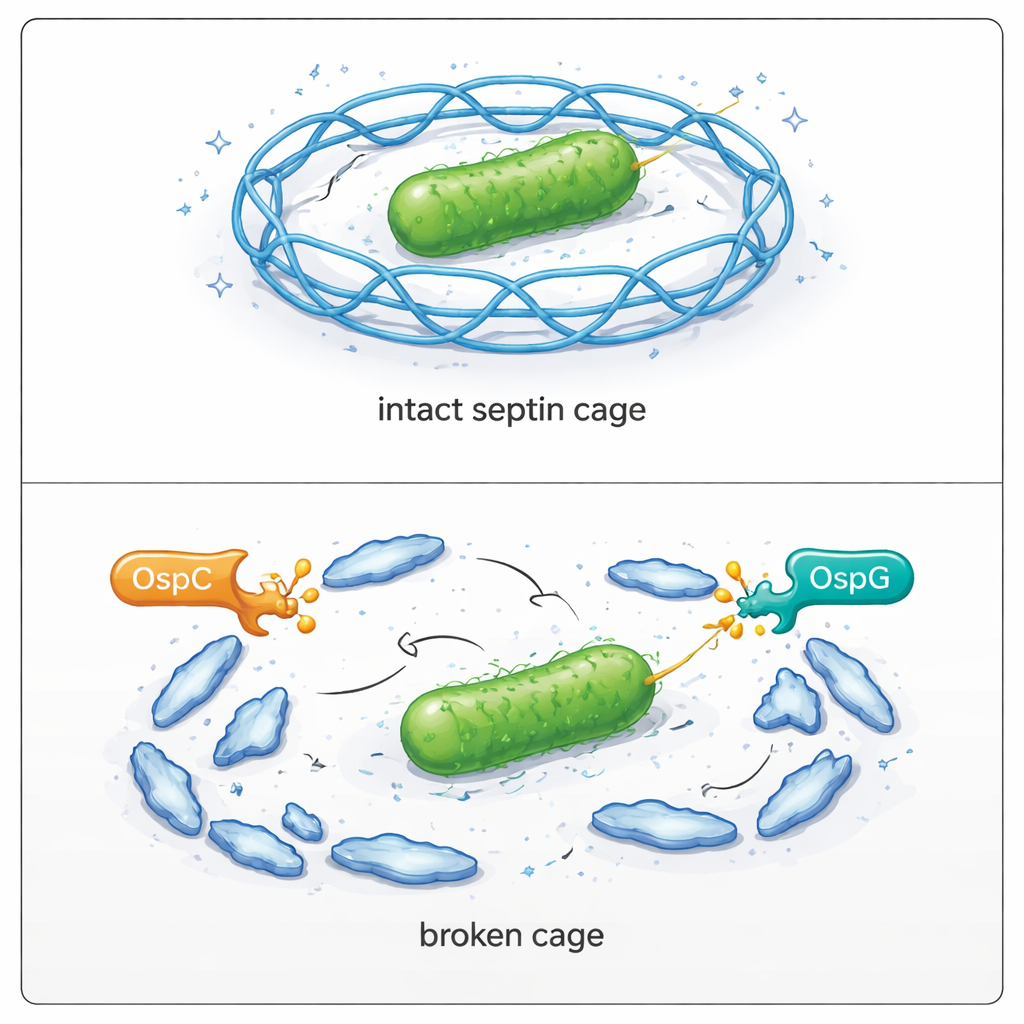
Osservare il fallimento delle gabbie nelle cellule infettate
Il team è quindi tornato nelle cellule vive per vedere le conseguenze. Nelle cellule umane infettate con Shigella normale, solo una minoranza dei batteri finiva nelle gabbie di setpina. Quando tutte le proteine OspC venivano eliminate geneticamente, la frazione di batteri incastrati raddoppiava quasi. La rimozione di OspG aveva un effetto simile, e la cancellazione contemporanea di OspC e OspG portava a un aumento ancora maggiore della formazione di gabbie e comprometteva gravemente la capacità dei batteri di diffondersi attraverso uno strato cellulare. Reintrodurre proteine OspC attive nei ceppi mutanti ripristinava la loro fuga dalle gabbie e la capacità di replicarsi e formare grosse placche. La microscopia ha confermato che quando SEPT9 non può essere modificato sull’arginina 561, si incorpora efficacemente nelle gabbie; quando invece è alterato da OspC, la formazione di gabbie attorno ai batteri cala drasticamente.
Cosa significa per la lotta contro Shigella
In termini accessibili, questo lavoro mostra che Shigella possiede una coppia corrispondente di strumenti molecolari progettati per aprire le sbarre di una “prigione” intracellulare. OspC indebolisce direttamente i mattoni proteici necessari per costruire le gabbie di setpina, mentre OspG ne favorisce lo smaltimento attraverso un’altra via chimica. Insieme, queste strategie permettono al batterio di liberarsi, muoversi all’interno delle cellule e invadere quelle vicine. Comprendere questi precisi meccanismi di fuga non solo approfondisce la nostra comprensione del funzionamento dell’immunità intrinseca cellulare, ma indica anche nuovi possibili approcci terapeutici: farmaci che bloccano OspC o proteggono i punti di contatto critici dei setpina potrebbero aiutare a ripristinare la capacità naturale della cellula di intrappolare ed eliminare questo pericoloso patogeno.
Citazione: Tang, Z., Xian, W., Özbaykal Güler, G. et al. Shigella flexneri evades septin-mediated cell-autonomous immunity via protein ADP-riboxanation. Nat Commun 17, 1727 (2026). https://doi.org/10.1038/s41467-026-68425-0
Parole chiave: Shigella, gabbie di setpine, immunità cellulo-autonoma, fattori di virulenza batterica, ADP-ribosilazione