Clear Sky Science · it
Prodotti naturali peptidici che prendono di mira ClpC1 deregOLano in modo differenziato il proteoma di Mycobacterium tuberculosis
Perché rompere le squadre di pulizia batterica è importante
La tubercolosi rimane una delle malattie infettive più letali al mondo e ceppi resistenti ai farmaci di Mycobacterium tuberculosis ne rendono il trattamento sempre più difficile. La maggior parte degli antibiotici attuali colpisce la parete cellulare del batterio o la sua capacità di produrre energia e copiare il materiale genetico. Questo studio esplora un punto debole molto diverso: il “team di pulizia” interno alla cellula che mantiene l’integrità delle proteine. Capendo come nuove molecole derivate da prodotti naturali disturbano questo sistema di manutenzione, gli scienziati sperano di progettare farmaci futuri in grado di uccidere i batteri della TB in modi nuovi e più duraturi.
Il centro di gestione delle proteine della cellula
Come tutte le cellule viventi, il batterio della TB costruisce, ripiega, ripara e ricicla continuamente le sue proteine. Un attore centrale in questa rete di “gestione” proteica è una grande macchina chiamata complesso ClpC1–ClpP1P2. Una parte (ClpC1) funge da chaperone, riconoscendo e attirando proteine danneggiate o non necessarie, mentre l’altra parte (ClpP1P2) le sminuzza per il riciclo. Questo sistema è essenziale per la sopravvivenza del batterio, soprattutto sotto stress come il calore o l’attacco di antibiotici. Diversi peptidi naturali—ecumicina, ilamycine (rufomicine) e ciclomarine—sono già noti per legarsi a ClpC1 e mostrare forte attività antibatterica contro la TB, suggerendo che questo complesso potrebbe essere un bersaglio farmacologico potente. 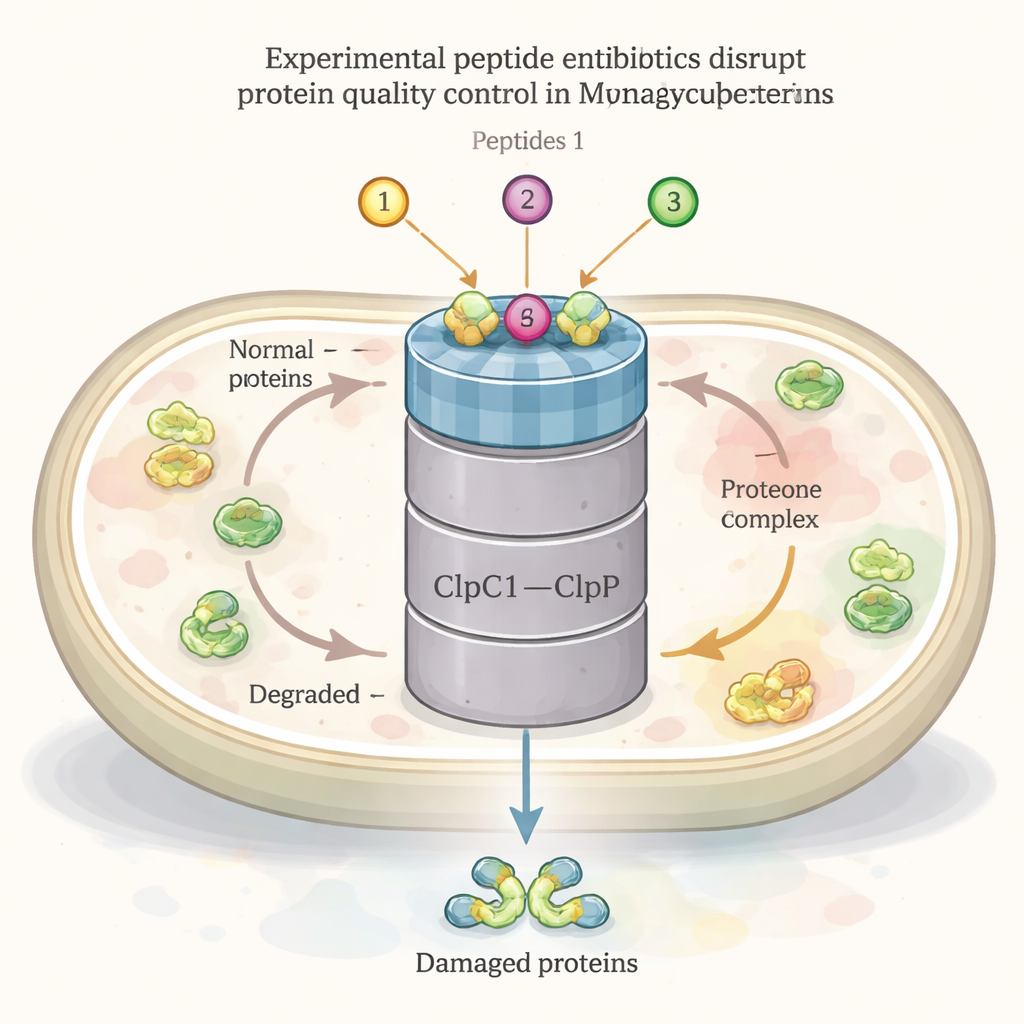
Tre farmaci correlati, tre impatti diversi
I ricercatori hanno esaminato un rappresentante di ciascuna delle tre famiglie peptidiche: un analogo di ecumicina (Ecu*), ilamycin E (IlaE) e un derivato della ciclomarina (desossiciclomarina, dCym). Sebbene tutti e tre si leghino alla stessa regione di ClpC1, non si comportano allo stesso modo all’interno della cellula. Utilizzando la proteomica quantitativa—un approccio che misura migliaia di proteine contemporaneamente—hanno scoperto che Ecu* ha provocato la perturbazione più ampia, alterando significativamente i livelli di quasi il 17% di tutte le proteine batteriche. IlaE ha modificato circa il 12% e dCym circa il 7%. Solo 72 proteine sono state costantemente influenzate da tutti e tre i composti, e la maggior parte di queste è diminuita in abbondanza. Ciò dimostra che ogni molecola spinge la macchina ClpC1 in direzioni diverse, rimodellando il panorama proteico della cellula in modi distinti anziché semplicemente “spegnere la macchina”.
Otturare il trituratore versus tagliare la corrente
Per contestualizzare questi effetti, il team ha confrontato i peptidi con il bortezomib, un farmaco oncologico che blocca in modo ampio gli enzimi deputati alla degradazione delle proteine. Nei batteri della TB, il bortezomib ha causato un accumulo generale di molte proteine, come ci si aspetta quando i trituratori sono disattivati. Al contrario, i peptidi hanno prodotto schemi più selettivi: alcuni noti bersagli di ClpC1 si sono accumulati, altri sono stati depleti, e non si è osservata un’inibizione globale di tutta la degradazione proteica. Test di laboratorio dettagliati con componenti purificati hanno mostrato che ogni peptide ha alterato il modo in cui specifici substrati venivano gestiti. Per esempio, tutti e tre interferivano con la distruzione di una proteina regolatoria (PanD), ma solo Ecu* bloccava la degradazione di una proteina modello disordinata, e solo dCym comprometteva la degradazione della proteina protettiva da stress Hsp20. Queste differenze suggeriscono che la forma complessiva e la flessibilità di ciascuna proteina bersaglio influenzano come essa viene colpita quando ClpC1 è “malaccordato” da un determinato composto. 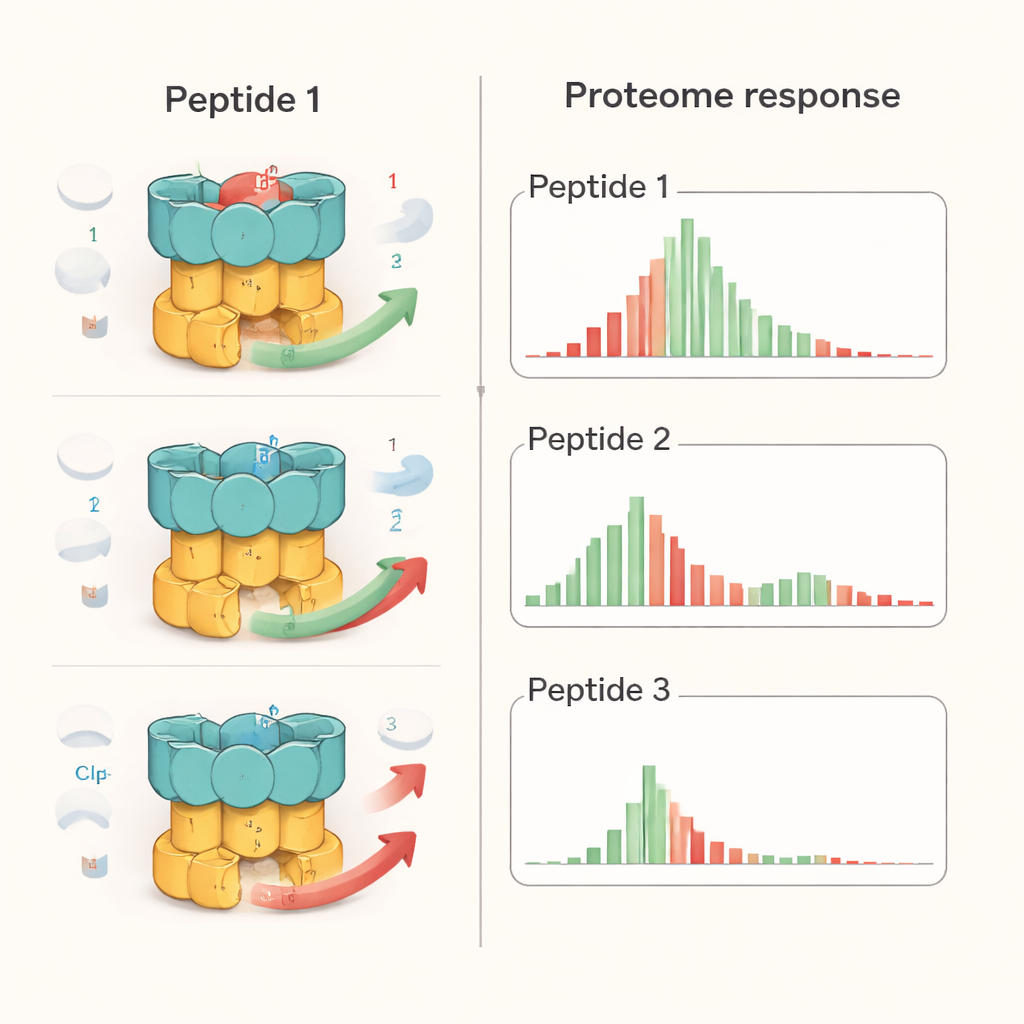
Risposte allo stress e auto-salvataggio batterico
Il batterio della TB dispone di sistemi di riserva per far fronte quando il danno proteico sovraccarica la macchina di pulizia principale. Uno di questi sistemi coinvolge un altro chaperone, ClpC2, che può legare molecole simili alla ciclomarina e ridurne l’impatto su ClpC1. Questo studio ha rilevato che sebbene tutti e tre i peptidi possano legare ClpC2 in provetta, solo il derivato della ciclomarina (dCym) ha effettivamente indotto livelli più elevati di ClpC2 nei batteri vivi e ha mostrato maggiore potenza quando ClpC2 è stato sperimentalmente ridotto. Al contrario, Ecu* e IlaE sono rimasti efficaci anche quando ClpC2 è stato abbassato, suggerendo che in gran parte aggirano questa via di auto-salvataggio. Il team ha anche scoperto un collegamento forte e specifico per composto con Hsp20, una piccola proteina che aiuta a prevenire aggregazioni dannose: Ecu* (e in misura minore IlaE) ha causato aumenti drammatici dei livelli di Hsp20 ed Ecu* si è legato direttamente a Hsp20, rivelando una nuova connessione tra questi candidati farmacologici e la rete di risposta allo stress della cellula.
Trasformare lo stress in un vantaggio terapeutico
Poiché il sistema ClpC1 è particolarmente importante in condizioni avverse, i ricercatori hanno testato i farmaci mentre i batteri erano sottoposti a un lieve stress termico, che aumenta il carico di proteine mal ripiegate. In queste condizioni, sia Ecu* sia dCym sono diventati molto più letali, raggiungendo una tossicità simile a quella del bortezomib, nonostante agiscano in modo più selettivo. Questo dimostra che mirare con attenzione la macchina del controllo qualità delle proteine può essere efficace quanto disattivare tutti i principali proteasi, ma con un controllo potenzialmente più preciso. Il lavoro ha anche mostrato che molte delle modifiche indotte da Ecu* nei livelli proteici non rispecchiavano semplicemente cambiamenti nell’attività genica, sottolineando che la perturbazione di ClpC1 altera soprattutto la regolazione post-traduzionale delle proteine.
Cosa significa per i futuri trattamenti della TB
Per i non specialisti, il messaggio chiave è che i batteri della TB dipendono da un sistema interno di pulizia e risposta allo stress finemente bilanciato per sopravvivere. I tre peptidi derivati da prodotti naturali testati qui attaccano tutti la stessa macchina centrale ma la spingono in modalità diverse, portando a distorsioni diverse e molto specifiche del paesaggio proteico del batterio. Importante, i composti simili all’ecumicina e all’ilamycin evitano un meccanismo di salvataggio batterico integrato che può attenuare l’effetto della ciclomarina, eppure debilitano comunque il patogeno sotto stress. Queste proprietà li rendono impalcature promettenti per futuri farmaci anti-tubercolosi, compresi molecole progettate che potrebbero costringere le cellule di TB a distruggere selettivamente le proprie proteine vitali o che potrebbero essere incorporate in “chimeri che mirano le proteine” per dirigere con precisione l’autodigestione batterica.
Citazione: Barter, I.K., Bedding, M.J., Leodolter, J. et al. ClpC1-targeting peptide natural products differentially dysregulate the proteome of Mycobacterium tuberculosis. Nat Commun 17, 1725 (2026). https://doi.org/10.1038/s41467-026-68423-2
Parole chiave: tubercolosi, controllo della qualità delle proteine, ClpC1, resistenza agli antibiotici, antibiotici da prodotti naturali