Clear Sky Science · it
Profilazione epigenomica simultanea e misurazione dell’attività regolatoria mediante e2MPRA
Leggere gli interruttori nascosti della cellula
Ogni cellula del corpo contiene essenzialmente lo stesso DNA, eppure una cellula cerebrale e una epatica si comportano in modo molto diverso. Il segreto risiede in brevi tratti di DNA che funzionano come dimmer per i geni, aumentandone, diminuendone o spegnendone l’espressione. Questo studio presenta un nuovo strumento potente, chiamato e2MPRA, che permette agli scienziati di testare migliaia di questi interruttori contemporaneamente osservando al contempo come il DNA è impacchettato e marcato all’interno della cellula—passi fondamentali per comprendere lo sviluppo, il rischio di malattie e perché alcune varianti genetiche sono importanti mentre altre no.
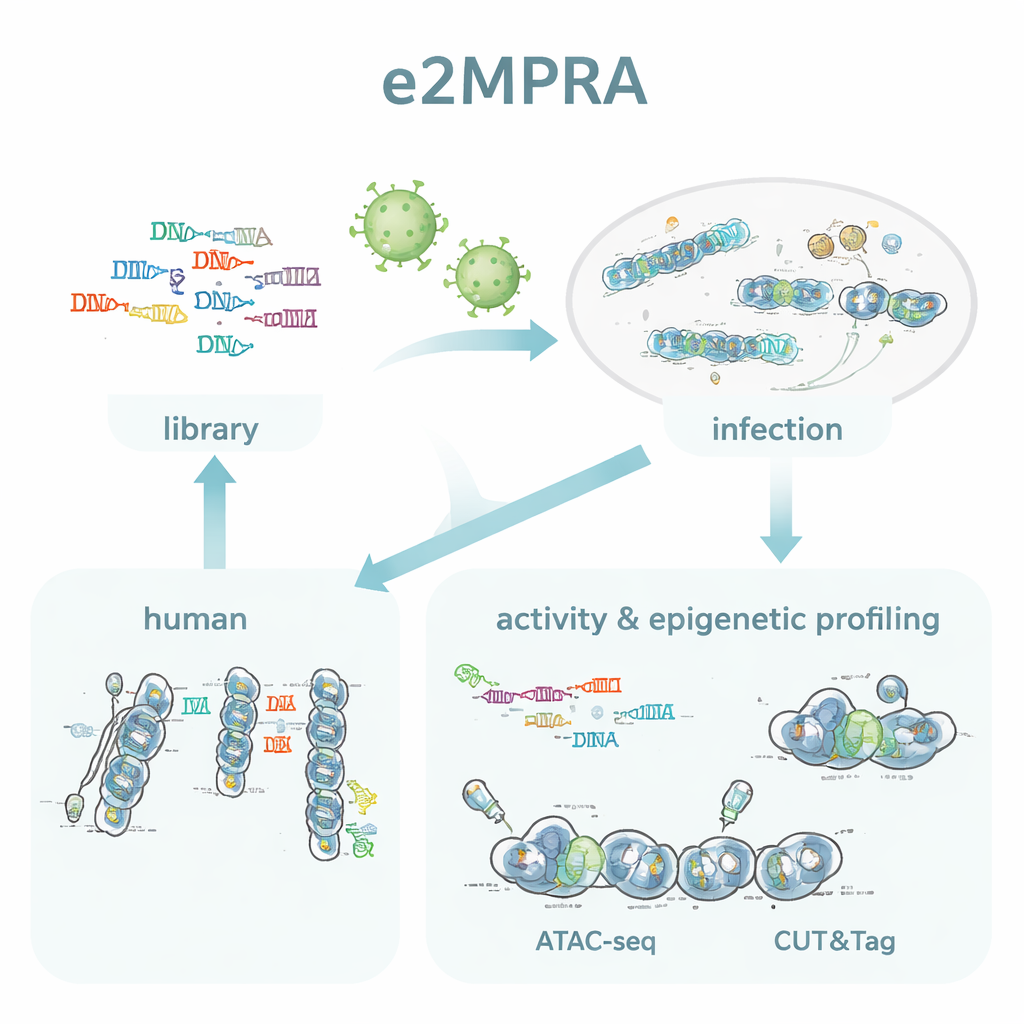
Dalle mappe del DNA alla funzione del DNA
Nell’ultimo decennio i ricercatori hanno disegnato vaste mappe di interruttori regolatori “candidati”, noti come elementi cis-regolatori. Utilizzano metodi che mostrano dove il DNA è sciolto (cromatina aperta), quali proteine vi sono legate e quali marche istoniche decorano il DNA circostante. Queste mappe sono impressionanti, ma perlopiù descrittive: il fatto che una proteina si leghi o che una marca compaia non dimostra che una sequenza controlli davvero l’attività genica. I tradizionali saggi reporter massivamente paralleli (MPRA) possono verificare se migliaia di frammenti di DNA aumentano o sopprimono l’espressione di un gene reporter, ma non ci dicono quali proteine si legano lì né quali cambiamenti epigenetici accompagnano quell’attività.
Un saggio due-in-uno per attività e marche epigenetiche
Gli autori hanno creato e2MPRA combinando un MPRA lentivirale con due tecniche epigenomiche, ATAC-seq e CUT&Tag. Innanzitutto costruiscono una libreria di DNA in cui ogni sequenza regolatoria candidata è collegata a un breve codice a barre e posta accanto a un promotore minimale e a un gene reporter. Questa libreria viene quindi confezionata in lentivirus e integrata ripetutamente nei genomi di cellule umane coltivate. Dallo stesso pool di cellule leggono i codici a barre nell’RNA per misurare l’attività regolatoria e utilizzano ATAC-seq e CUT&Tag per misurare rispettivamente l’apertura della cromatina e una marcatura istonica chiave (H3K27ac) specificamente sulle sequenze inserite. Normalizzando questi segnali rispetto alla frequenza di integrazione di ciascuna sequenza, ottengono misurazioni affiancate della “forza on/off” e dello stato epigenetico per migliaia di elementi in un unico esperimento.
Decodificare come i motivi dei fattori di trascrizione lavorano insieme
Per mostrare cosa può rivelare questa tecnologia, il team ha costruito enhancer sintetici a partire da motivi noti dei fattori di trascrizione impiegati nelle cellule del fegato. Hanno disposto questi motivi in numeri e ordini diversi su matrici di DNA neutre. Alcuni fattori, come HNF1A e XBP1, si sono comportati da attivatori classici: aggiungere copie aumentava l’espressione del reporter. Altri, come HNF1A e ONECUT1, hanno principalmente aumentato l’accessibilità della cromatina, coerenti con il loro ruolo di fattori “pionieri” che aprono il DNA compattato. PPARA ha mostrato un comportamento diverso, alterando fortemente cromatina e marche istoniche ma non la trascrizione da solo, pur cooperando con altri fattori per innalzare l’attività genica. REST, noto repressore, ha attenuato l’attività quando era posizionato accanto ad attivatori. È notevole che il semplice riorientare quattro motivi potesse modificare sostanzialmente la forza dell’enhancer, e gli attivatori tendevano a funzionare meglio se più vicini al promotore, rivelando una sorta di struttura grammaticale nell’organizzazione di questi motivi.
Individuare basi sensibili negli enhancer di pluripotenza
I ricercatori si sono poi concentrati su enhancer importanti per l’identità delle cellule staminali, focalizzandosi su regioni legate dai fattori di pluripotenza POU5F1 (detto anche OCT4) e SOX2. Hanno creato librerie di mutazioni dense in cui ogni base di enhancer di 100 paia di basi veniva sistematicamente alterata, insieme a finestre casuali di sei basi frammentate. Usando e2MPRA in cellule iPS, hanno potuto vedere quali mutazioni indebolivano o rafforzavano l’attività del reporter e come influenzavano l’apertura della cromatina e l’acetilazione. La distruzione del motivo di legame POU5F1::SOX2 spesso riduceva sia l’attività genica sia le marche epigenetiche, confermandone il ruolo centrale. In un enhancer ben studiato vicino al gene POU5F1, hanno anche scoperto che modificare un motivo YY1 aumentava la trascrizione ma riduceva l’apertura della cromatina, suggerendo che alcuni fattori possono promuovere uno stato aperto pur limitando l’espressione.
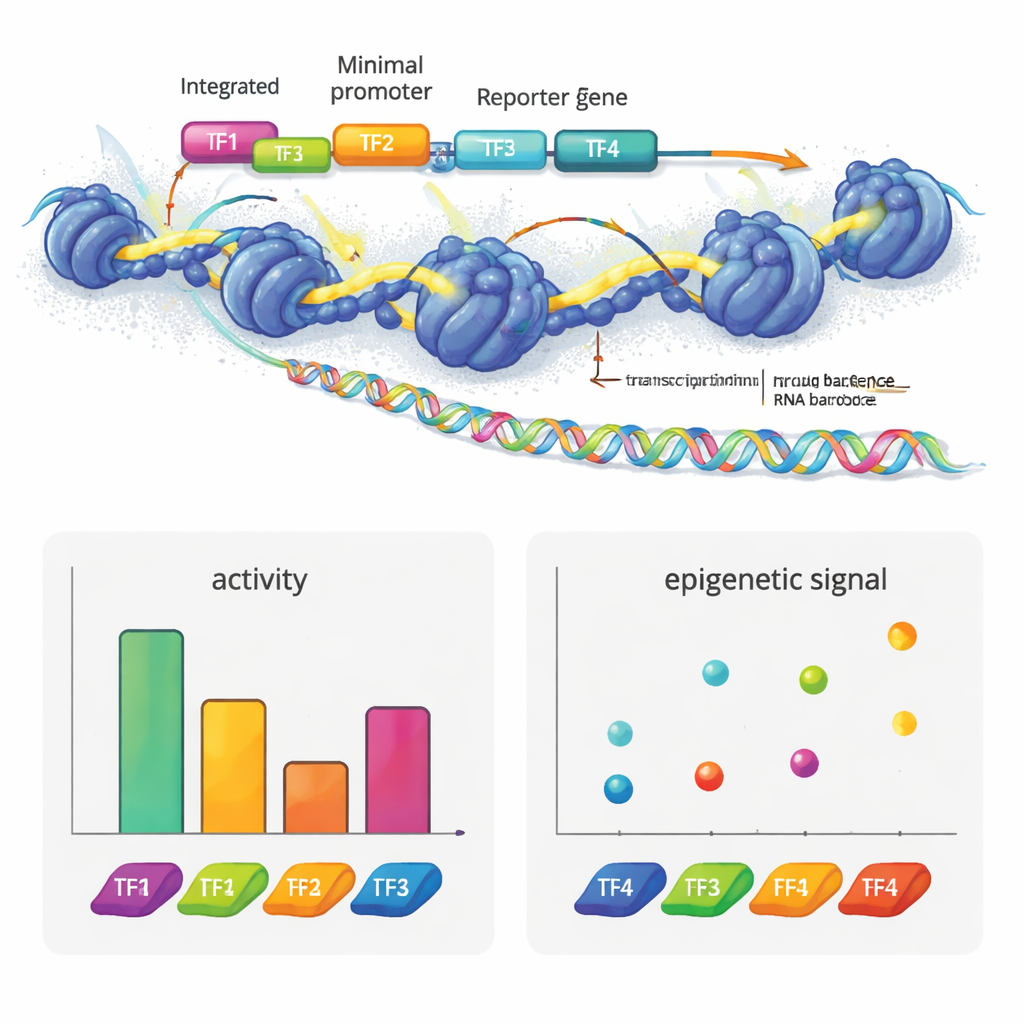
Cosa significa per i geni e per le malattie
e2MPRA non riproduce perfettamente tutte le sfumature del naturale wiring 3D del genoma, ma offre un modo pratico per confrontare migliaia di sequenze regolatorie e varianti nelle stesse condizioni. Accoppiando una lettura funzionale (quanto intensamente un segmento di DNA guida un gene) con letture epigenetiche (come quel DNA è impacchettato e marcato), questo metodo aiuta a spiegare perché certi motivi dei fattori di trascrizione, combinazioni e posizioni siano così cruciali. A lungo termine, strumenti come e2MPRA possono facilitare l’interpretazione delle varianti genetiche non codificanti associate a malattie, progettare enhancer sintetici per terapie geniche e costruire un “codice regolatorio” più completo che colleghi la sequenza del DNA al comportamento cellulare.
Citazione: Zhang, Z., Georgakopoulos-Soares, I., Bourque, G. et al. Simultaneous epigenomic profiling and regulatory activity measurement using e2MPRA. Nat Commun 17, 1724 (2026). https://doi.org/10.1038/s41467-026-68422-3
Parole chiave: regolazione genica, enhancer, epigenetica, fattori di trascrizione, genomica funzionale