Clear Sky Science · it
I ligasi E3 dell’ubiquitina guardiani prendono di mira le deaminasi APOBEC3 associate al cancro per la degradazione per promuovere l’integrità del genoma umano
Proteggere il nostro DNA dal fuoco amico
Le nostre cellule impiegano enzimi potenti per danneggiare il DNA virale, aiutandoci a difenderci dalle infezioni. Ma alcuni di questi stessi enzimi, se lasciati senza controllo, possono per errore segnare il nostro genoma e contribuire al cancro. Questo studio svela come le cellule umane controllano questi enzimi rischiosi, rivelando un sistema di “controllo qualità” incorporato che marca per la distruzione le versioni pericolose prima che possano riscrivere il nostro DNA.
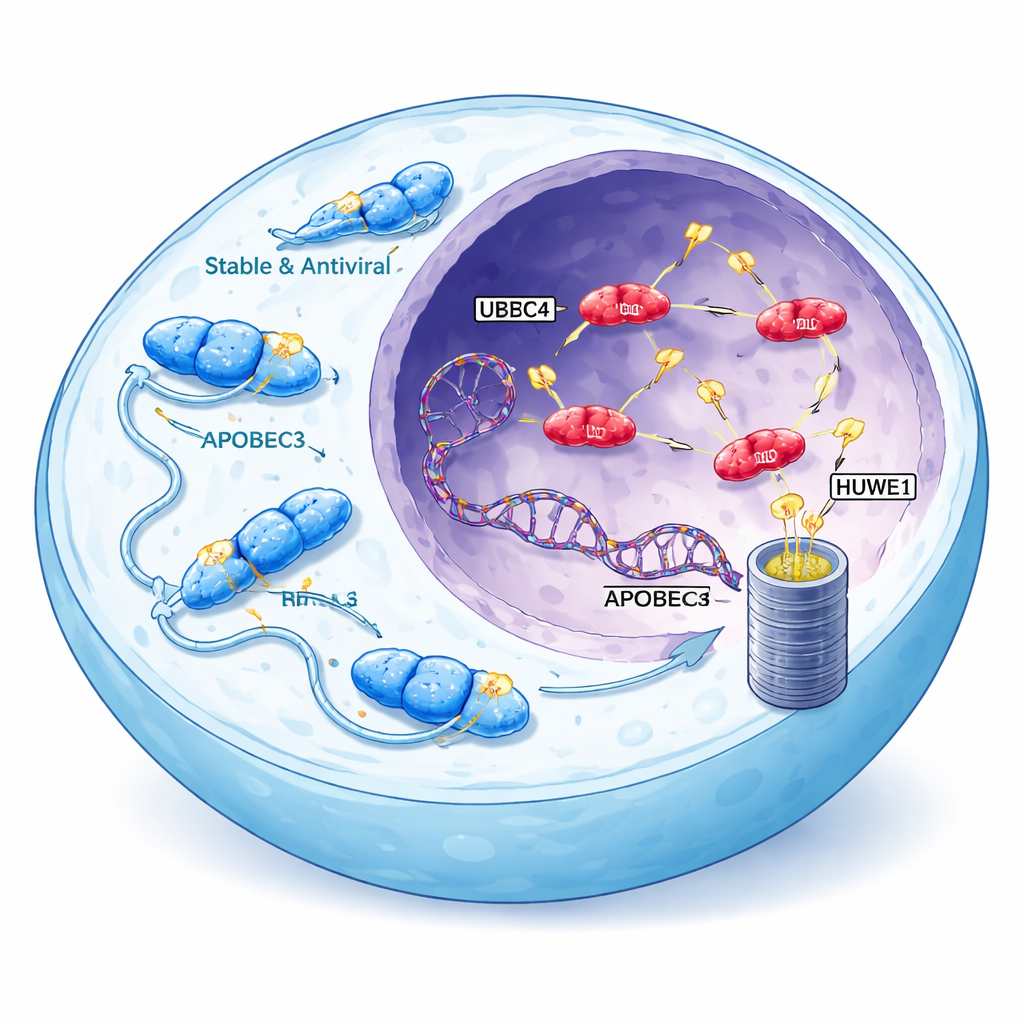
Combattenti virali che possono rivoltarsi contro di noi
La famiglia di enzimi APOBEC3 normalmente aiuta a difendersi da virus come l’HIV alterando chimicamente il DNA virale e causando errori fatali. Gli esseri umani posseggono sette varianti di APOBEC3, e tre di esse—A3A, A3B e una forma di A3H chiamata aplotipo I (A3H-I)—sono fortemente associate ai modelli di mutazione osservati in molti tumori. Questi enzimi particolari possono spostarsi nel nucleo cellulare, dove risiedono i nostri cromosomi, e introdurre ammassi caratteristici di mutazioni nel genoma. Le firme legate a APOBEC compaiono in oltre la metà dei tumori umani, soprattutto nei tumori al seno, polmone e vescica, dove ampliano il repertorio di cambiamenti genetici di cui i tumori possono servirsi per adattarsi e resistere alle terapie.
Perché le forme più pericolose sono stranamente instabili
Curiosamente, gli enzimi APOBEC3 più fortemente legati al cancro sono anche i meno stabili. A differenza delle loro controparti citosoliche, che si accumulano a livelli elevati e bloccano efficacemente i virus, A3A, A3B e A3H-I vengono degradati rapidamente e sono solitamente presenti a basse concentrazioni nel nucleo. I ricercatori hanno ipotizzato che questa instabilità possa essere intenzionale: se le cellule limitano attivamente i livelli di APOBEC3 nucleari, qualsiasi rottura di questo controllo potrebbe scatenare ondate di mutagenesi. Usando A3H-I come modello, hanno dimostrato che gli APOBEC3 associati al cancro vengono distrutti principalmente dal proteasoma, il trituratore proteico della cellula, dopo essere stati marcati con piccoli “segnali” molecolari chiamati ubiquitina su più siti amminoacidici.
Alla ricerca dei guardiani cellulari
Per identificare la macchina responsabile della marcatura di A3H-I e A3B, il gruppo ha combinato screening CRISPR con mappature di prossimità proteica. Hanno ingegnerizzato cellule che si illuminano differentemente a seconda della stabilità di A3H-I e della sua variante innocua A3H-II, quindi hanno disattivato sistematicamente geni coinvolti nella degradazione proteica. Tre ligasi dell’ubiquitina—UBR4, UBR5 e HUWE1—sono emerse come rilevanti. L’eliminazione di ciascuna di queste ligasi aumentava selettivamente i livelli dell’instabile A3H-I nucleare senza influire sulla stabile A3H-II citosolica. Le stesse ligasi aumentavano in modo indipendente i livelli di A3B endogeno in linee cellulari coloniche e immunitarie, e la cancellazione simultanea di tutte e tre produceva un aumento additivo dell’abbondanza di A3B. Esperimenti biochimici hanno inoltre mostrato che UBR5 e HUWE1 si legano fisicamente ad A3B e A3H-I e attaccano direttamente catene di ubiquitina, mentre UBR4 sembra specializzarsi nell’estendere queste catene per rendere le proteine più facilmente smaltibili.
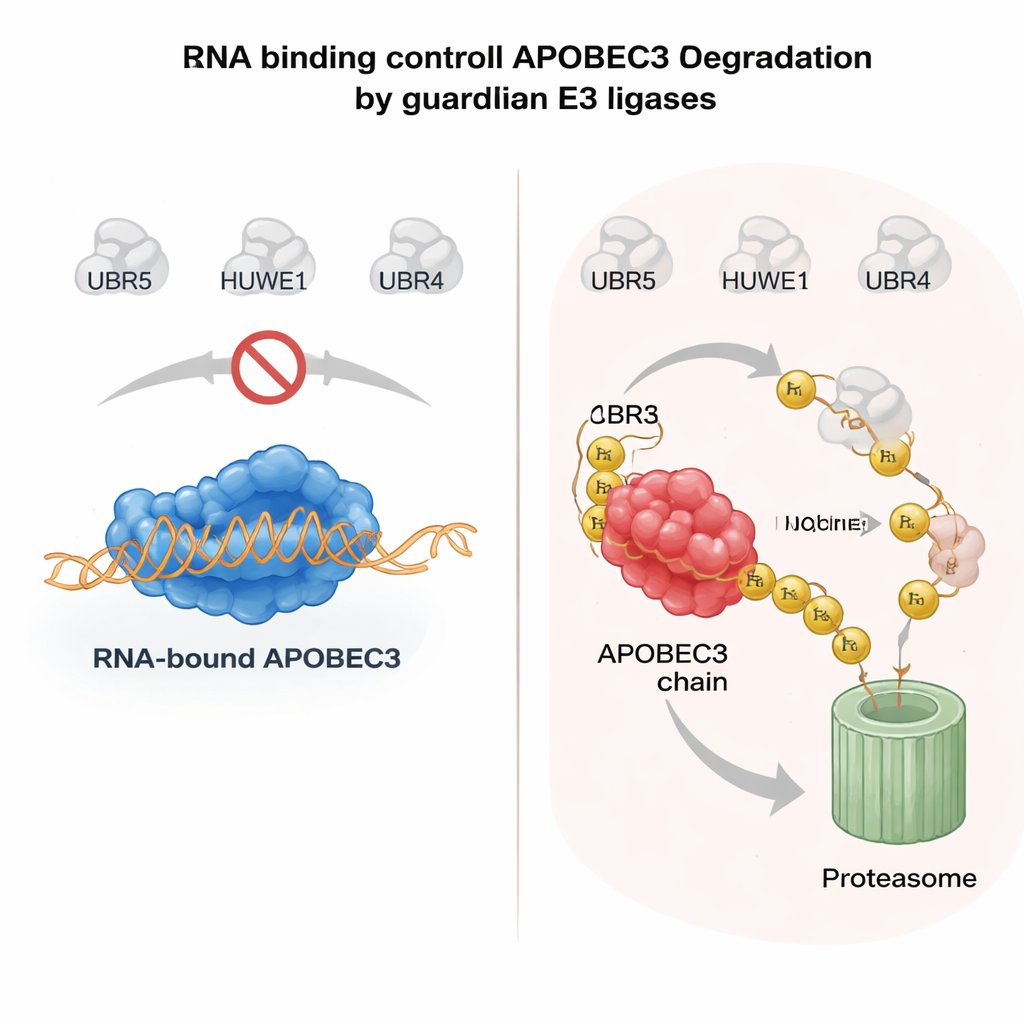
L’RNA come cintura di sicurezza per enzimi rischiosi
Cosa determina se un enzima APOBEC3 viene risparmiato o distrutto? Un indizio chiave è venuto dal modo in cui le proteine APOBEC3 si legano alle molecole di RNA nel citoplasma. Quando A3H o un altro membro della famiglia, A3G, si legano all’RNA, tendono a rimanere in grandi complessi nel citosol e risultano relativamente stabili. Mutazioni che indeboliscono il legame con l’RNA fanno sì che questi enzimi migrino nel nucleo, perdano i partner protettivi e diventino altamente instabili. Gli autori hanno dimostrato che quando le proteine APOBEC3 non sono legate all’RNA, UBR5 e HUWE1 riconoscono superfici esposte sull’enzima, le decorano con ubiquitina e le indirizzano alla degradazione nucleare. In sistemi purificati, l’aggiunta di RNase per rimuovere l’RNA aumentava notevolmente la capacità di queste ligasi di legarsi e ubiquitinare gli APOBEC3, confermando che il legame all’RNA agisce come uno scudo molecolare. Questo meccanismo permette alle cellule di mantenere gli APOBEC3 antivirali attivi nel citoplasma eliminando rapidamente qualsiasi pool non legato e pericoloso nel nucleo.
Quando i guardiani falliscono: collegamenti con le mutazioni tumorali
Se UBR4, UBR5 e HUWE1 agiscono da guardiani, la loro perdita dovrebbe aumentare i livelli di mutazione. I ricercatori hanno testato ciò disabilitando ciascuna ligasi in cellule di cancro colon-rettale e monitorando i cambiamenti del DNA nel tempo utilizzando un metodo di sequenziamento sensibile che legge le “firme” mutazionali. La rimozione di queste ligasi, in particolare in cellule che esprimono A3H-I, ha amplificato i modelli mutazionali specifici di APOBEC—proprio il tipo riscontrato nei tumori umani. Estendendo l’analisi ai dati dei pazienti, hanno esaminato migliaia di genomi tumorali e scoperto che i tumori con mutazioni in UBR5 o HUWE1 presentavano una frazione significativamente maggiore di firme mutazionali legate ad APOBEC rispetto ai tumori con ligasi intatte, anche tenendo conto del carico mutazionale complessivo. Ciò suggerisce che ligasi-guardiane difettose nei pazienti potrebbero consentire agli APOBEC3 associati al cancro di scatenarsi e rimodellare il genoma tumorale.
Cosa significa per la cura del cancro in futuro
Per un non specialista, il messaggio è che le nostre cellule dispongono di un sofisticato sistema di controllo per impedire agli enzimi antivirali utili di sabotare accidentalmente il nostro DNA. UBR4, UBR5 e HUWE1 agiscono da guardiani che percepiscono quando gli enzimi APOBEC3 non sono più saldamente legati all’RNA e, specialmente nel nucleo, li mandano al trituratore cellulare. Quando questo sistema di controllo è indebolito—per mutazioni nelle ligasi o per farmaci che bloccano la degradazione proteica—l’attività di APOBEC3 può alimentare il caos genetico che guida l’evoluzione tumorale e la resistenza alle terapie. Comprendere questa rete di guardiani apre la strada a nuovi marcatori diagnostici, come le mutazioni delle ligasi o i livelli delle proteine APOBEC, e suggerisce che modulare con attenzione questa via potrebbe un giorno aiutare a limitare le esplosioni di mutazioni dannose nei tumori senza compromettere le nostre difese antivirali.
Citazione: Schwartz, I., Budroni, V., Meyenberg, M. et al. Guardian ubiquitin E3 ligases target cancer-associated APOBEC3 deaminases for degradation to promote human genome integrity. Nat Commun 17, 1723 (2026). https://doi.org/10.1038/s41467-026-68420-5
Parole chiave: APOBEC3, stabilità del genoma, ligasi dell’ubiquitina, mutagenesi nel cancro, degradazione proteica