Clear Sky Science · it
Patternazione spaziale della contrattilità da un gradiente di attività di un meccanogeno auto-organizzato sottende la gastrulazione di Drosophila
Come i tessuti si modellano
Gli embrioni precoci trasformano in qualche modo semplici fogli cellulari in forme tridimensionali complesse. Questo studio pone una domanda fondamentale dietro quel trucco: come coordinano le cellule dove stringere e flettersi affinché un tessuto si pieghi nel punto e nella direzione giusti? Osservando embrioni di mosca ad alta risoluzione, gli autori scoprono un segnale chimico che si comporta come un “morfogeno meccanico”, modellando direttamente dove le cellule si contraggono per guidare un evento cruciale di piegatura durante lo sviluppo.
Un’onda che piega l’embrione
Nella mosca della frutta Drosophila, un passo chiave dello sviluppo precoce è la gastrulazione, quando uno strato piatto di cellule si incurva verso l’interno per cominciare a formare l’intestino. Nella parte posteriore dell’embrione, un ammasso di cellule chiamato primordio dell’endoderma posteriore avvia questo processo contraendosi sul lato superiore (apicale). Questa piega iniziale dà il via a un’onda viaggiante di invaginazione tissutale che si propaga in avanti attraverso le cellule vicine. Gli autori mostrano che quest’onda dipende da un segnale chiamato Fog, una molecola secreta che attiva una famiglia di recettori noti come GPCR, i quali a loro volta accendono la macchina contrattile cellulare formata dalla proteina motrice Miosina-II.
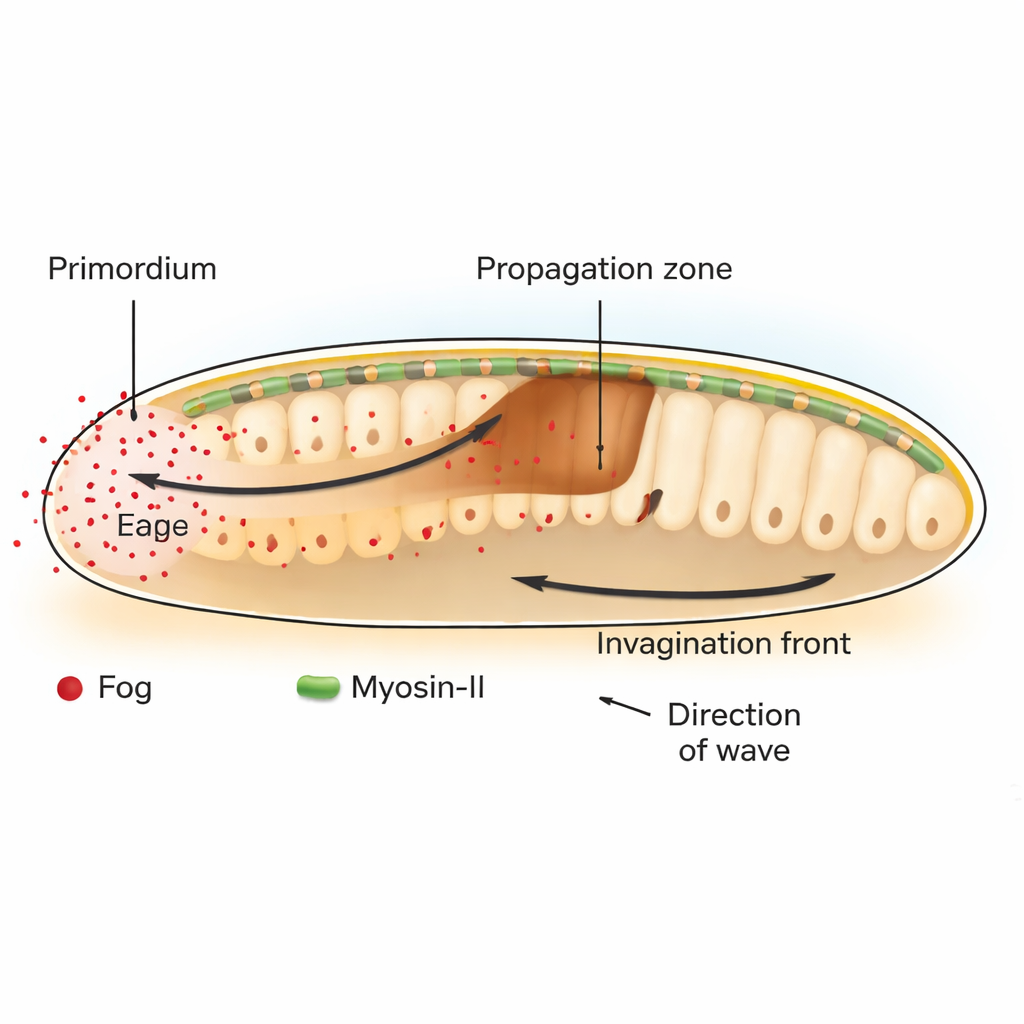
Una chimica che modella la forza, non il destino
Classicamente, i biologi dello sviluppo si sono concentrati sui “morfogeni”, molecole diffondenti i cui gradienti di concentrazione dicono alle cellule quale identità assumere. Qui, Fog si comporta in modo diverso. Piuttosto che cambiare che tipo di cellula diventerà una regione, Fog regola direttamente quanto forte le cellule si contraggono. Ripristinando o bloccando selettivamente Fog e il suo messaggero a valle Gα solo in certe regioni, i ricercatori dimostrano che il Fog prodotto nel primordio è sia necessario sia sufficiente per attivare Miosina-II e la piegatura tissutale a distanza nella zona di propagazione adiacente. Quando Fog è ancorato in modo da non potersi diffondere, si contraggono solo le cellule produttrici e l’onda di invaginazione si arresta dopo una o due file cellulari.
Un gradiente nascosto sulla superficie cellulare
Un’idea naturale è che Fog possa formare un classico gradiente di concentrazione al di fuori delle cellule. Usando una versione fluorescentemente marcata di Fog e misure di fluorescenza sensibili, il gruppo trova l’opposto: nello strato fluido sottile tra il tessuto e la sua membrana esterna (la membrana vitellina), Fog è sorprendentemente uniforme. Eppure l’attività di Miosina-II forma chiaramente un gradiente viaggiante ripido, massimo proprio davanti alla piega avanzante e che sfuma dopo poche diametri cellulari. Il pezzo mancante è che Fog non agisce come un semplice indizio di concentrazione nel volume; invece, una piccola frazione di Fog rimane brevemente intrappolata sulla superficie cellulare, legandosi ai suoi recettori GPCR e formando un gradiente di attività legata alla superficie anche se le molecole libere di Fog restano uniformemente miscelate nel fluido.
Recettori, endocitosi e adesione plasmano l’onda
Gli autori mostrano che questo Fog legato alla superficie, insieme ai suoi recettori, si auto-organizza in un pattern. Dove Fog incontra ripetutamente i recettori, promuove l’aggregazione e l’attivazione dei recettori, che recluta più Miosina-II. Un processo cellulare di “pulizia”—l’endocitosi dei GPCR—rimuove poi i complessi attivi, impedendo un’attivazione incontrollata e aiutando a sintonizzare quanto lontano il segnale si diffonde. Quando questa endocitosi è geneticamente rallentata, il gradiente di Miosina-II diventa più alto e più ampio. Un secondo attore chiave è un insieme di molecole di adesione chiamate integrine. Mano a mano che il tessuto si piega, le cellule davanti alla piega premono contro la membrana vitellina; questo contatto attiva localmente le integrine, che a loro volta potenziano l’efficacia della segnalazione Fog–GPCR. La regione di forte ingaggio delle integrine corrisponde all’estensione del gradiente di Miosina-II e senza integrine l’onda diventa debole e di breve raggio anche se la segnalazione Fog è altrimenti potenziata.
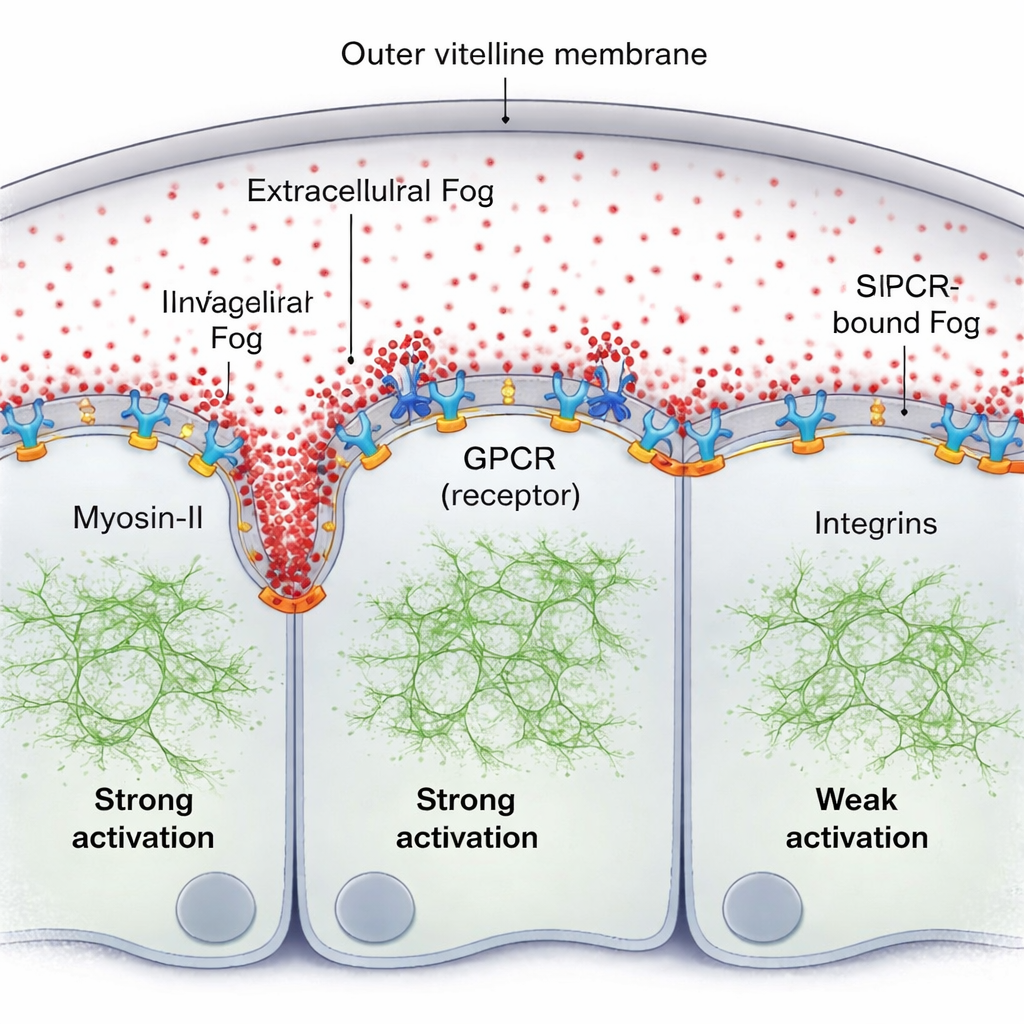
Un pattern meccanico auto-rigenerante
Per un non specialista, il messaggio principale è che l’embrione non si affida esclusivamente a mappe chimiche preimpostate per decidere dove piegarsi. Invece costruisce un pattern mobile di attività meccanica in tempo reale. Fog si diffonde in modo uniforme, ma la sua azione efficace è scolpita sulla superficie cellulare dall’aggregazione dei recettori, dalla rimozione dei recettori e dalla geometria tissutale che cambia quando le cellule premono contro l’ambiente circostante. Questo crea un gradiente viaggiante auto-organizzato di forza contrattile che tira il tessuto verso l’interno in un’onda coordinata. Il lavoro offre un esempio concreto di un a lungo teorizzato “meccanogeno”: una molecola diffusiva che modella direttamente le forze fisiche in un tessuto, aiutando a spiegare come gli organismi viventi si scolpiscono così affidabilmente durante lo sviluppo.
Citazione: Mundhe, G., Dunsing-Eichenauer, V., Philippe, JM. et al. Spatial patterning of contractility by a self-organized mechanogen activity gradient underlies Drosophila gastrulation. Nat Commun 17, 1721 (2026). https://doi.org/10.1038/s41467-026-68418-z
Parole chiave: gastrulazione, meccanogeno, embrione di Drosophila, meccanica tissutale, segnalazione Fog