Clear Sky Science · it
Le configurazioni delle estremità del DNA determinano la formazione del complesso sinaptico durante il ponte degli estremi mediato da NHEJ
Quando il DNA si rompe, le cellule devono agire in fretta
Ogni giorno il DNA nelle nostre cellule viene scheggiato, tagliato e danneggiato dal metabolismo normale e da stress ambientali. Tra le lesioni più pericolose ci sono le rotture a doppio filamento, in cui entrambi i filamenti della doppia elica si spezzano. Se queste lesioni non vengono riparate rapidamente e con precisione, le cellule possono morire o, peggio, avviarsi verso il cancro. Questo studio esplora come la forma e la chimica esatte delle estremità del DNA spezzato contribuiscano a decidere se una via di riparazione chiave, chiamata giunzione non omologa delle estremità (NHEJ), metta insieme quegli estremi in modo efficiente e con il minor numero possibile di errori.
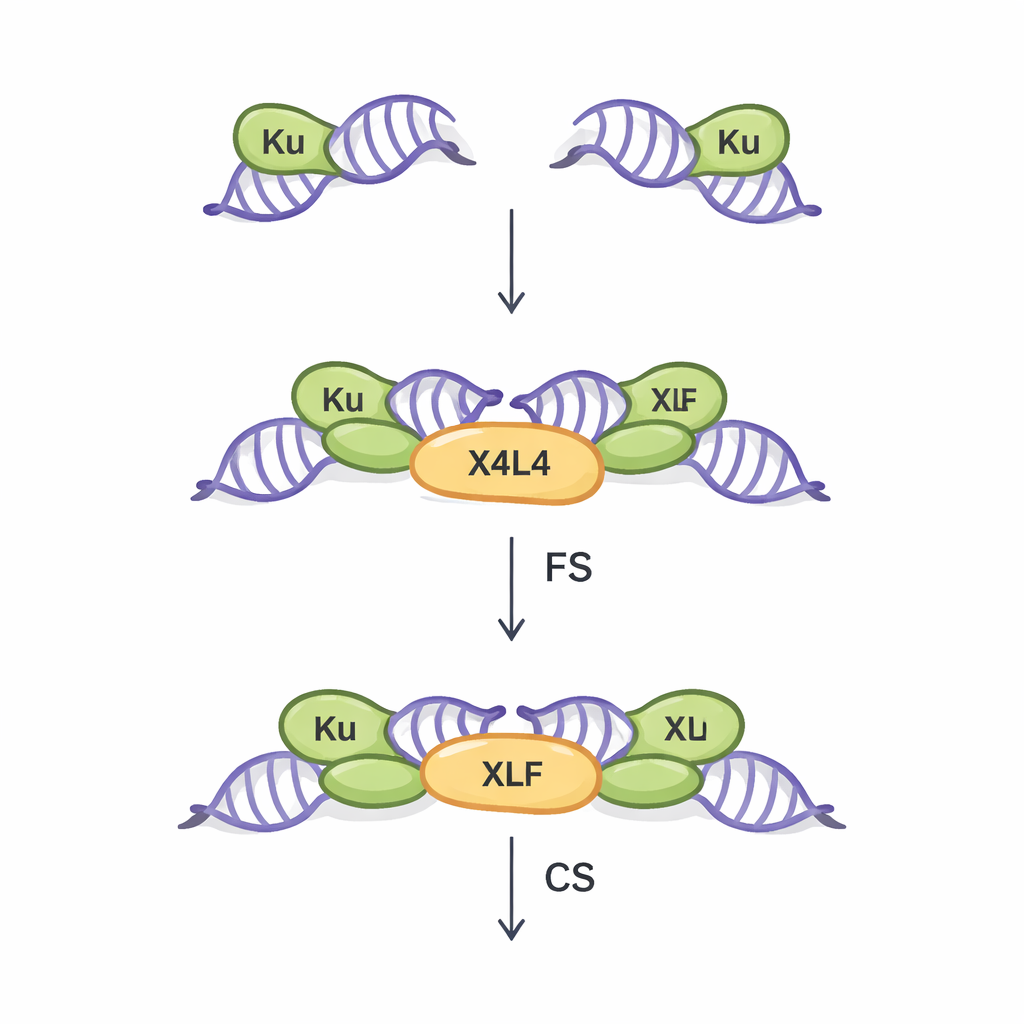
Due modi per avvicinare estremità di DNA spezzate
La NHEJ è la principale via di riparazione per le rotture a doppio filamento nella maggior parte delle cellule del nostro corpo. Funziona senza bisogno di un modello di DNA corrispondente, il che la rende rapida ma in qualche misura soggetta a errori. Il primo passaggio cruciale in questa via è chiamato sinapsi: il ponte fisico tra le due estremità del DNA spezzato in modo che possano poi essere unite. Lavori precedenti, per lo più basati su estremità di DNA ideali e nette, avevano rivelato due tipi di assemblaggi sinaptici. Nello stato “sinaptico flessibile” (FS), le estremità sono tenute vicine e possono muoversi, sondando possibili accoppiamenti. Nello stato “sinaptico stretto” (CS), le estremità si allineano testa a testa e sono pronte per essere sigillate da un enzima ligante. Tre proteine fondamentali—Ku, XRCC4–Ligasi IV (insieme indicate come X4L4) e XLF—sono note per coordinare questo processo, ma è rimasto poco chiaro come estremità di DNA reali e irregolari influenzino quale stato sinaptico si formi.
La forma delle estremità e brevi corrispondenze indirizzano la via di riparazione
I ricercatori hanno utilizzato la FRET a molecola singola, una tecnica basata sulla fluorescenza che misura distanze a scala nanometrica, per osservare singole molecole di DNA mentre venivano avvicinate dalle proteine NHEJ. Hanno confrontato estremità semplici e nette con estremità più realistiche che portavano brevi sporgenze—piccole code a filamento singolo che possono potenzialmente appaiarsi. Hanno scoperto che quando le sporgenze sono complementari, anche solo per poche basi, aumentano drasticamente la probabilità di formare un complesso sinaptico stretto. In effetti, tre basi corrispondenti di “microomologia” alla rottura sono state sufficienti perché Ku e X4L4 da soli generassero un complesso CS stabile, senza bisogno di XLF. Ciò dimostra che lo stesso DNA può fornire parte dell’energia e dell’orientamento normalmente forniti dalle proteine ausiliarie.
Come piccole alette di DNA aiutano a stabilizzare il ponte
Analizzando distinti segnali FRET, il gruppo ha identificato almeno due configurazioni strutturali dello stato sinaptico stretto per estremità con sporgenze. In una, le punte delle sporgenze si appaiano tra loro, generando una giunzione nickata o con gap. Nell’altra, le giunzioni in cui il DNA a doppio filamento incontra le sporgenze a filamento singolo si comprimono in linea, mentre le sporgenze si ripiegano verso l’esterno come piccole alette. Queste alette consentono comunque l’appaiamento delle basi e mantengono le estremità in strettissima prossimità, il che probabilmente stabilizza il complesso e lascia spazio agli enzimi per accorciare o allungare il DNA secondo necessità prima della sigillatura finale. In modo intrigante, danni ossidativi comuni nelle sporgenze, come l’8-ossoguanina, hanno influenzato solo modestamente questo processo, evidenziando quanto la NHEJ sia robusta rispetto a certe forme di danno.
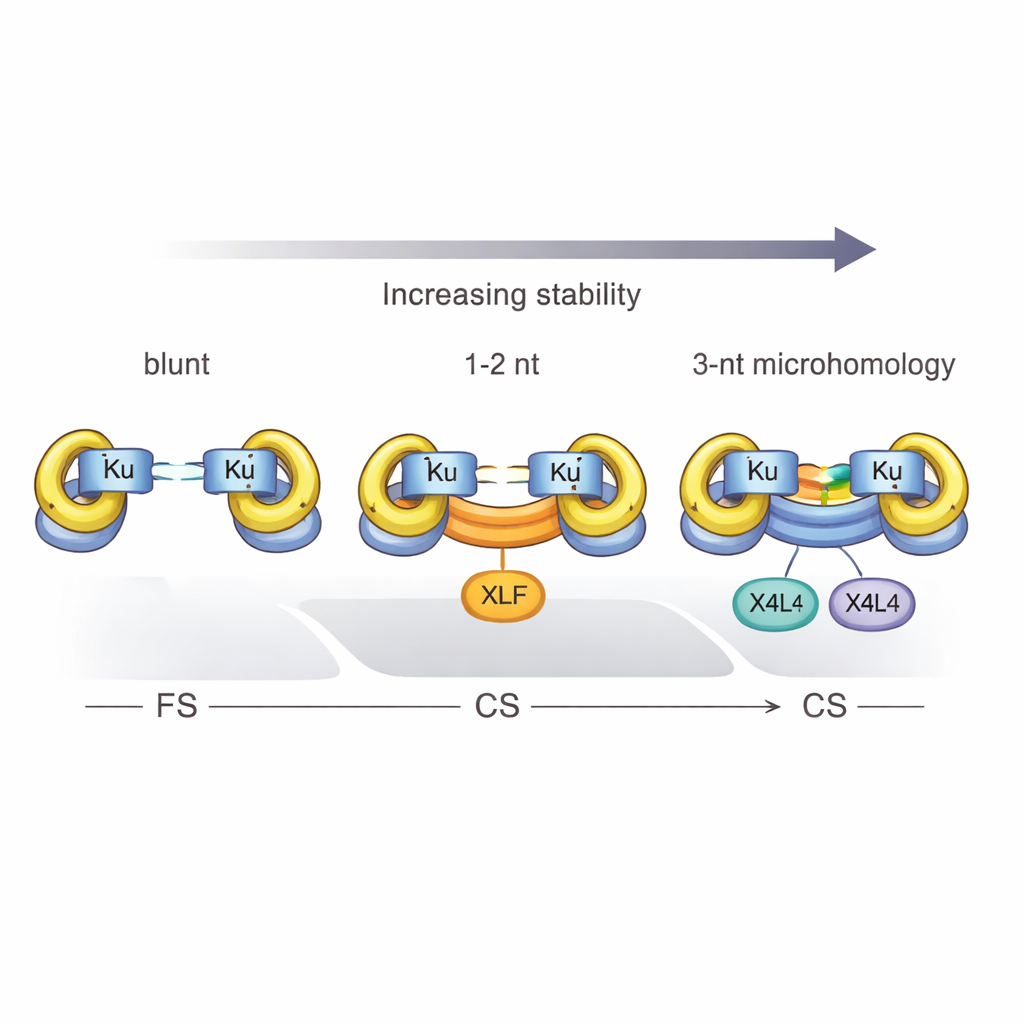
Proteine, fosfati e la forza del tre
Lo studio ha anche definito una soglia netta: sono richieste almeno tre basi appaianti complementari perché Ku e X4L4 convertano in modo affidabile un complesso flessibile in uno stretto. Con una o due corrispondenze, il sistema resta per lo più bloccato nello stato flessibile a meno che XLF non intervenga per aiutare a serrare le estremità. Anche i dettagli chimici contano. Quando il DNA rotto porta un gruppo fosfato 5′—una caratteristica normale di molte rotture fisiologiche—la sinapsi diventa più efficiente e i complessi stretti hanno maggior probabilità di essere effettivamente ligati, trasformando un ponte temporaneo in una riparazione permanente. Tuttavia, questo potenziamento dovuto al fosfato non può sostituire completamente l’effetto stabilizzante dell’appaiamento delle basi alla rottura.
Perché questo conta per la salute e l’editing genomico
In parole semplici, questo lavoro mostra che le estremità del DNA spezzato non sono vittime passive in attesa di essere riparate. Le loro forme esatte, piccole aree di sequenza corrispondente e tag chimici guidano attivamente il modo in cui le proteine di riparazione afferrano, allineano e riconnettono gli estremi. Quando sono presenti tre o più basi corrispondenti, le estremità del DNA aiutano esse stesse a bloccare la rottura in una configurazione pronta per la riparazione, rendendo talvolta opzionali alcune proteine ausiliarie. Quando tali corrispondenze scarseggiano, fattori proteici aggiuntivi diventano essenziali. Queste intuizioni aiutano a spiegare perché alcune rotture vengono riparate ordinatamente mentre altre portano a piccole mutazioni o riorganizzazioni. Offrono anche indizi per migliorare strumenti di editing del genoma come CRISPR, dove rotture del DNA deliberate vengono riparate dalla stessa macchina NHEJ. Regolando le estremità di quelle rotture, gli scienziati potrebbero controllare meglio come il genoma viene rimodellato.
Citazione: Zhang, C., Jin, W., Jiang, Y. et al. DNA end configurations dictate synaptic complex formation during NHEJ-mediated end bridging. Nat Commun 17, 1720 (2026). https://doi.org/10.1038/s41467-026-68417-0
Parole chiave: riparazione delle rotture a doppio filamento del DNA, giunzione non omologa delle estremità, sinapsi del DNA, microomologia, stabilità del genoma