Clear Sky Science · it
Un singolo cambiamento da valina a leucina interrompe il legame di Plasmodium falciparum AP2-G con il DNA e rivela il ruolo di GDV1 nell’attivazione di ap2-g
Come i parassiti della malaria prendono una scelta cruciale di vita o di morte
I parassiti della malaria che vivono nel nostro sangue affrontano costantemente una decisione che cambia la loro esistenza: continuare a moltiplicarsi in un singolo ospite o trasformarsi in una forma capace di passare al prossimo ospite tramite la puntura di una zanzara. Questo studio svela come una singola, piccolissima modifica in una proteina del parassita possa spegnere completamente quella fase infettiva pronta per la zanzara, offrendo nuovi punti di attacco per bloccare la trasmissione della malaria.
Il bivio del parassita
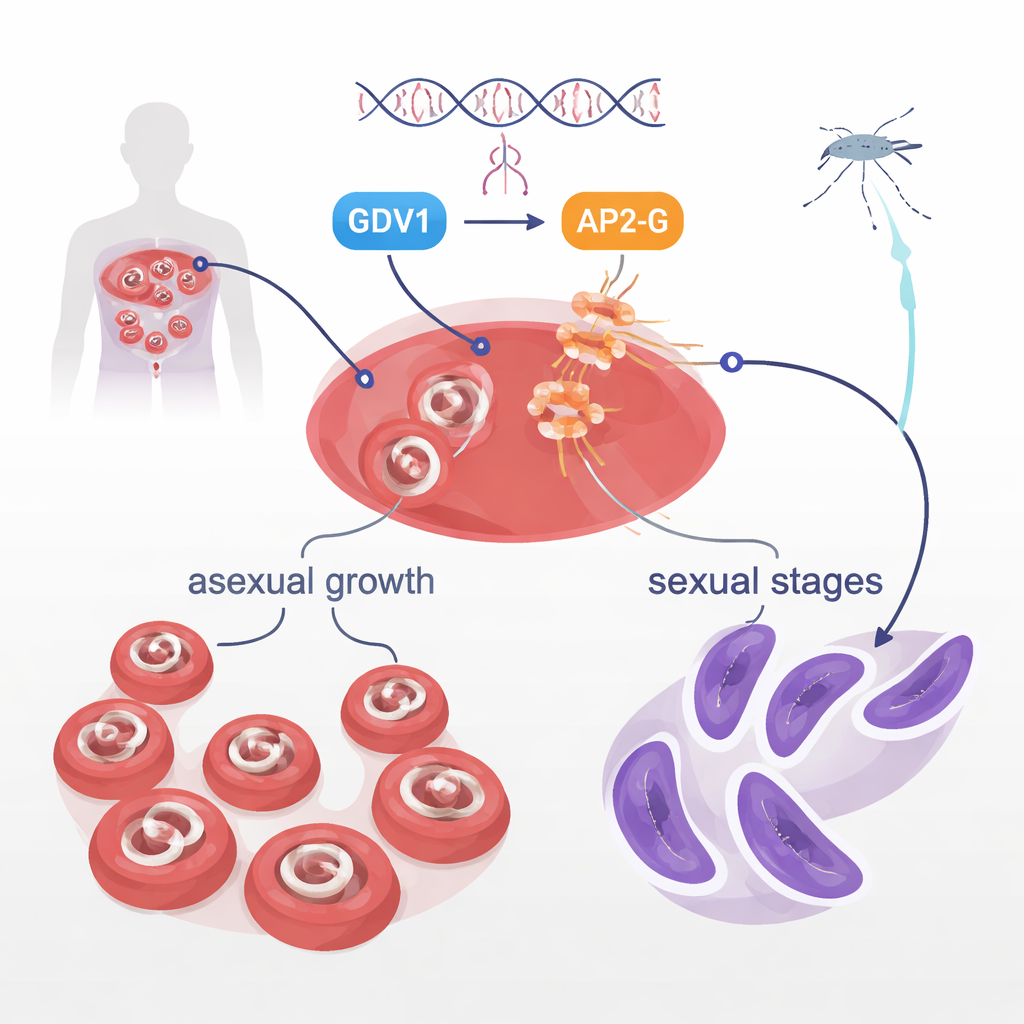
Nella circolazione sanguigna, i parassiti Plasmodium falciparum si concentrano per lo più sulla crescita rapida, che provoca la malattia. Ma una piccola minoranza si trasforma in forme sessuate chiamate gametociti, le uniche fasi che le zanzare possono acquisire e trasmettere. Perché solo alcuni parassiti in un popolazione facciano questo passaggio è stato a lungo un mistero. Studi precedenti avevano mostrato che due proteine del parassita, GDV1 e una proteina legante il DNA chiamata AP2-G, sono al centro di questa decisione. GDV1 aiuta a risvegliare il gene ap2-g normalmente silenziato, e AP2-G a sua volta attiva una serie di geni che guidano lo sviluppo sessuale. L’attuale studio si proponeva di esplorare un’altra proteina, una chinasi chiamata STK2, ma ha invece scoperto un risultato molto più drammatico proprio in AP2-G.
Un singolo amminoacido che blocca la trasmissione
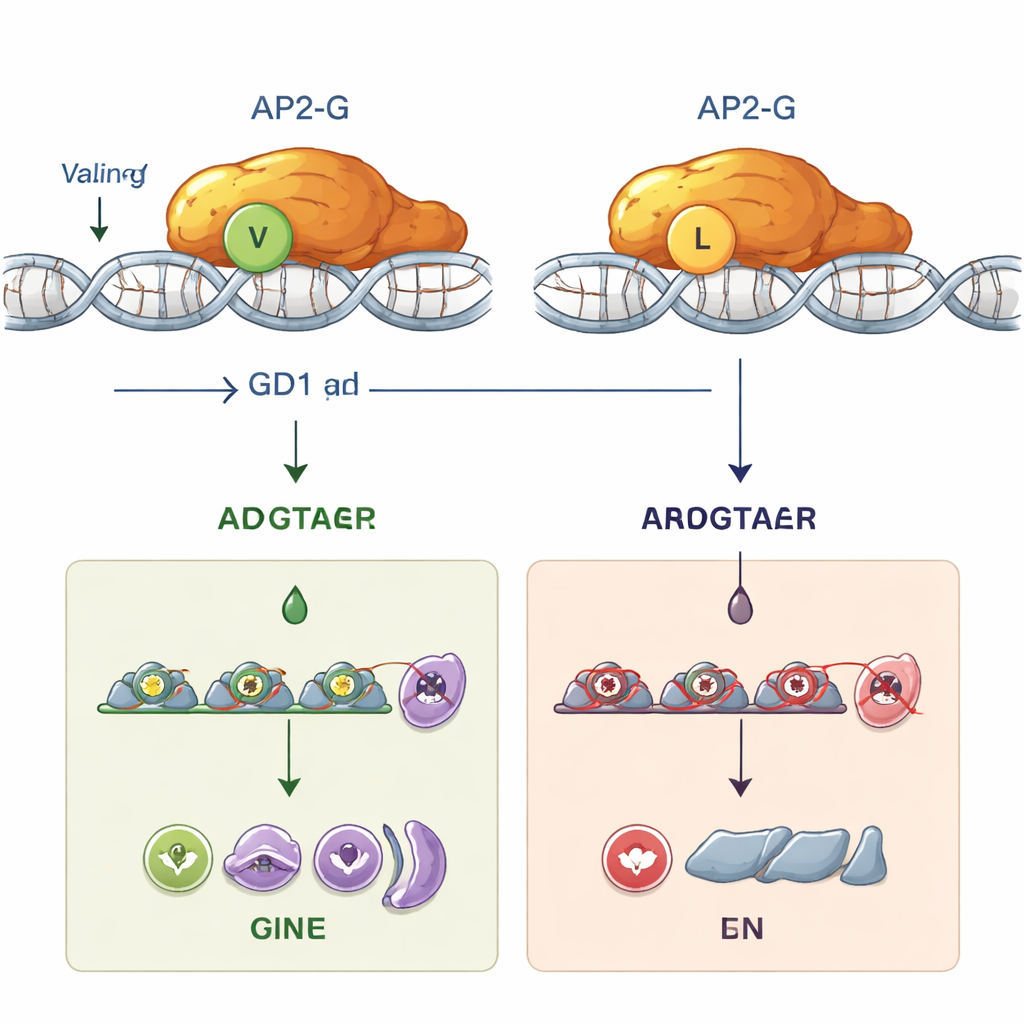
Nel corso della cancellazione del gene stk2 in un ceppo di laboratorio del parassita, i ricercatori hanno notato che questi parassiti avevano perso completamente la capacità di produrre gametociti, pur continuando a crescere asessualmente senza problemi. Con sorpresa, ripetendo manipolazioni analoghe in un altro ceppo, i gametociti si formavano normalmente. Il sequenziamento dell’intero genoma ha rivelato il colpevole nascosto: un singolo cambiamento di “lettera” nel gene ap2-g, che scambia un amminoacido, valina, con uno molto simile, leucina, nella posizione 2163. Questa posizione si trova all’inizio della regione di legame al DNA di AP2-G, la parte che afferra fisicamente specifici motivi del DNA per attivare i geni. Questo minuscolo passaggio da valina a leucina da solo era sufficiente ad abolire la formazione dei gametociti. Quando gli scienziati hanno introdotto ingegneristicamente questa mutazione in parassiti altrimenti normali, i gametociti sono scomparsi; quando l’hanno ripristinata a valina, lo sviluppo sessuale è stato completamente recuperato.
Come l’interruttore rompe la serratura molecolare
Per capire perché questo cambiamento sottile sia così devastante, il gruppo ha combinato modellizzazione al computer e esperimenti di laboratorio. Le previsioni strutturali suggerivano che la sostituzione della valina con la leucina sposta e destabilizza la forma precisa del dominio di legame al DNA di AP2. In saggi in provetta con proteine purificate, l’AP2-G normale si legava con forza alla sua sequenza di DNA preferita, un breve codice contenente il motivo “GnGTAC”. Al contrario, l’AP2-G mutante con la leucina in posizione 2163 non si legava affatto a questa sequenza. Senza un legame stabile al DNA, AP2-G non poteva più attivare il proprio gene (un circuito di retroazione positiva noto come autoregolazione) né attivare dozzine di geni a valle necessari a spingere i parassiti verso il percorso sessuale. Funzionalmente, i parassiti mutanti sono diventati “sterili”: non potevano produrre le forme che infettano le zanzare, pur prosperando nei globuli rossi.
Il ruolo nascosto di GDV1 prima che AP2-G prenda il sopravvento
La mutazione ha inoltre fornito ai ricercatori uno strumento unico: parassiti in cui il gene ap2-g può essere attivato, ma AP2-G non è in grado di legare il DNA. Utilizzando reporter fluorescenti e luminescenti, hanno seguito quando agiscono i diversi attori durante il ciclo di 48 ore del parassita nei globuli rossi. Hanno scoperto che la proteina GDV1 compare per prima, precocemente in una fase chiamata scizogonia, ed è essenziale per avviare l’espressione di ap2-g dallo stato silenziato. Questa attivazione precoce avveniva sia che ap2-g codificasse AP2-G normale sia la versione mutante. Solo più tardi, una volta che si era accumulata una quantità sufficiente di AP2-G normale, il forte circuito di autoamplificazione e l’attivazione di altri geni “sessuali” si verificavano. Un marcatore chiave, una proteina chiamata MSRP1, si accendeva solo nei parassiti con AP2-G funzionale, offrendo un modo pratico per distinguere i parassiti sessualmente impegnati in fasi iniziali o tardive. Nelle linee mutanti con la sostituzione in leucina, GDV1 riusciva ancora a risvegliare ap2-g, ma la proteina AP2-G difettosa non poteva portare avanti il processo, così lo sviluppo sessuale si arrestava.
Implicazioni per fermare la diffusione della malaria
Per il lettore generale, la conclusione è semplice: i parassiti della malaria si affidano a una serratura molecolare estremamente sensibile per decidere se diventeranno trasmissibili. Questo studio mostra che cambiare una sola “dente” di quella serratura — una singola valina nella regione che afferra il DNA di AP2-G — impedisce al parassita di formare le fasi infettive per le zanzare. Allo stesso tempo, chiarisce che un’altra proteina, GDV1, agisce prima come chiave per sbloccare inizialmente il gene ap2-g silenziato, prima che AP2-G ne rafforzi la propria produzione e attivi un programma sessuale più ampio. Mappando questa sequenza di eventi e creando linee di parassiti reporter che si illuminano quando ogni passaggio avviene, il lavoro fornisce strumenti potenti per testare farmaci o fattori umani che interferiscono con l’impegno sessuale. A lungo termine, prendere di mira la regione di legame al DNA di AP2-G o il passaggio di attivazione guidato da GDV1 potrebbe costituire la base di nuove strategie che non solo curano la malaria in un paziente, ma interrompono completamente la catena di trasmissione.
Citazione: Prajapati, S.K., Dong, J.X., Morahan, B.J. et al. A single valine to leucine switch disrupts Plasmodium falciparum AP2-G DNA binding and reveals GDV1’s role in ap2-g activation. Nat Commun 17, 1719 (2026). https://doi.org/10.1038/s41467-026-68416-1
Parole chiave: trasmissione della malaria, Plasmodium falciparum, sviluppo dei gametociti, AP2-G, GDV1