Clear Sky Science · it
I meccanismi gerarchici controllano lo smaltimento della RNA polimerasi II bloccata da lesioni del DNA
Quando le macchine che copiano i geni incontrano un ostacolo
Ogni secondo, milioni di piccole macchine molecolari chiamate RNA polimerasi II percorrono il nostro DNA copiando i geni in RNA. Ma quando il DNA è danneggiato — per esempio dalla luce ultravioletta (UV) del sole — queste macchine possono bloccarsi. Se le copie bloccate si accumulano, le cellule non riescono più a leggere correttamente i loro geni, cosa particolarmente pericolosa per le cellule cerebrali e che può portare a malattie rare come la sindrome di Cockayne. Questo studio svela, in dettaglio, come le cellule riconoscono queste macchine bloccate e le riavviano o le rimuovono prima che causino danni duraturi.
Un nuovo modo per osservare gli ingorghi cellulari
Per capire come le cellule liberano le polimerasi bloccate, i ricercatori hanno costruito una «telecamera del traffico» temporale per la trascrizione. Hanno usato un farmaco che permette alle molecole esistenti di RNA polimerasi II di continuare a muoversi ma impedisce a nuove di iniziare il viaggio, per poi creare una piccola zona di danno da UV all’interno di ogni nucleo cellulare. Seguendo un marcatore chimico della forma attiva della polimerasi, hanno potuto osservare quanto rapidamente questa scompariva dalla zona danneggiata rispetto al resto del genoma. In parallelo, hanno sviluppato un test complementare che misurava la quantità totale di polimerasi attiva negli estratti cellulari, rivelando non solo quando le polimerasi lasciavano il DNA, ma anche quando venivano degradate dal sistema di smaltimento cellulare.
Marcatura delle macchine bloccate per la rimozione
Il team si è concentrato sulla riparazione accoppiata alla trascrizione, un sistema specializzato che corregge le lesioni sui geni attivamente letti. Hanno utilizzato una serie corrispondente di linee cellulari umane, ciascuna priva di un diverso fattore di riparazione. Due proteine, CSB e CSA, sono emerse come guardiani decisivi. Quando una delle due mancava, la RNA polimerasi II si accumulava e rimaneva ostinatamente nei siti di danno, e la cellula non riusciva a degradarla. A livello biochimico, queste cellule non riuscivano neppure ad attaccare piccole etichette ubiquitine in un sito chiave della polimerasi. Al contrario, le cellule prive di proteine coinvolte nelle fasi successive della riparazione — quelle che asportano e sostituiscono il DNA danneggiato — eliminavano comunque la polimerasi in modo normale. Questo ha mostrato che la marcatura iniziale con ubiquitina della polimerasi bloccata è il segnale critico per decidere il suo destino.
Due squadre di pulizia: una veloce e una di riserva
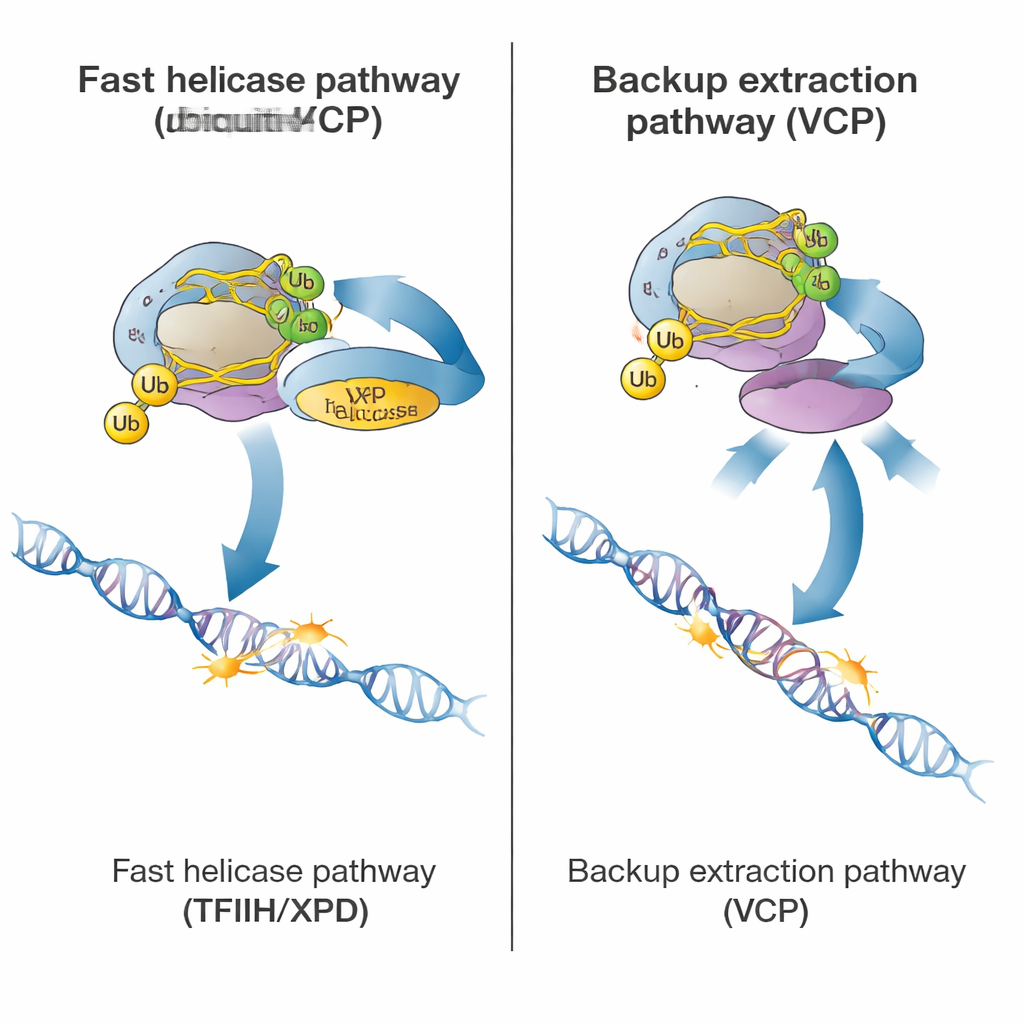
Una volta marcata, la cellula può scegliere tra due vie per eliminarla. La via primaria e rapida si affida a un grande complesso di riparazione chiamato TFIIH, e in particolare alla sua subunità elicasi XPD, che usa energia per svolgere il DNA. Proteine helper, tra cui ELOF1, UVSSA e STK19, portano TFIIH alla polimerasi bloccata e posizionano XPD sul DNA appena davanti ad essa. Usando nuovi test in cellule di pazienti portatrici di una mutazione che inattiva l’elicasi XPD, gli autori hanno mostrato che quando XPD non può svolgere il DNA, la rimozione della polimerasi rallenta drasticamente, anche se il resto della macchina di riparazione è presente. Ciò indica che l’azione meccanica di «strappo» operata da XPD è ciò che di norma «scongela» la polimerasi dalla lesione permettendo agli enzimi di riparazione di raggiungere il sito danneggiato.
Un piano B lento ma essenziale
Lo studio ha anche rivelato una via di emergenza più lenta per liberare la polimerasi bloccata. Questo percorso dipende da VCP (noto anche come p97), una proteina che riconosce i marchi di ubiquitina e può estrarre forzatamente le proteine dalla cromatina. Nelle cellule sane con TFIIH pienamente funzionante, il blocco di VCP aveva solo un effetto modesto. Ma nelle cellule in cui TFIIH era assente, mal posizionato o con l’elicasi inattiva, la rimozione della polimerasi diventava quasi interamente dipendente da VCP. In questi casi, VCP riusciva comunque a tirare la polimerasi marcata lontano dal DNA, anche quando la riparazione normale non poteva procedere. Crucialmente, questa via di riserva richiedeva comunque una certa marcatura con ubiquitina, spiegando perché le cellule prive di CSB o CSA — e quindi senza marchi di ubiquitina — fallivano sia nella via principale sia in quella di riserva.
Perché questo è importante per la salute e la malattia
Nel complesso, il lavoro delinea un programma di sicurezza gerarchico che le cellule usano ogni volta che la RNA polimerasi II incontra un danno al DNA. Per prima cosa, CSB e CSA segnalano la macchina bloccata con ubiquitina. Se tutto funziona correttamente, TFIIH e la sua elicasi XPD smuovono rapidamente la polimerasi in modo che la lesione possa essere rimossa e riparata. Se TFIIH non può svolgere il suo compito, VCP interviene per estrarre la polimerasi e inviarla alla degradazione, impedendo che ostruisca l’espressione genica anche se il danno al DNA rimane. Questo quadro aiuta a spiegare perché i difetti ereditari in CSB o CSA causano problemi neurologici particolarmente gravi: senza la marcatura con ubiquitina, le cellule perdono sia la via primaria guidata dalla riparazione sia la via di riserva dell’estrazione, lasciando le polimerasi bloccate sui geni danneggiati e la trascrizione cronicamente arrestata.
Citazione: van der Meer, P.J., Yakoub, G., Tsukada, K. et al. Hierarchical mechanisms control the clearance of DNA lesion–stalled RNA polymerase II. Nat Commun 17, 1647 (2026). https://doi.org/10.1038/s41467-026-68413-4
Parole chiave: riparazione del DNA accoppiata alla trascrizione, RNA polimerasi II, danno al DNA indotto da UV, ubiquitinazione delle proteine, sindrome di Cockayne