Clear Sky Science · it
Visualizzazione in situ dell’eterogeneità fenotipica e della morfologia cellulare singola di Clostridioides difficile durante l’infezione intestinale
Perché i microbi intestinali non si comportano tutti allo stesso modo
Clostridioides difficile, spesso chiamato C. diff, è un microrganismo noto per le infezioni ospedaliere che può provocare diarrea grave e talvolta pericolosa per la vita dopo che gli antibiotici hanno alterato i normali batteri intestinali. Eppure, anche quando questi batteri sono geneticamente identici e condividono lo stesso ambiente, le singole cellule possono comportarsi in modo molto diverso. Questo studio rivela, con dettaglio senza precedenti, come singole cellule di C. diff attivino o disattivino la produzione di tossine e perfino cambino forma durante l’infezione dell’intestino del topo, offrendo indizi sul perché la malattia possa essere così persistente e difficile da trattare.
Seguire in tempo reale un pericoloso invasore intestinale
Per capire come si comportano le singole cellule di C. diff all’interno dell’organismo, i ricercatori avevano bisogno di un modo per vederle chiaramente in mezzo alla densa e diversificata comunità microbica intestinale. Hanno ingegnerizzato ceppi di C. diff che brillano continuamente con colori accesi al microscopio, usando proteine fluorescenti speciali che non interferiscono con la capacità dei batteri di crescere o di causare malattia. Infettando topi trattati con antibiotici con questi ceppi luminosi e poi affettando e colorando il colon, hanno potuto individuare le posizioni esatte e i comportamenti di migliaia di singole cellule batteriche all’interno del tessuto intestinale integro. 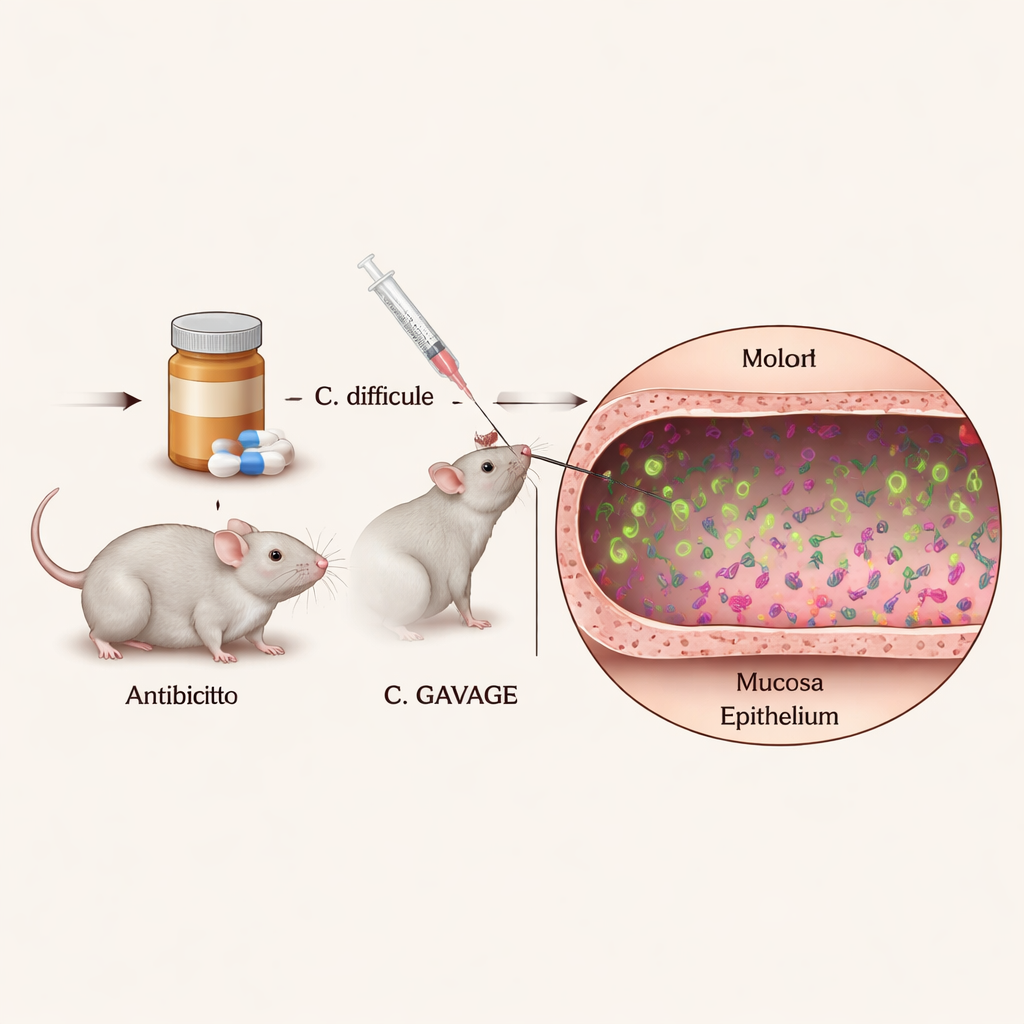
Dove vivono i batteri nel colon
Le immagini hanno mostrato che la maggior parte delle cellule di C. diff vive al centro del contenuto del colon, noto come lume, confermando che l’organismo è principalmente un patogeno “luminale” che galleggia libero. Tuttavia, una minoranza significativa di cellule è apparsa costantemente vicino allo strato mucoso e direttamente adiacente alla superficie epiteliale — il sottile strato di cellule che riveste il colon e funge da barriera verso l’esterno. Questa sottopopolazione a contatto ravvicinato non era stata osservata chiaramente prima nei topi convenzionali con sistemi immunitari normali. È importante sottolineare che i marcatori fluorescenti ingegnerizzati non hanno indebolito in modo evidente i batteri negli animali, il che suggerisce che le immagini riflettono probabilmente il comportamento di C. diff in un’infezione realistica.
Chi produce la tossina, e dove?
Il team ha quindi aggiunto un secondo segnale fluorescente che si attiva solo quando C. diff accende i geni delle tossine. Le tossine sono le proteine dannose che lesionano la mucosa intestinale e causano i sintomi della malattia, ed è anche ciò che i medici dosano nelle analisi delle feci per diagnosticare l’infezione. Sorprendentemente, i batteri non producevano tutti le tossine simultaneamente. Invece, solo una frazione delle cellule si illuminava come “tossina‑ON” in un dato momento, sia nelle fasi precoci sia in quelle tardive dell’infezione. Questa frazione era maggiore in un ceppo mutante geneticamente predisposto a sovraprodurre tossina, ma anche in quel caso non tutte le cellule partecipavano. Ugualmente notevole, la posizione di una cellula — galleggiante nel lume, immersa nel muco o a contatto con l’epitelio — non modificava in modo marcato né la frequenza con cui veniva prodotta tossina né l’intensità con cui quei geni venivano attivati. 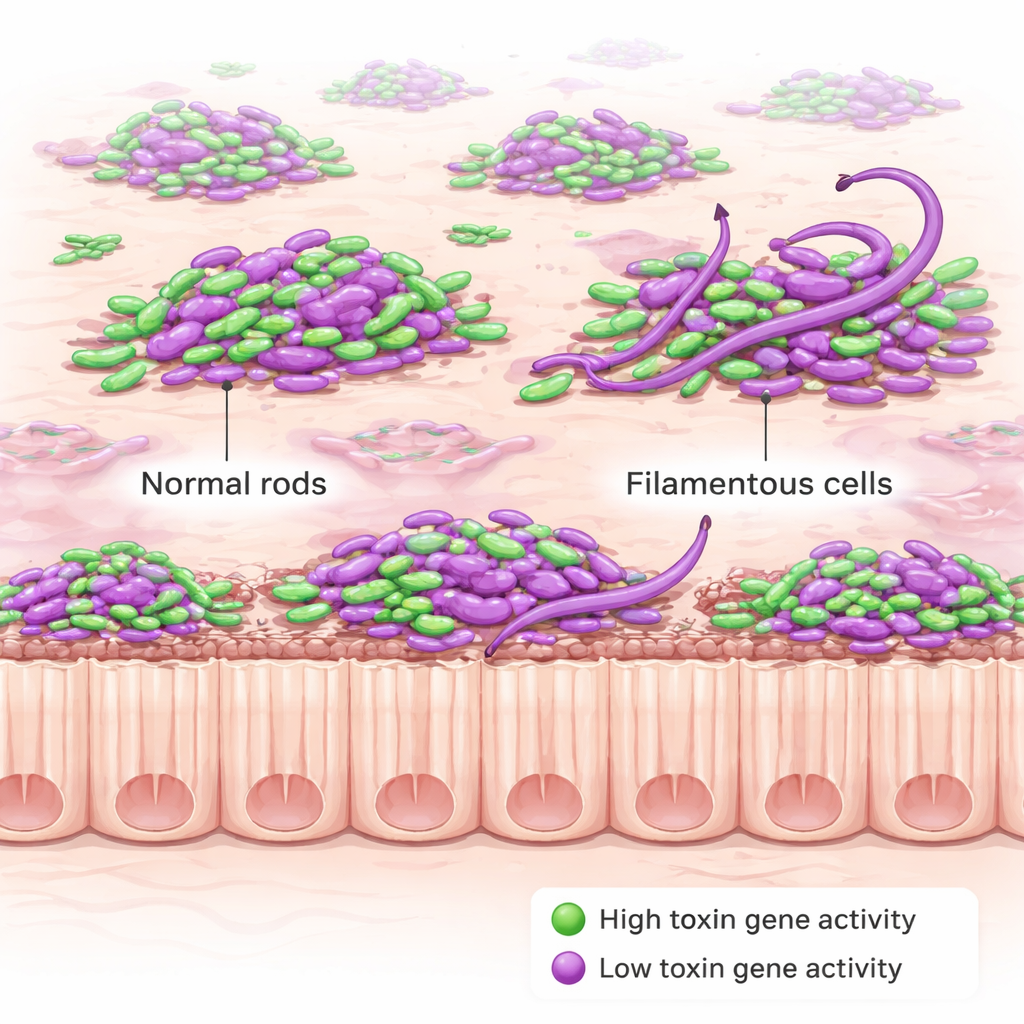
Cellule che cambiano forma sotto stress
Mappando la produzione di tossine, i ricercatori hanno scoperto per caso un comportamento nuovo e sorprendente. Nei topi infettati con il mutante che sovraproduce tossina, molte cellule di C. diff durante la fase acuta della malattia sono diventate filamenti insolitamente lunghi e curvi, alcuni più di dieci volte la lunghezza dei normali bacilli corti. Questa morfologia “a filo” è comparsa prevalentemente nelle fasi iniziali e severe dell’infezione ed è diminuita in seguito; non si è manifestata quando lo stesso ceppo veniva coltivato in brodo di laboratorio. Ciò suggerisce che le condizioni stressanti all’interno dell’intestino infiammato — piuttosto che le sole modifiche genetiche — inneschino questo drastico rimodellamento. Esperimenti successivi hanno mostrato che la perdita di una proteina regolatoria chiamata RstA, che controlla sia i geni delle tossine sia altre risposte allo stress, favorisce la formazione di questi filamenti.
Cosa significa per la malattia da C. diff
Per i non specialisti, il messaggio chiave è che anche un singolo ceppo di C. diff si comporta come una forza lavoro divisa. Alcune cellule sopportano il costo energetico di produrre tossina e danneggiare l’intestino, liberando nutrienti che i loro vicini privi di tossina possono sfruttare. Questa “divisione del lavoro” condivisa può aiutare l’infezione a persistere e a ricomparire, perché non tutte le cellule sono ugualmente vulnerabili ai trattamenti che mirano alle tossine o ai batteri in rapida crescita. Il sistema di reporter fluorescenti appena sviluppato fornisce agli scienziati un modo potente per osservare, cellula per cellula, come C. diff e i microbi intestinali correlati si adattano nel tempo e nello spazio all’interno dell’organismo. Questa conoscenza potrebbe infine guidare terapie non solo mirate a uccidere i batteri, ma a disturbare i ruoli dannosi di particolari sottopopolazioni che guidano malattia e recidiva.
Citazione: DiBenedetto, N.V., Donnelly-Morell, M.L., Kumamoto, C.A. et al. In situ visualization of Clostridioides difficile phenotypic heterogeneity and single-cell morphology during gut infection. Nat Commun 17, 1716 (2026). https://doi.org/10.1038/s41467-026-68411-6
Parole chiave: Clostridioides difficile, microbioma intestinale, tossine batteriche, eterogeneità fenotipica, imaging fluorescente