Clear Sky Science · it
Gli stati delle cellule epiteliali danneggiate influenzano la sopravvivenza dell’allo trapianto renale dopo il rigetto mediato da cellule T
Perché questa ricerca sul rene è importante per i pazienti
I trapianti renali possono salvare la vita, ma molti falliscono anni dopo l’intervento anche quando i medici sembrano aver controllato l’attacco immunitario noto come rigetto mediato da cellule T. Questo studio pone una domanda semplice ma cruciale: se la reazione immunitaria appare “curata” al microscopio, perché alcuni reni trapiantati si deteriorano comunque precocemente? Analizzando le singole cellule di reni trapiantati di topi e di esseri umani, i ricercatori hanno scoperto uno strato nascosto di danno all’interno dei tubuli filtranti del rene che aiuta a spiegare quali innesti sopravvivono e quali no.
Oltre i segni classici del rigetto
I medici di solito diagnosticano il rigetto mediato da cellule T osservando l’invasione del rene da parte di globuli bianchi che attaccano i piccoli tubuli che elaborano l’urina. Farmaci antirigetto potenti possono spesso allontanare queste cellule immunitarie e migliorare l’aspetto della biopsia. Tuttavia i pazienti con questa forma di rigetto restano ad alto rischio di perdita del trapianto. Studi genetici su larga scala avevano già suggerito che i segnali di danno tissutale all’interno delle cellule renali predicono l’esito meglio delle misure del numero di cellule immunitarie presenti. Gli autori hanno voluto definire questi segnali di danno a risoluzione a singola cellula e testare quanto siano legati alla sopravvivenza a lungo termine del trapianto.
Analizzare il rigetto una cellula alla volta
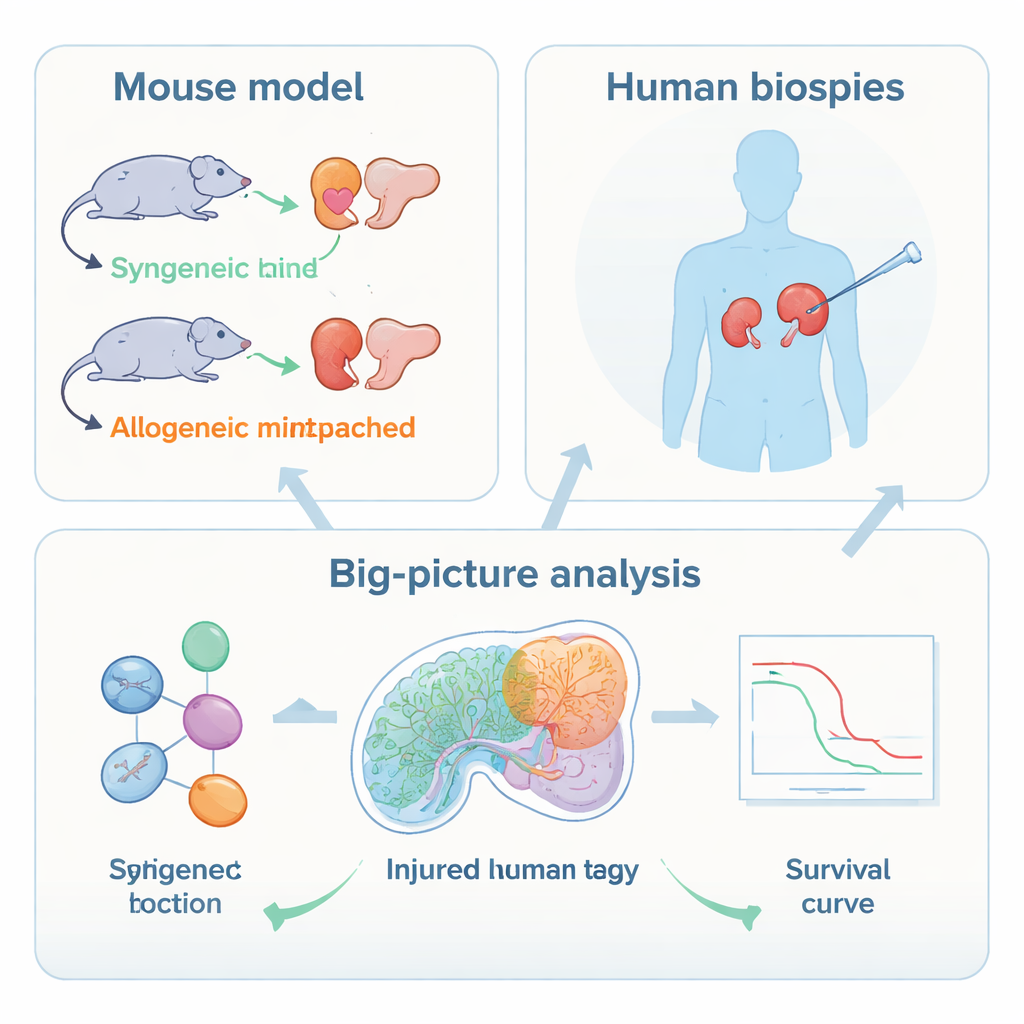
Il gruppo ha prima utilizzato un modello murino controllato, trapiantando reni tra topi geneticamente identici o tra ceppi incompatibili per indurre il rigetto. Hanno poi impiegato il sequenziamento dell’RNA da singolo nucleo, che legge l’attività di migliaia di geni in singole cellule, e la trascrittomica spaziale, che mostra dove quelle cellule sono collocate nel campione tissutale. Questi strumenti hanno rivelato che, durante il rigetto, i cambiamenti molecolari più marcati non avvengono nelle cellule immunitarie ma nelle cellule epiteliali renali che rivestono i tubuli prossimali e un segmento chiamato tratto ascendente spesso. In queste aree le cellule attivano geni di danno e stress, segnali infiammatori e marcatori di uno stato più primitivo e meno specializzato, riducendo al contempo le funzioni di trasporto necessarie per una filtrazione sana.
Nicchie nascoste di cellule tubolari gravemente danneggiate
Raggruppando le cellule in base all’attività genica simile, i ricercatori hanno scoperto diversi “stati di danno” distinti tra le cellule tubolari nei reni dei topi. Alcuni riflettevano risposte di stress precoci, mentre altri rappresentavano cellule gravemente danneggiate e fortemente alterate che avevano perso la normale identità e producevano numerose molecole associate all’infiammazione e alla formazione di cicatrici. La mappatura spaziale ha mostrato che questi stati cellulari non erano distribuiti in modo uniforme: alcuni stati di danno severo formavano nicchie a chiazze nella corteccia renale e nella midollare esterna e si trovavano in complesse vicinanze con cellule T, macrofagi e fibroblasti. Al contrario, alcune cellule danneggiate in regioni più profonde erano sorprendentemente isolate dalle cellule immunitarie, suggerendo modalità diverse con cui il danno può insorgere e persistere.
Mettere in corrispondenza gli stati di danno del topo con i trapianti umani
Gli autori hanno quindi verificato se stati cellulari simili esistessero nell’uomo. Hanno analizzato biopsie di trapianti renali umani con rigetto mediato da cellule T attivo e di innesti stabili. Anche nei dati umani le singole cellule hanno rivelato cellule danneggiate dei tubuli prossimali e del tratto ascendente spesso i cui modelli di espressione genica corrispondevano strettamente agli stati di danno più gravi osservati nei topi. Usando queste firme umane, il team ha “deconvoluto” migliaia di profili di espressione genica di biopsie più vecchie e ha trovato che gli stati tubolari gravemente danneggiati erano più frequenti nel rigetto mediato da cellule T e nel rigetto misto rispetto al rigetto solo anticorpale o all’assenza di rigetto. Importante, hanno costruito insiemi compatti di geni rappresentativi di ciascuno stato di danno e li hanno valutati in una ampia coorte con follow‑up dettagliato.
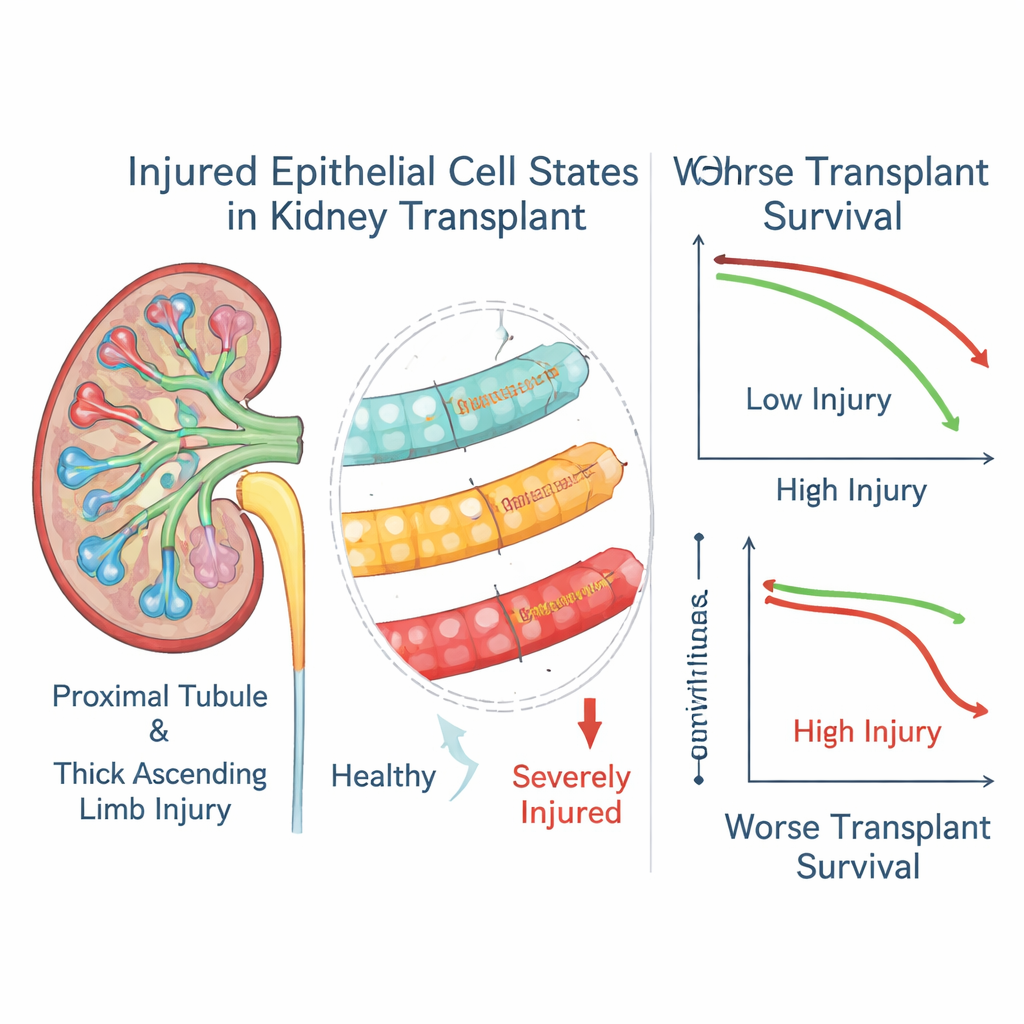
Cellule tubolari danneggiate come predittori del destino del trapianto
Collegando questi punteggi genici agli esiti a tre anni in oltre mille riceventi di trapianto, è emerso un quadro chiaro. Alti livelli di marker per gli stati epiteliali più gravemente danneggiati, sia nei tubuli prossimali sia nel tratto ascendente spesso, erano fortemente associati a una maggiore probabilità di perdita del trapianto, anche tra i pazienti le cui biopsie erano altrimenti classificate come rigetto trattato. Uno stato di danno tubulare più lieve mostrava la tendenza opposta ed era legato a una migliore sopravvivenza, suggerendo che potrebbe rappresentare un programma di riparazione più efficace. In un sottogruppo di pazienti con biopsie ripetute, i punteggi di “danno severo” spesso restavano elevati a lungo dopo che l’episodio di rigetto sembrava risolto, il che implica che queste cellule alterate possono persistere e continuare a influenzare la malattia.
Cosa significa per la cura dei trapianti
Per i non specialisti, il messaggio chiave è che non tutto il danno in un rene rigettato deriva direttamente dalle cellule immunitarie, e non tutto il danno scompare quando l’attacco immunitario si placa. Questo studio dimostra che nicchie persistenti di cellule tubolari gravemente danneggiate fungono da sistema di allerta precoce per un futuro fallimento dell’innesto. A lungo termine, test semplici basati su queste firme geniche di danno—possibilmente anche utilizzando cellule eliminate con le urine—potrebbero aiutare i medici a identificare i pazienti ad alto rischio, personalizzare i trattamenti e monitorare se i reni si riprendono davvero. Il lavoro indica inoltre che le stesse cellule epiteliali danneggiate potrebbero essere target per nuove terapie volte a proteggere i trapianti renali oltre la sola immunosoppressione standard.
Citazione: Pfefferkorn, A.M., Jahn, L., Gauthier, P.T. et al. Injured epithelial cell states impact kidney allograft survival after T-cell-mediated rejection. Nat Commun 17, 1060 (2026). https://doi.org/10.1038/s41467-026-68397-1
Parole chiave: rigetto di trapianto renale, danno delle cellule tubolari, sequenziamento a singola cellula, sopravvivenza del trapianto, stati delle cellule epiteliali