Clear Sky Science · it
La modellizzazione del metabolismo tessuto-specifico in Drosophila identifica la disgregazione metabolica indotta da una dieta ricca di zuccheri nel muscolo a livello di reazioni e vie
Perché questo studio sulla mosca della frutta è importante per la salute umana
Un eccesso di zucchero nella nostra dieta può mettere sotto pressione la capacità dell’organismo di gestire i combustibili, contribuendo nel tempo allo sviluppo del diabete di tipo 2. Questo studio utilizza la mosca della frutta per mettere in luce, con grande dettaglio, come i diversi tessuti gestiscono il metabolismo e come una dieta ricca di zuccheri comprometta la funzione muscolare. Poiché le mosche condividono molti geni metabolici e sistemi d’organo con gli esseri umani, questi risultati aiutano a spiegare cosa potrebbe andare storto nei nostri muscoli in caso di sovraccarico zuccherino prolungato.
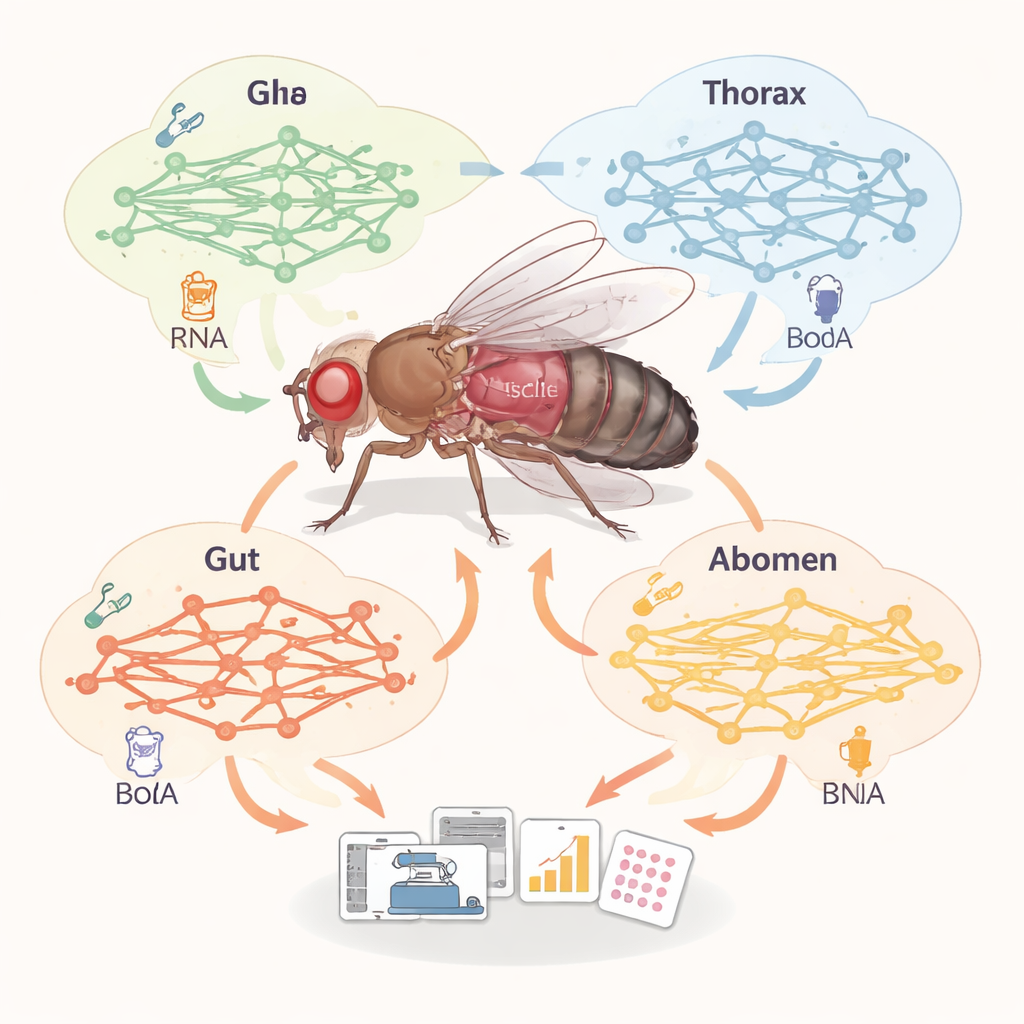
Mappare il metabolismo tessuto per tessuto
I nostri corpi, come quelli delle mosche, sono costituiti da tessuti che svolgono ruoli metabolici molto diversi: il muscolo brucia combustibile, il tessuto adiposo lo immagazzina, l’intestino elabora il cibo, e così via. Invece di misurare ogni enzima direttamente, i ricercatori hanno costruito ampie “mappe” del metabolismo—chiamate modelli metabolici su scala genomica—per 32 tessuti distinti della mosca. Hanno combinato una rete di reazioni chimiche esistente e curata con dati di espressione genica a singola cellula, che indicano quali geni metabolici sono attivi in ciascun tessuto. Questo ha permesso di confrontare quante reazioni, metaboliti e geni sono attivi in ogni rete tessuto-specifica e di vedere quali vie sono privilegiate nel muscolo, nel corpo adiposo, nell’intestino e in diversi tipi di cellule nervose.
Ruoli energetici distinti per organi diversi
Il confronto ha rivelato chiare “personalità” metaboliche tra i tessuti. Il corpo adiposo e le oenociti—controparti della mosca del tessuto adiposo e del fegato umano—contenevano il set più ricco di reazioni, in particolare quelle che ossidano i grassi tramite beta-ossidazione. Il muscolo, al contrario, non aveva la rete più ampia, ma presentava la frazione più alta di reazioni che muovono sostanze dentro e fuori dalle cellule, suggerendo che il muscolo è un importante nodo per lo scambio di combustibili e mattoni con il resto dell’organismo. Gli scienziati hanno inoltre verificato se le vie predette corrispondessero ai reali schemi di metaboliti misurati in diverse regioni corporee. Usando la metabolomica mirata, hanno analizzato centinaia di piccole molecole da teste, toraci, intestini e addomi delle mosche e poi hanno verificato se le vie arricchite nei dati si sovrapponessero a quelle predette dai modelli. In muscolo e corpo adiposo la corrispondenza è stata forte, dando fiducia che i modelli tessuto-specifici catturassero la biologia reale meglio della sola espressione genica.
Cosa fa una dieta ricca di zucchero al flusso energetico muscolare
Con un modello muscolare validato a disposizione, il team ha simulato cosa accade quando le mosche sono alimentate con una dieta a lungo termine ricca di zuccheri, un modello ben consolidato del diabete di tipo 2. Hanno vincolato il modello usando caratteristiche note del muscolo diabetico, come la ridotta captazione del glucosio e l’attività rallentata del ciclo energetico centrale nei mitocondri. Analisi computazionali di “flusso”—calcoli della velocità con cui le reazioni possono procedere—hanno mostrato riduzioni diffuse nelle reazioni che dipendono dalla coppia redox NAD/NADH, molecole che trasportano elettroni ed sono essenziali per la produzione di energia. In particolare, le reazioni della via centrale di ossidazione degli zuccheri, la glicolisi, si sono rallentate, comprese quelle catalizzate dall’enzima GAPDH. Il modello ha anche previsto una riduzione di circa un quarto nella capacità complessiva del muscolo di produrre NADH, suggerendo uno squilibrio redox sotto stress. Misurazioni dirette nel muscolo toracico delle mosche hanno confermato che il rapporto NAD/NADH effettivamente diminuiva sotto una dieta ricca di zuccheri.
Seguire zucchero etichettato e proteine ossidate
Per verificare se questi colli di bottiglia predetti si verificassero davvero negli animali vivi, i ricercatori hanno alimentato le mosche con una dieta ricca di zuccheri contenente glucosio uniformemente etichettato con carbonio-13 e poi hanno tracciato dove andava il carbonio etichettato. Hanno osservato che gli intermedi glicolitici precoci a monte di GAPDH si accumulavano, mentre i prodotti a valle e le loro frazioni etichettate diminuivano, segnalando un rallentamento reale a partire da questo punto e oltre. Analogamente, il contributo del carbonio del glucosio al ciclo energetico centrale è risultato ridotto. Allo stesso tempo, la proteomica redox—una tecnica che rileva modifiche ossidative su specifici aminoacidi nelle proteine—ha mostrato un aumento dell’ossidazione di molti enzimi glicolitici, inclusi più siti su GAPDH. Lungo tutta la glicolisi, gli enzimi che mostravano più modifiche ossidative tendevano a presentare cali maggiori nel flusso predetto, anche se i loro livelli proteici complessivi restavano per lo più invariati. Ciò suggerisce che il danno chimico dovuto allo stress ossidativo, piuttosto che la perdita di abbondanza degli enzimi, sia un fattore chiave dell’impairment nella lavorazione degli zuccheri nel muscolo.
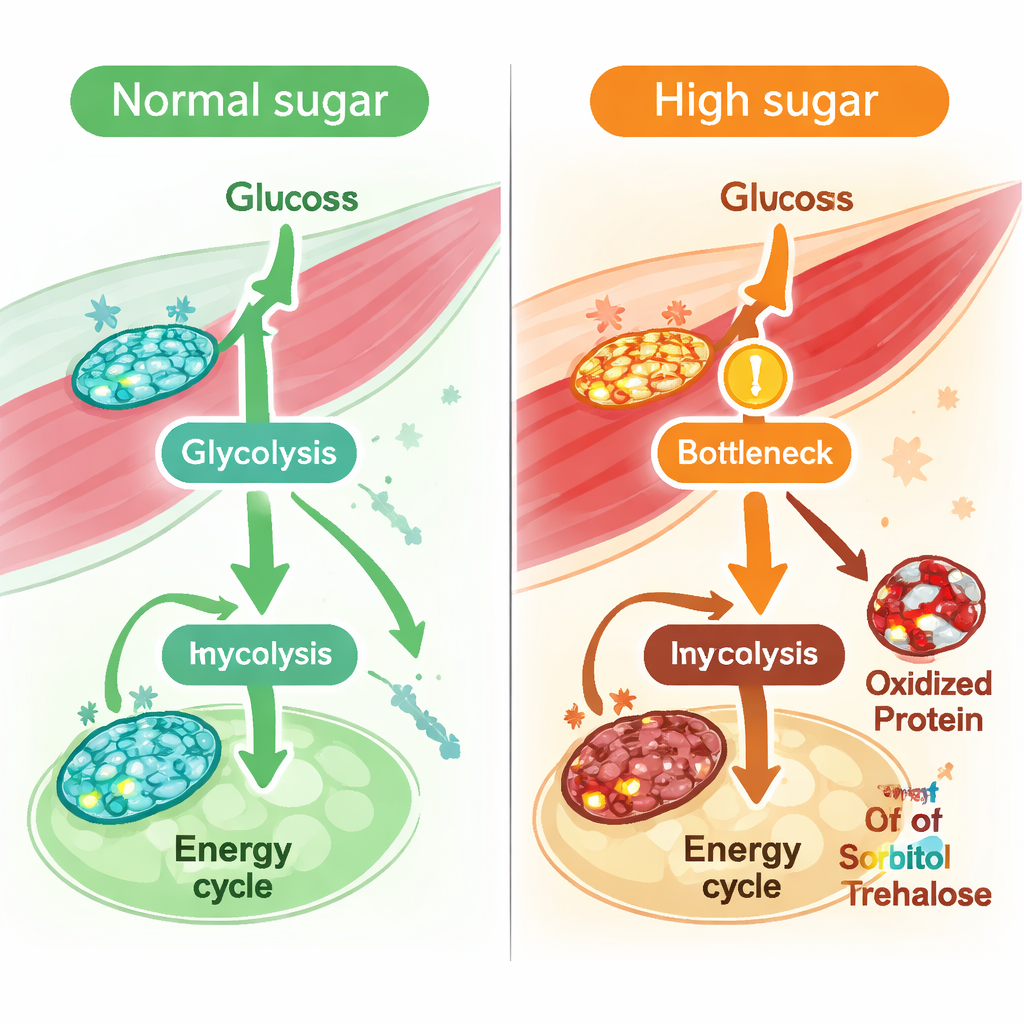
Problemi nascosti nella gestione di fruttosio e saccarosio
Guardando oltre singole reazioni, il team ha mediato i flussi attraverso intere vie per vedere quali fossero più perturbate dallo zucchero elevato. Glicolisi, ciclo energetico e fosforilazione ossidativa hanno mostrato tutti cali, ma una delle diminuzioni predette più marcate riguardava il metabolismo del fruttosio. Il profilo dei metaboliti nel muscolo ha supportato questa idea: i livelli di sorbitolo e trealosio/saccarosio sono aumentati, e un enzima chiave che converte la trealosio in glucosio, la trealasi, ha mostrato sia una ridotta attività predetta sia un’aumentata ossidazione in un residuo metionina sensibile. Nel complesso, questi risultati indicano un disturbo più ampio nella gestione degli zuccheri dietetici da parte del muscolo—in particolare dei combustibili derivati da fruttosio e saccarosio—sotto un sovraccarico zuccherino cronico.
Cosa significa per la comprensione del diabete
In termini semplici, questo lavoro mostra che troppo zucchero non solo sovraccarica il flusso sanguigno; rimodella silenziosamente anche il modo in cui le cellule muscolari instradano e bruciano il carburante. Costruendo mappe metaboliche dettagliate e tessuto-specifiche per la mosca della frutta e verificandole con metabolomica, tracciamento isotopico e proteomica redox, i ricercatori dimostrano che l’elevato apporto di zuccheri guida lo stress redox, ossida enzimi glicolitici chiave come GAPDH, rallenta la degradazione degli zuccheri e altera le vie legate al fruttosio. Questi approfondimenti, ottenuti in un organismo modello altamente maneggevole, offrono un quadro potente per individuare quali reazioni e vie potrebbero essere più importanti da proteggere o ripristinare nel muscolo umano per prevenire o trattare il diabete di tipo 2.
Citazione: Moon, S.J., Hu, Y., Dzieciatkowska, M. et al. Modeling tissue-specific Drosophila metabolism identifies high sugar diet-induced metabolic dysregulation in muscle at reaction and pathway levels. Nat Commun 17, 1692 (2026). https://doi.org/10.1038/s41467-026-68395-3
Parole chiave: Metabolismo di Drosophila, modelli metabolici tessuto-specifici, dieta ricca di zuccheri, glicolisi muscolare, regolazione redox