Clear Sky Science · it
OCT4 aumenta l’efficienza di attivazione delle origini di replicazione tardive nelle cellule staminali embrionali di topo
Perché questo è importante per le nostre cellule
Ogni volta che una cellula si divide deve copiare con accuratezza e nei tempi giusti l’intero DNA. Se questo processo di copiatura fallisce, può portare a problemi dello sviluppo o a malattie, compreso il cancro. Questo studio analizza come una proteina chiave delle cellule staminali, OCT4, contribuisca a organizzare quando e dove inizia la duplicazione del DNA nelle cellule staminali embrionali di topo—offrendo una finestra su come gli embrioni precoci mantengono stabile il loro genoma mentre si dividono a velocità elevata.
Mappare quando il DNA viene copiato
Gli autori si concentrano sulla “tempistica della replicazione”—l’ordine con cui diverse parti del genoma vengono duplicate durante la fase S del ciclo cellulare. Il genoma è suddiviso in grandi quartieri, o domini temporali, che vengono copiati presto, a metà o tardi nella fase S. Utilizzando metodi di sequenziamento ad alto rendimento che marcano il DNA appena sintetizzato, il gruppo ha tracciato il paesaggio della tempistica di replicazione nelle cellule staminali embrionali di topo e lo ha confrontato con quello di tipi cellulari più maturi, come fibroblasti e cellule staminali mesenchimali. Hanno identificato migliaia di “zone di inizio”, tratti di DNA dove la replicazione ha effettivamente inizio, e le hanno classificate come precoci, medie o tardive in base al dominio temporale in cui ricadono.
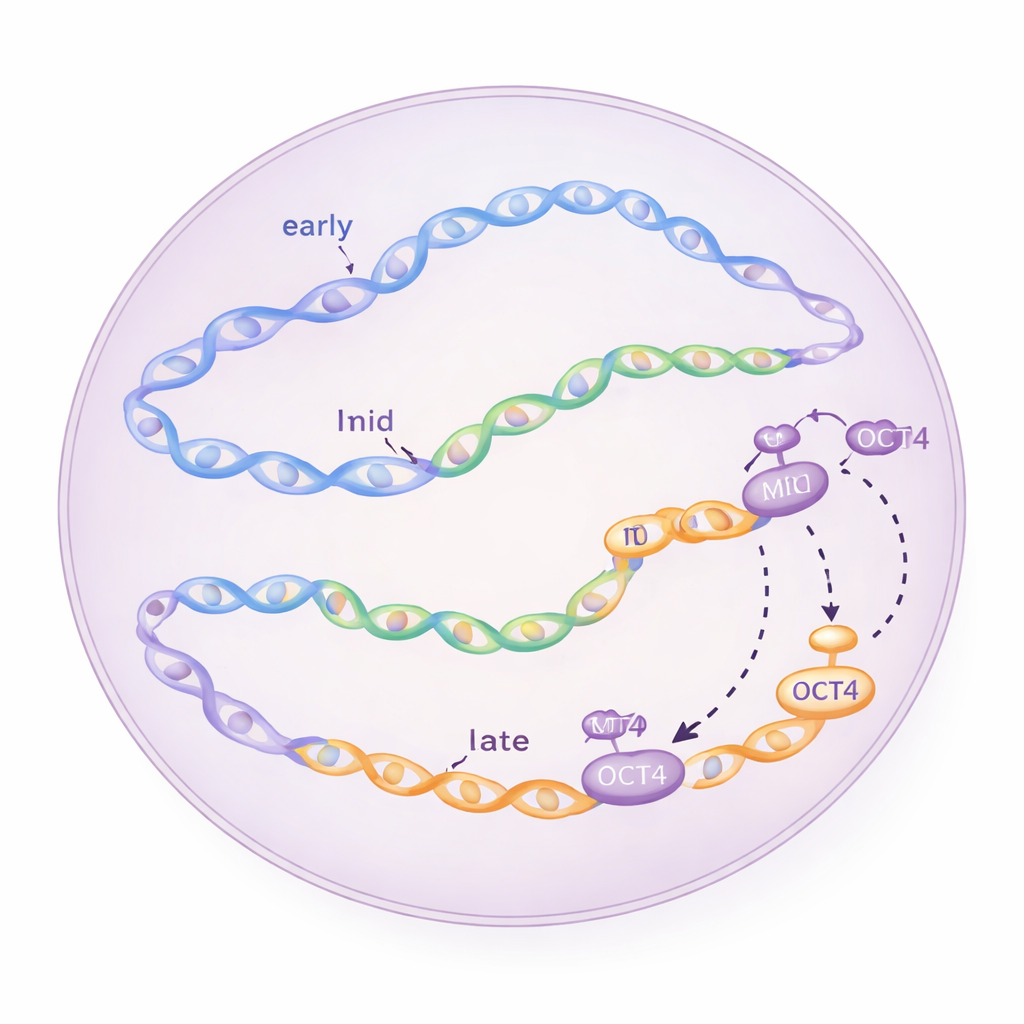
Starter tardivi che saltano la coda
La saggezza convenzionale sostiene che le regioni programmate per la replicazione tardiva aspettino in gran parte fino alla fine della fase S per iniziare la copiatura. Sorprendentemente, nelle cellule staminali embrionali i ricercatori hanno osservato che alcune zone di inizio collocate in domini tardivi cominciano ad attivarsi molto poco dopo l’inizio della fase S—entro solo una o due ore. Sincronizzando le cellule in diverse fasi del ciclo cellulare e acquisendo ripetutamente istantanee del DNA appena sintetizzato, hanno confermato che queste zone “tardive” si attivano davvero precocemente e che la loro attività dipende da regolatori standard del ciclo cellulare come le chinasi CDC7 e CDK1, oltre che dalla via di checkpoint ATR, che normalmente aiuta a prevenire il sovraccarico della macchina di replicazione.
Quartieri di DNA aperto e il ruolo di OCT4
Per capire cosa renda speciali queste insolite regioni tardive che si attivano presto, il gruppo ha esaminato il loro ambiente locale. Ha sovrapposto le mappe di replicazione con dati sulla produzione di RNA e sui marchi della cromatina—tag chimici e caratteristiche strutturali che indicano se il DNA è in uno stato aperto e accessibile o compattato. Le zone di inizio precoci tendevano a trovarsi vicino a geni attivi e cromatina aperta, mentre le zone tardive erano più spesso in regioni represse e compattate. Tuttavia, le particolari zone tardive che si attivavano presto nelle cellule staminali embrionali mostravano segnali di apertura: coincidevano con cromatina accessibile, elementi simili a enhancer e siti di legame per fattori di pluripotenza come OCT4, SOX2, NANOG e KLF4. Ciò suggerisce che le stesse proteine che mantengono flessibile il destino delle cellule staminali possano anche preparare specifiche regioni tardive del genoma a una replicazione anticipata.
Spegnere OCT4 sposta il programma
Gli autori hanno poi messo alla prova quest’idea usando una linea staminale speciale in cui i livelli di OCT4 possono essere rapidamente ridotti aggiungendo il farmaco doxiciclina. Quando OCT4 è stato deplezionato per solo una parte di un singolo ciclo cellulare, l’ingresso complessivo nella fase S è rimasto in gran parte invariato, ma l’attivazione di molte zone di inizio medio e tardivo è risultata indebolita o ritardata. Analisi a livello genomico hanno mostrato che, nelle regioni dove OCT4 normalmente si lega, sia l’accessibilità della cromatina sia i segnali di inizio della replicazione diminuiscono in parallelo quando OCT4 viene spento. La modellizzazione statistica ha confermato che questo effetto è più forte nelle zone a replicazione tardiva: più una zona di inizio dipendeva da OCT4 per mantenere la cromatina aperta, maggiore era il calo della sua efficienza di replicazione in assenza di OCT4.
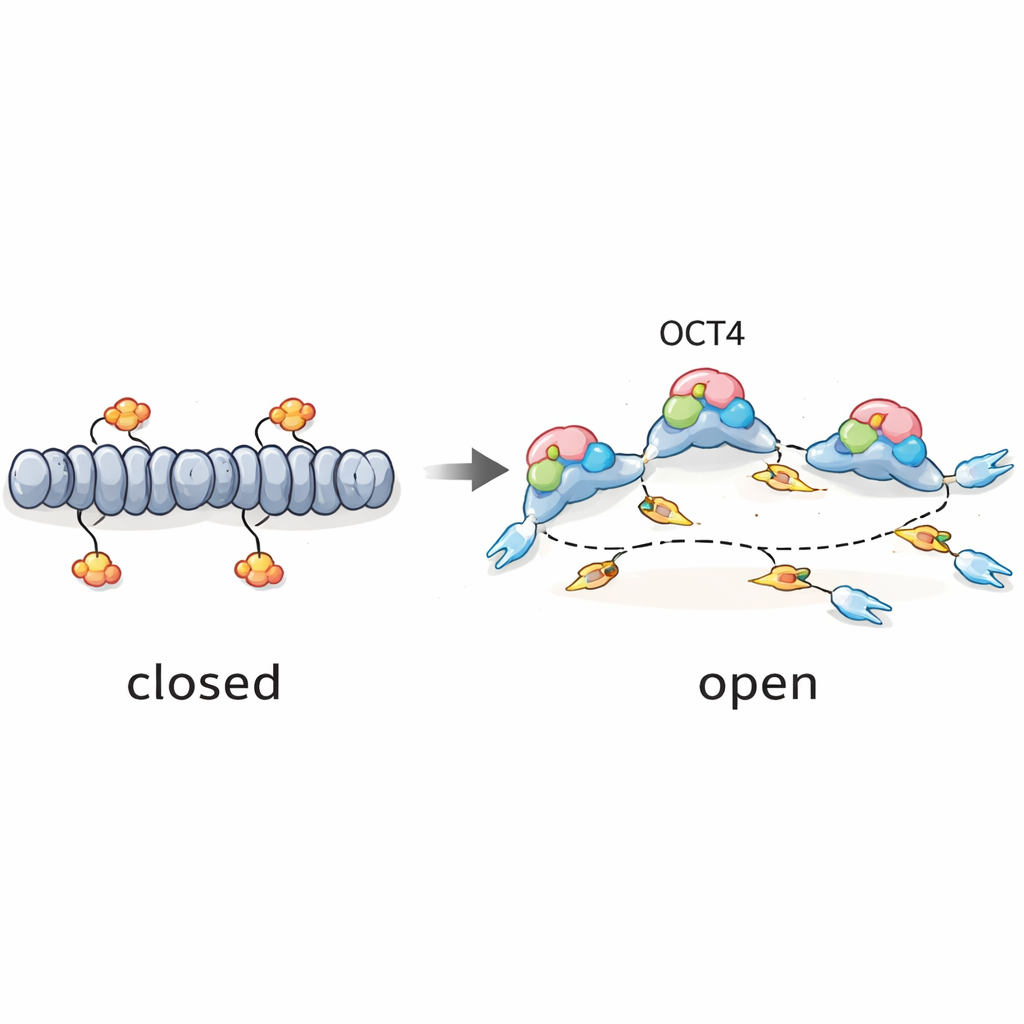
Un fattore pione che regola anche la tempistica della replicazione
Nel loro insieme, i risultati supportano un’idea semplice: OCT4 agisce come un fattore “pioniere” non solo per l’attività genica, ma anche per la replicazione del DNA. Aprendo specifiche regioni tardive del genoma nelle cellule staminali embrionali, OCT4 crea punti di partenza per la copiatura del DNA che possono attivarsi prima e in modo più affidabile rispetto a quanto avverrebbe nelle cellule differenziate. Allo stesso tempo, regolatori globali come ATR, CDC7 e CDK1 modulano quanti di questi siti possono essere attivati, impedendo che il sistema di replicazione venga sovraccaricato. Per il lettore non specialistico, il messaggio chiave è che le stesse proteine che mantengono versatili le cellule staminali contribuiscono anche a orchestrare quando vengono copiate le diverse parti del loro DNA, aggiungendo un ulteriore livello alla nostra comprensione di come le cellule embrionali che si dividono rapidamente mantengano ordine nel loro genoma.
Citazione: Rodriguez-Carballo, E., Dionellis, V.S., Ntallis, S.G. et al. OCT4 enhances the firing efficiency of late DNA replication origins in mouse embryonic stem cells. Nat Commun 17, 1686 (2026). https://doi.org/10.1038/s41467-026-68389-1
Parole chiave: tempistica della replicazione del DNA, cellule staminali embrionali, OCT4, accessibilità della cromatina, attivazione dell’origine