Clear Sky Science · it
Ringiovanimento meccanico delle cellule staminali senescenti e delle ossa invecchiate tramite rimodellamento della cromatina
Perché mantenere le ossa giovani è importante
Con l’avanzare dell’età, le nostre ossa perdono gradualmente forza, diventando più sottili e fragili. Questo aumenta il rischio di fratture, la perdita di autonomia e il dolore cronico. La maggior parte dei trattamenti attuali si concentra su farmaci che rallentano la degradazione ossea o aggiungono minerali, ma non riparano direttamente l’invecchiamento delle cellule staminali che costruiscono l’osso. Questo studio esplora un approccio diverso: utilizzare forze fisiche accuratamente controllate — piuttosto che medicine — per “ringiovanire” le cellule staminali osteogeniche invecchiate e migliorare la salute ossea e il livello di fitness complessivo nei topi anziani.
Quando i costruttori dell’osso invecchiano
Nel profondo delle nostre ossa risiedono le cellule staminali mesenchimali del midollo osseo, i principali artefici che possono trasformarsi in cellule che formano l’osso. Con l’età queste cellule staminali si dividono meno, formano meno tessuto osseo e mostrano i segni classici dell’invecchiamento cellulare, come danni al DNA e segnali infiammatori. I ricercatori hanno confrontato cellule provenienti da donatori umani giovani e anziani e hanno rilevato che le cellule staminali invecchiate non erano soltanto diverse dal punto di vista biochimico: erano anche meccanicamente più deboli. Generavano meno forza interna, avevano impalcature interne più flosce e mostravano una peggiore trasmissione dei segnali meccanici verso il nucleo cellulare. Nel tessuto osseo di topi anziani emerse un declino simile: il reticolo di osso spugnoso era assottigliato, proteine chiave per la segnalazione meccanica erano ridotte e i marcatori dell’invecchiamento risultavano elevati.
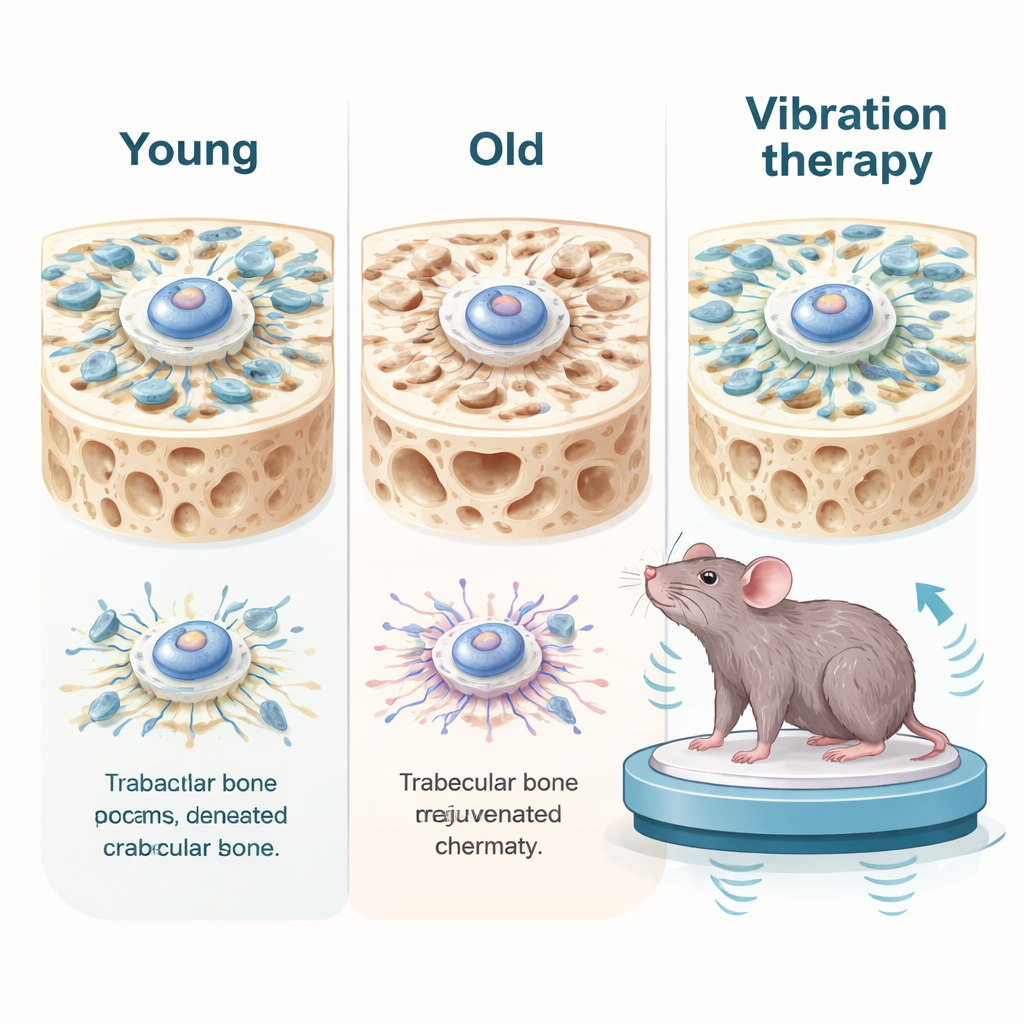
Tirare delicatamente le cellule verso la giovinezza
Il gruppo si è quindi chiesto se il ripristino della forza meccanica potesse invertire questi segni di invecchiamento. In colture, hanno applicato un lieve stiramento alle cellule staminali senescenti o hanno usato un farmaco che aumenta l’attività dei motori molecolari. Questi trattamenti hanno rafforzato le forze di trazione cellulari e migliorato l’organizzazione dell’impalcatura interna. Sorprendentemente, le cellule invecchiate hanno cominciato ad apparire e comportarsi da più giovani: i marcatori di senescenza sono diminuiti, i danni al DNA si sono ridotti e le cellule si sono moltiplicate più facilmente. È valso anche il contrario: quando hanno ammorbidito l’ambiente sotto cellule giovani o indebolito chimicamente il loro apparato contrattile, le cellule sono scivolate in uno stato simile all’invecchiamento, rallentando e attivando marcatori di età anche in un gel 3D che riproduce l’osso.
Come la forza parla ai geni
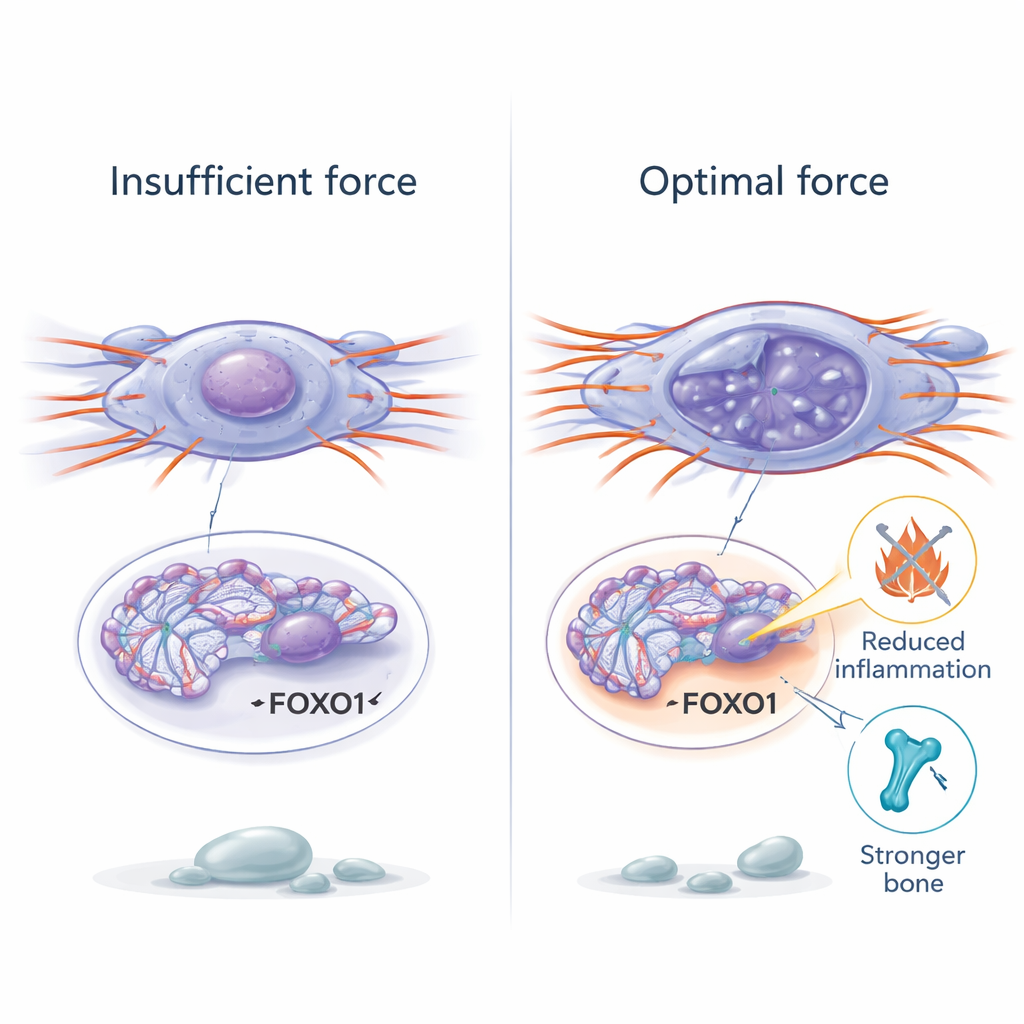
Per capire come le forze fisiche potessero modificare così profondamente il comportamento cellulare, i ricercatori si sono concentrati sulla cromatina — la forma impacchettata del DNA all’interno del nucleo. Nelle cellule staminali anziane la cromatina era più condensata e meno accessibile, rendendo più difficile l’attivazione di geni benefici. Il ripristino della forza meccanica ha causato un rilassamento locale della cromatina, aumentando i marchi chimici associati al DNA aperto e attivo. Tramite un’analisi dell’accessibilità della cromatina su scala genomica, il team ha scoperto che una delicata stimolazione meccanica apriva regioni vicino a geni coinvolti nel controllo dell’invecchiamento. Un gene, chiamato FOXO1, è emerso come particolarmente sensibile alla forza. Quando la forza aumentava, la regione del DNA di FOXO1 si rendeva più accessibile, la sua attività saliva e le cellule diventavano meno senescenti. Bloccare FOXO1 annullava i benefici della stimolazione meccanica, rivelandolo come un interruttore chiave che collega la sollecitazione fisica ai programmi genetici di resilienza e riparazione.
Trovare il punto giusto per la terapia meccanica
I ricercatori hanno quindi testato la stimolazione meccanica su topi viventi. Gli animali anziani sono stati posti su una piattaforma a vibrazione a bassa intensità per brevi sessioni quotidiane per un mese, mentre altri hanno subito il carico ridotto degli arti posteriori mediante sospensione per la coda, mimando un’inattività estrema. Nei topi anziani la vibrazione delicata ha aumentato la segnalazione meccanica nell’osso, ridotto i marcatori di invecchiamento e infiammazione e parzialmente ricostruito il reticolo di osso spugnoso. Ha inoltre migliorato la forza di presa, la resistenza all’esercizio, le prestazioni in compiti legati alla memoria e ridotto l’infiammazione nel sangue, nel fegato e nei reni. Tuttavia, quando la vibrazione veniva applicata in modo continuativo senza giorni di riposo, i benefici scomparivano e persino si invertivano: la struttura ossea peggiorava, i danni al DNA aumentavano e l’infiammazione saliva. In studi su cellule, stiramenti eccessivamente forti o frequenti provocavano rotture del DNA e riportavano le cellule in senescenza, dimostrando che la forza meccanica può guarire o danneggiare a seconda della dose.
Da imitazioni dell’esercizio a possibili terapie future
Per un lettore non specialista, il messaggio centrale è che le nostre cellule non rispondono solo a ormoni e sostanze chimiche: «ascoltano» anche da vicino le forze fisiche. In questo lavoro gli autori mostrano che una stimolazione meccanica moderata e ben calibrata può risvegliare le cellule staminali ossee invecchiate, attivare programmi genetici protettivi come FOXO1, ricostruire l’osso indebolito e calmare l’infiammazione cronica nei topi anziani. Allo stesso tempo, troppo poca o troppa forza accelera l’usura cellulare. Questi risultati suggeriscono che terapie meccaniche disegnate con cura — forse specifici regimi di esercizio o dispositivi sicuri a base di vibrazione — potrebbero un giorno affiancare i farmaci per mantenere le ossa, e possibilmente altri tessuti, più sani più a lungo.
Citazione: Liu, X., Ye, Y., Li, Z. et al. Mechanical rejuvenation of senescent stem cells and aged bone via chromatin remodeling. Nat Commun 17, 1684 (2026). https://doi.org/10.1038/s41467-026-68387-3
Parole chiave: invecchiamento delle ossa, stimolazione meccanica, ringiovanimento delle cellule staminali, rimodellamento della cromatina, FOXO1