Clear Sky Science · it
Escissione precisa delle ripetizioni GGC amplificate in NOTCH2NLC mediante CRISPR/Cas9 per il trattamento della malattia delle inclusioni intranucleari neuronali
Modificare il DNA per affrontare un misterioso disturbo cerebrale
La malattia delle inclusioni intranucleari neuronali (NIID) è un disturbo cerebrale raro ma devastante che può provocare demenza, problemi di movimento e persino morte precoce. Attualmente non esiste una cura. Questo studio esplora se un potente strumento di editing genico, CRISPR, possa essere usato per asportare un tratto di DNA piccolo ma tossico che porta alla NIID, offrendo uno sguardo su come trattamenti futuri potrebbero riscrivere i nostri geni per combattere le malattie cerebrali. 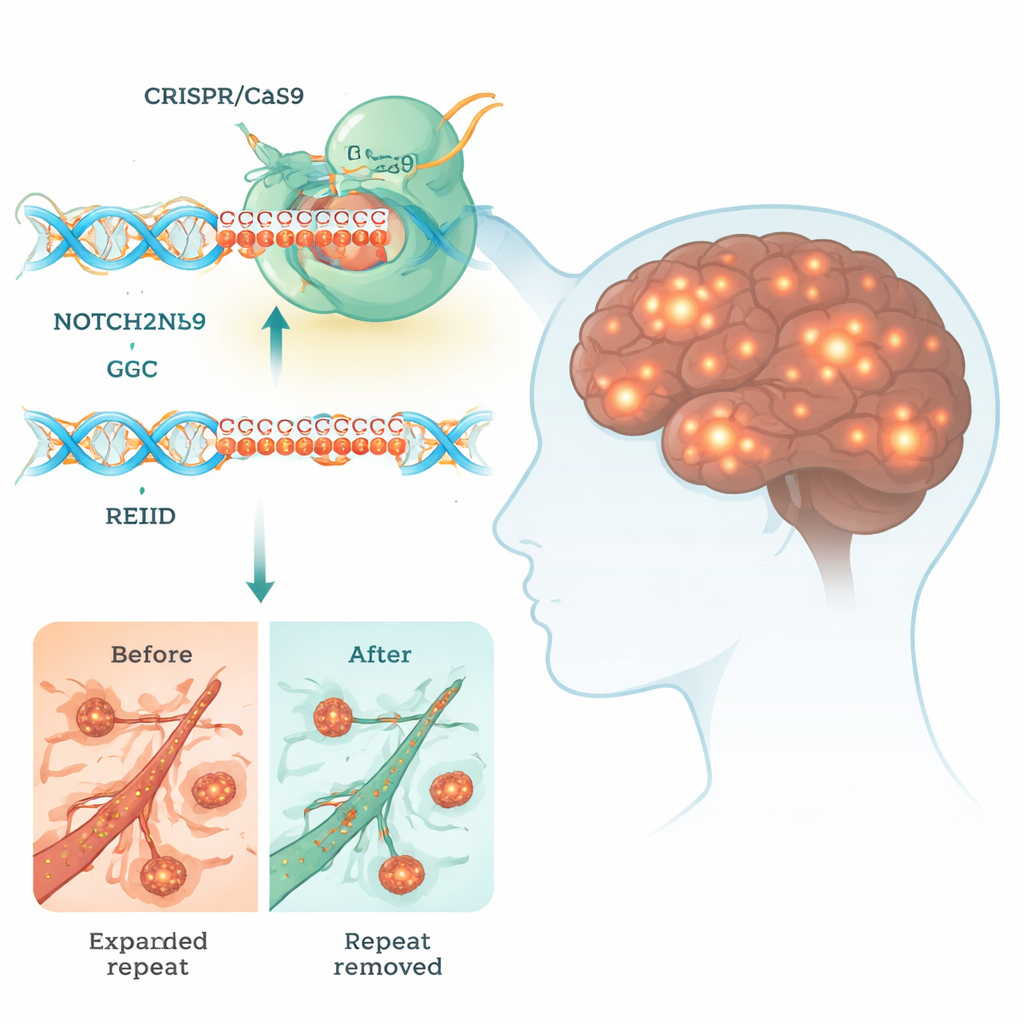
Un colpevole genetico nascosto
Molti disturbi cerebrali ereditari sono causati da brevi sequenze di DNA che si sono allungate ben oltre la loro lunghezza normale. Nella NIID, il problema è una corsa sovradimensionata di unità di tre lettere del DNA, «GGC», in un gene chiamato NOTCH2NLC. Sebbene questo tratto si trovi in una regione che non codifica direttamente per una proteina classica, può comunque essere letto dalla macchina cellulare per produrre catene anomale di poliglicina (polyG). Queste catene appiccicose si aggregano in ammassi all’interno del nucleo delle cellule nervose e di altri tessuti, perturbando processi vitali come la produzione di energia, l’elaborazione dell’RNA e il traffico di molecole tra nucleo e citoplasma.
La sfida della chirurgia genica precisa
Progettare un trattamento di editing genico per la NIID è particolarmente difficile perché NOTCH2NLC ha diverse geni «sorella» quasi identici che sono importanti per lo sviluppo del cervello umano. Se CRISPR taglia quello sbagliato, potrebbe fare più danno che bene. I ricercatori hanno esaminato attentamente il DNA attorno alla ripetizione GGC e hanno trovato piccole differenze di sequenza che distinguono NOTCH2NLC dai suoi parenti. Hanno quindi progettato coppie di RNA guida CRISPR che indirizzano le «forbici molecolari» Cas9 a tagliare subito prima e subito dopo la ripetizione espansa. Questa strategia a doppio taglio permette al sistema di riparazione cellulare di rimuovere il segmento tossico lasciando intatto il resto della famiglia genica.
Dalle cellule in coltura ai neuroni derivati da pazienti
Il team ha prima testato il progetto CRISPR in cellule umane standard e in cellule ingegnerizzate per contenere una grande ripetizione di NOTCH2NLC. In questi modelli, l’editor ha efficacemente eliminato la ripetizione e i livelli di ammassi di polyG sono diminuiti di circa la metà o più. Hanno poi utilizzato cellule staminali pluripotenti indotte (iPSC) derivate da un paziente con NIID e le hanno convertite in cellule progenitrici neuronali, uno stadio precoce delle cellule cerebrali. Usando CRISPR, hanno o cancellato la ripetizione espansa o l’hanno sostituita con una versione di lunghezza normale. Sequenziamento dettagliato del DNA e dell’intero genoma ha mostrato che l’editing era altamente accurato, con poche evidenze di tagli indesiderati, e le cellule modificate continuavano a dividersi e maturare normalmente. 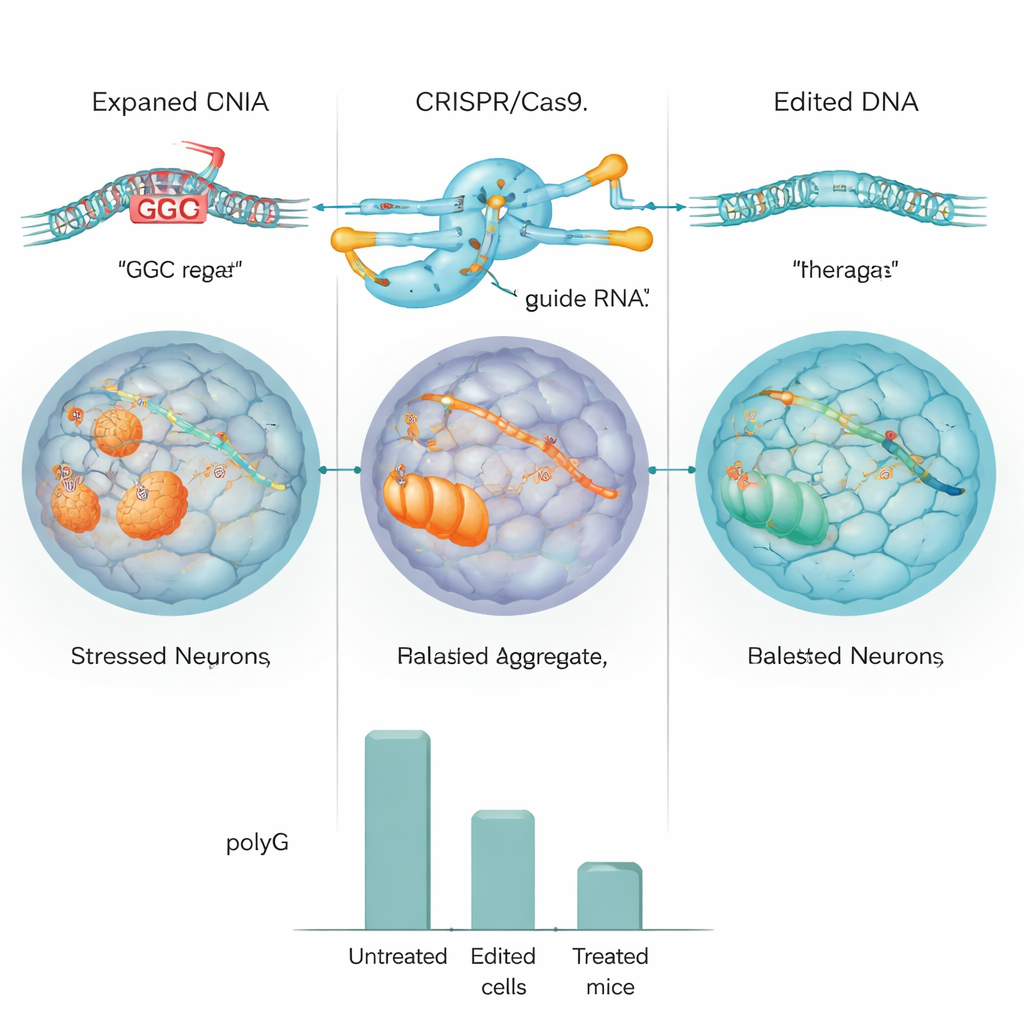
Ripristinare cervello e organismo in un modello murino
Per valutare se questo approccio potesse effettivamente migliorare la malattia, i ricercatori si sono rivolti a topi ingegnerizzati per portare la ripetizione umana di NOTCH2NLC e sviluppare caratteristiche simili alla NIID, incluse inclusioni nucleari, problemi di movimento e vita accorciata. Hanno confezionato il sistema CRISPR in un virus modificato in grado di diffondersi nel cervello dopo una semplice iniezione nel flusso sanguigno dei topi neonati. Negli animali trattati la ripetizione espansa è stata rimossa con successo nel tessuto cerebrale. Di conseguenza, i livelli tossici di polyG sono calati drasticalmente, i marcatori di salute dei neuroni sono migliorati e si è attenuata l’attivazione anomala delle cellule di supporto cerebrali. I test comportamentali hanno mostrato che i topi trattati si muovevano di più, mantenevano meglio l’equilibrio e vivevano più a lungo rispetto ai fratelli non trattati. Benefici simili sono stati osservati nel cuore, che in questo modello accumula anch’esso polyG.
Cosa potrebbe significare per i trattamenti futuri
Per un lettore non specialista, il messaggio principale è che la NIID sembra essere guidata in gran parte da una specifica ripetizione di DNA ingrandita e che rimuovere con precisione quella ripetizione può invertire molti segni della malattia nelle cellule e nei topi. Questo lavoro non si traduce ancora in una terapia pronta per l’uso umano: i ricercatori devono ancora perfezionare la sicurezza a lungo termine, migliorare i metodi di somministrazione e testare in animali più grandi e più simili all’uomo. Ma lo studio offre una forte prova di principio che l’editing genico attentamente mirato può silenziare in sicurezza una ripetizione tossica risparmiando geni strettamente correlati. Tale strategia potrebbe un giorno essere adattata non solo per la NIID, ma anche per altri disturbi cerebrali e muscolari causati da espansioni di ripetizioni simili.
Citazione: Xie, N., Pan, Y., Tong, H. et al. Precise excision of expanded GGC repeats in NOTCH2NLC via CRISPR/Cas9 for treating neuronal intranuclear inclusion disease. Nat Commun 17, 1683 (2026). https://doi.org/10.1038/s41467-026-68385-5
Parole chiave: Editing genico CRISPR, malattia delle inclusioni intranucleari neuronali, disturbi da espansione di ripetizioni, NOTCH2NLC, neurodegenerazione