Clear Sky Science · it
Progettazione di sintetasi del triptofano versatili mediante IA generativa basata sulla sequenza
Insegnare nuovi trucchi agli enzimi con l’IA
La società moderna si basa su molecole—medicinali, materiali e prodotti chimici speciali—spesso realizzate con processi energivori e inquinanti. I catalizzatori della natura, gli enzimi, possono svolgere lavori simili in modo pulito ed efficiente, ma trovare o costruire l’enzima giusto per un nuovo compito industriale è lento e incerto. Questo studio mostra che l’intelligenza artificiale generativa, la stessa classe di tecnologia dietro i chatbot che scrivono testo, può essere usata per progettare enzimi completamente nuovi che non solo funzionano bene in laboratorio ma talvolta superano i migliori esemplari ottenuti dall’evoluzione naturale e da anni di ingegneria.
Perché gli enzimi sono importanti nella vita quotidiana
Gli enzimi sono piccole macchine proteiche che accelerano reazioni chimiche nelle cellule viventi. I chimici hanno imparato a riutilizzarli per produrre farmaci, ingredienti alimentari e altri prodotti di valore usando meno energia e meno reagenti tossici rispetto alla chimica tradizionale. Il problema è che ogni nuova applicazione di solito richiede un enzima con prestazioni su misura—capace di accettare particolari materiali di partenza, sopravvivere alle condizioni di processo e fornire rese elevate. La «evoluzione diretta» convenzionale migliora gli enzimi creando e testando molte varianti mutate, generazione dopo generazione. Questo funziona, ma dipende da un enzima di partenza adeguato e può richiedere mesi o anni di tentativi ed errori, lasciando molte reazioni utili inesplorate.
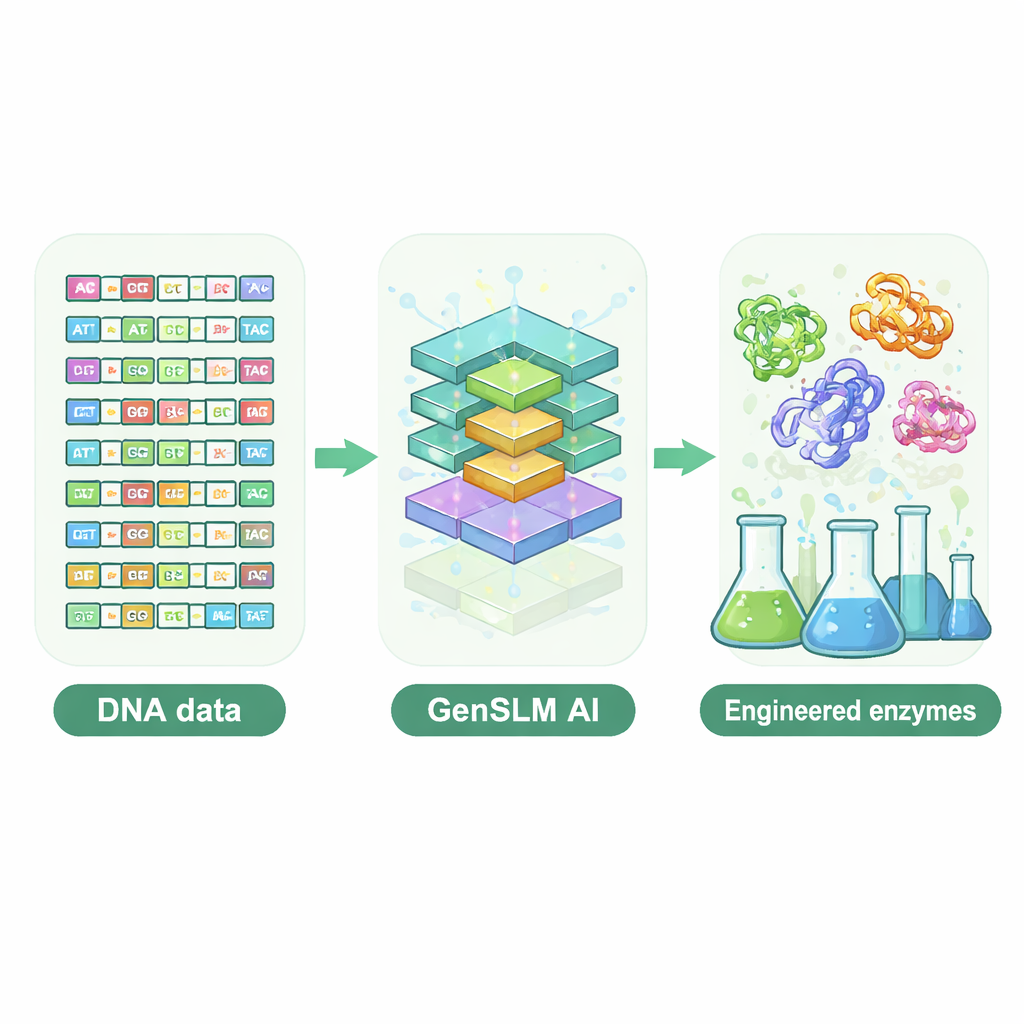
Lasciare che un modello linguistico scriva DNA
I ricercatori si sono rivolti a un modello linguistico su scala genomica chiamato GenSLM, che impara i pattern nel DNA così come un modello linguistico impara grammatica e stile nel testo. Invece di lavorare con sequenze proteiche finite, GenSLM legge e scrive DNA in codoni di tre lettere, rispecchiando il modo in cui le cellule traducono i geni in proteine. Il team ha prima messo a punto GenSLM su decine di migliaia di geni naturali per una sottounità enzimatica particolarmente complessa, chiamata TrpB, che aiuta a costruire l’amminoacido triptofano. Poi ha chiesto al modello di generare migliaia di nuovi geni trpB completamente inventati. Filtri computazionali semplici hanno eliminato sequenze troppo corte o troppo lunghe, improbabili da ripiegare correttamente o quasi identiche a enzimi naturali noti, lasciando 105 candidati diversi per i test sperimentali nei batteri.
Dai progetti al computer ai catalizzatori funzionanti
Quando questi 105 TrpB progettati dall’IA sono stati prodotti in E. coli, molti si sono ripiegati correttamente ed sono stati espressi in abbondanza. Dozzine sono state in grado di svolgere il loro compito principale: convertire indolo e l’amminoacido partner naturale, la serina, in triptofano. Alcuni hanno funzionato in modo robusto anche a temperature elevate, nonostante non fosse stato progettato esplicitamente per la resistenza al calore. In test affiancati, un sottoinsieme di GenSLM‑TrpB ha eguagliato o superato un enzima di riferimento che era stato evoluto in laboratorio per anni per funzionare autonomamente a 75 °C. Un progetto di particolare rilievo, etichettato 230, ha prodotto più triptofano di questo benchmark industriale sia a temperatura ambiente sia ad alta temperatura, dimostrando che un modello addestrato solo su dati di sequenza può raggiungere direttamente prestazioni di alto livello.
Una nuova flessibilità oltre ciò che ha costruito la natura
Il team ha poi messo alla prova gli enzimi con un paniere di substrati non naturali—derivati dell’indolo, un partner diverso simile a un alcol e un composto fluorurato usato nella produzione di farmaci. Le versioni naturali di TrpB sono di solito schizzinose: favoriscono fortemente i loro substrati nativi e mostrano poca attività su alternative di questo tipo. Sorprendentemente, gli enzimi generati dall’IA si sono spesso dimostrati più avventurosi. Per ogni substrato non naturale testato, almeno un progetto GenSLM ha mostrato attività misurabile, e molti hanno reso meglio degli enzimi naturali. Anche in questo caso, la variante 230 si è distinta, convertendo tutti e sette i substrati alternativi con rese che vanno dal modesto al quasi completo, una ampiezza di «promiscuità» non osservata prima in questa famiglia enzimatica. Tuttavia, quando i ricercatori hanno confrontato 230 con il suo parente naturale più prossimo—diverso in soli 78 su 400 residui amminoacidici—hanno scoperto che l’enzima naturale non possedeva questa versatilità nonostante la struttura complessiva e i residui chiave del sito attivo fossero quasi identici.
Cosa significa per la chimica verde del futuro
Per un non specialista, il messaggio principale è che un modello di IA addestrato solo su sequenze di DNA esistenti può immaginare enzimi nuovi e realistici che la natura non ha sperimentato, alcuni dei quali sono strumenti migliori per la chimica rispetto a quelli che usiamo attualmente. Queste varianti di TrpB progettate dall’IA mantengono la forma e la funzione essenziali dei loro cugini naturali ma acquisiscono un’abilità insolita di gestire molti materiali di partenza diversi. Questa flessibilità potrebbe ridurre drasticamente il lavoro di laboratorio necessario per scoprire vie enzimatiche verso nuovi farmaci e altri prodotti. Man mano che progettazione, sintesi del DNA e test diventano più veloci ed economici, modelli generativi simili potrebbero trasformare la scoperta di enzimi da una lunga ricerca del tesoro in un compito di progettazione rapido e di routine, contribuendo a spostare più chimica industriale verso processi più puliti e alimentati da enzimi.
Citazione: Lambert, T., Tavakoli, A., Dharuman, G. et al. Sequence-based generative AI design of versatile tryptophan synthases. Nat Commun 17, 1680 (2026). https://doi.org/10.1038/s41467-026-68384-6
Parole chiave: ingegneria degli enzimi, IA generativa, progettazione proteica, sintetasi del triptofano, biocatalisi