Clear Sky Science · it
Tmem110 regola la conformazione di TRPML1 per mantenere l’omeostasi endolisosomiale e prevenire la fuoriuscita del DNA mitocondriale e l’elaborazione patologica del DNA proprio
Perché conta il DNA fuoriuscito dopo una lesione
Quando subiamo un trauma grave, come un forte colpo alla testa, il danno non si limita al punto dell’impatto. Molti pazienti sviluppano una reazione sistemica pericolosa in cui polmoni, fegato, reni e altri organi cominciano a cedere. Questo studio mostra come piccole strutture intracellulari—lisosomi, mitocondri e sensori immunitari—comunicano tra loro per decidere se il corpo eliminerà silenziosamente i detriti o precipiterà in un attacco immunitario diretto contro se stesso. Comprendere questo sistema di pulizia nascosto potrebbe aprire nuove strade per prevenire l’insufficienza d’organo dopo un trauma e per trattare malattie autoimmuni e infiammatorie.
Dalla lesione cerebrale alla crisi sistemica
Il trauma cranico (TBI) può scatenare una potente tempesta infiammatoria chiamata sindrome da disfunzione multiorgano (MODS), ma è rimasto poco chiaro come il danno cerebrale si propaghi verso organi distanti. Gli autori si concentrano su monociti e macrofagi, cellule immunitarie che pattugliano il sangue e i tessuti e fungono da spazzini professionisti. Dopo il TBI, le cellule muoiono in modo incontrollato e rilasciano interi mitocondri—piccoli organelli energetici che contengono il proprio DNA—nella circolazione. Questo DNA mitocondriale (mtDNA) somiglia al DNA batterico per il sistema immunitario e può attivare forti difese di tipo antivirale se non viene rimosso rapidamente. Normalmente, le cellule internalizzano questi mitocondri erranti in compartimenti acidi detti lisosomi, dove enzimi degradano il DNA prima che fuoriesca nel fluido cellulare. 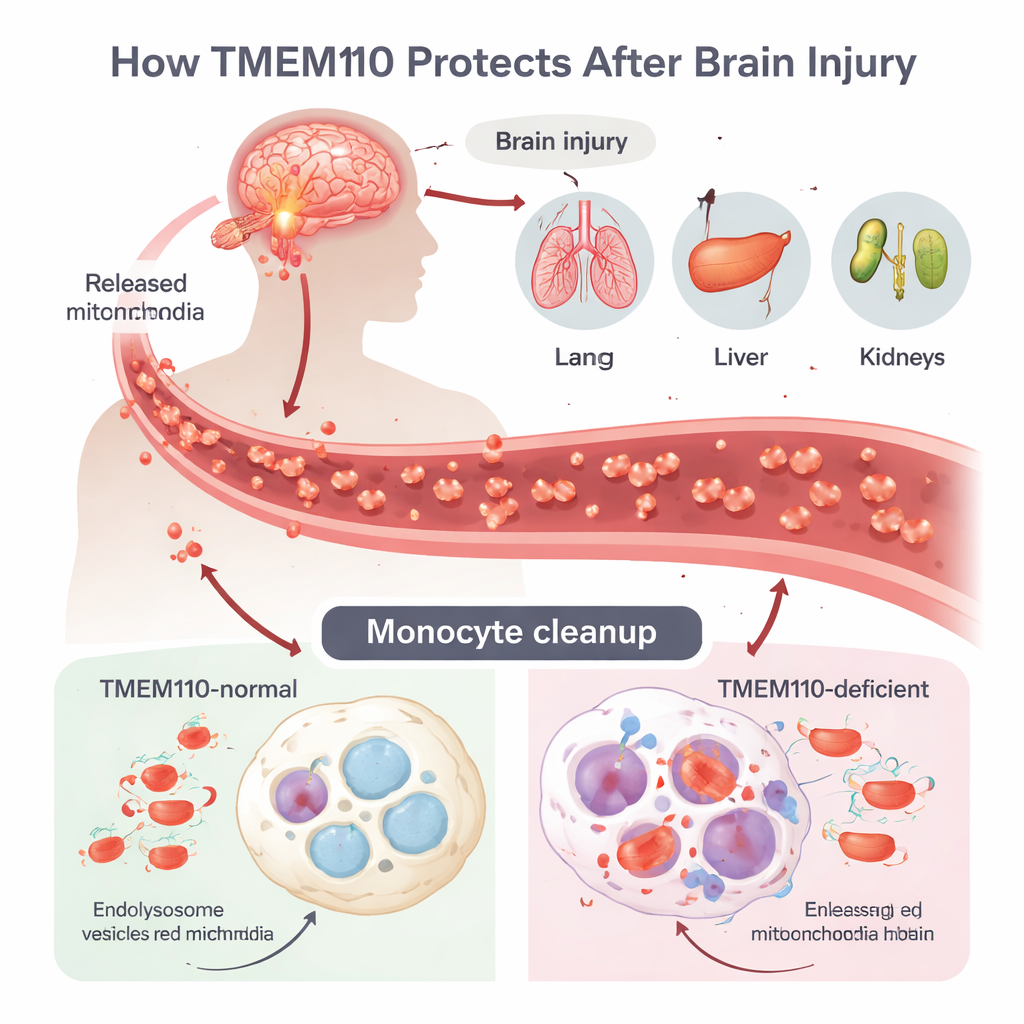
Una proteina guardiana che mantiene stabili i lisosomi
Il gruppo ha identificato TMEM110, una proteina che attraversa la membrana del reticolo endoplasmatico (un ampio network di membrane intracellulari), come un guardiano cruciale in questo processo. Utilizzando topi geneticamente modificati privi di TMEM110 solo nei monociti e nei macrofagi, hanno creato un modello controllato di lesione cerebrale. Rispetto ai topi normali, gli animali privi di TMEM110 hanno sviluppato livelli molto più alti di interferoni di tipo I—potenti molecole di segnalazione antivirale—nel sangue e nel liquido cerebrospinale. Polmoni, fegato, reni e linfonodi mostrano danni più gravi e la sopravvivenza a lungo termine dopo il TBI è risultata notevolmente peggiore. Quando i ricercatori hanno bloccato il recettore per gli interferoni di tipo I, o sostituito il midollo osseo mutante con cellule normali, i tassi di danno agli organi e di mortalità sono diminuiti, dimostrando che un’eccessiva segnalazione interferonica da parte dei monociti periferici è un motore chiave della MODS in questo contesto.
Come una gestione ionica difettosa permette la fuga del DNA
Analizzando queste cellule immunitarie dall’interno, gli autori hanno scoperto che i lisosomi privi di TMEM110 erano chimicamente squilibrati: erano meno acidi e sovraccarichi di calcio. In tali condizioni, l’enzima DNasi II—che normalmente frammenta il DNA nei lisosomi—perde attività, le membrane lisosomiali diventano fragili e il mtDNA fuoriesce nel citosol circostante. Esperimenti in vitro con monociti umani che inglobavano mitocondri donatori marcati hanno confermato che, senza TMEM110, più mtDNA perdeva nel fluido cellulare e innescava un’impennata di geni stimolati dagli interferoni. Lo studio mostra che TMEM110 agisce controllando un’altra proteina, il canale ionico lisosomiale TRPML1. Quando TMEM110 è presente, entra in contatto fisico con TRPML1 e lo sposta in una conformazione “aperta” che crea piccole aree di rilascio di calcio sulla superficie lisosomiale. Questi deflussi controllati di calcio aiutano a mantenere il giusto grado di acidità, supportano la riparazione della membrana e mantengono il mtDNA intrappolato e degradato all’interno. 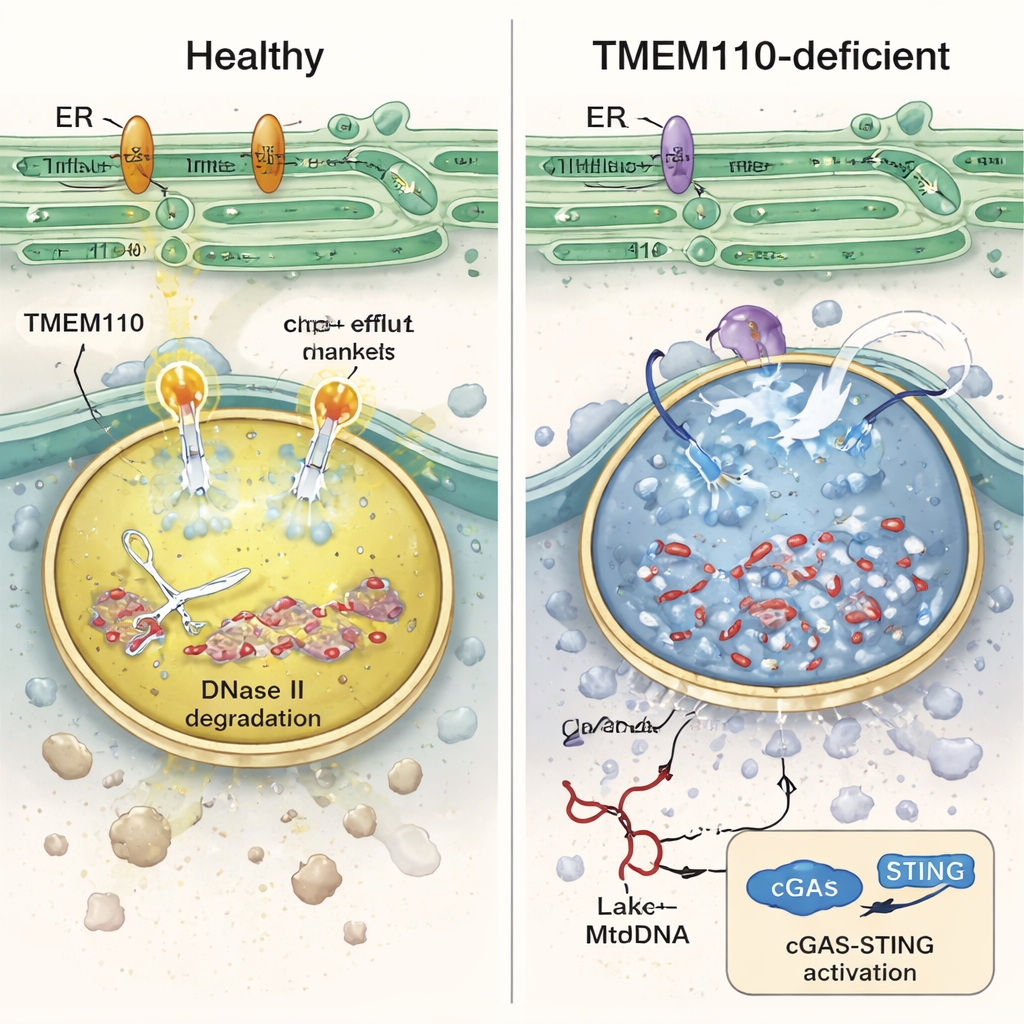
Un circuito di retroazione con l’allarme del DNA cellulare
Una volta che il mtDNA si riversa nel citosol, viene riconosciuto dalla via cGAS–STING, il principale sistema di allarme cellulare per il DNA estraneo. È interessante che TMEM110 si leghi anche a STING a riposo e lo tenga sequestrato nel reticolo endoplasmatico, prevenendo falsi allarmi. Quando il DNA citosolico si accumula, STING viene attivato e si allenta dal controllo di TMEM110. Ciò espone a sua volta una diversa regione di TMEM110 che interagisce con TRPML1 e aumenta il deflusso di calcio lisosomiale, creando un circuito di retroazione: il riconoscimento del DNA proprio attiva un meccanismo che potenzia la sua stessa pulizia. Mutazioni patologiche in STING trovate in sindromi autoinfiammatorie umane interrompono questo passaggio, intrappolando TMEM110 in uno stato inibito e contribuendo all’attivazione cronica degli interferoni. In topi portatori di una tale mutazione di STING, il TBI ha provocato danni d’organo più severi e una maggiore mortalità, ma la somministrazione di un piccolo frammento di TMEM110 ai lisosomi usando una terapia a nanoparticelle lipidiche contenenti mRNA ha parzialmente ripristinato il controllo del mtDNA e migliorato la sopravvivenza.
Indizi dai pazienti e percorsi verso nuovi trattamenti
Gli autori si sono poi rivolti a una coorte clinica di 143 persone con lesione cerebrale da trauma e MODS. I pazienti i cui monociti mostravano livelli più elevati di TMEM110 nelle fasi iniziali dopo la lesione avevano maggiori probabilità di recuperare la funzione d’organo e di sopravvivere. Coloro con TMEM110 più basso presentavano più mtDNA circolante e mitocondri decellularizzati, risposte interferoniche più intense, punteggi di insufficienza d’organo più elevati e profili autoanticorpali più ampi, inclusi anticorpi contro il DNA e proteine nucleari. Questi schemi rispecchiavano da vicino i risultati nei topi, supportando l’idea che il controllo della stabilità lisosomiale e dello smaltimento del mtDNA guidato da TMEM110 sia un meccanismo condiviso nelle malattie umane.
Cosa significa per i pazienti con traumi gravi
In termini pratici, questo lavoro suggerisce che dopo un grave trauma il nostro sistema immunitario si trova di fronte a una scelta delicata: digerire silenziosamente l’ondata di DNA proprio rilasciata dalle cellule morenti, oppure interpretarla come un’invasione virale e scatenare un attacco totale che può danneggiare i nostri organi. TMEM110, regolando un canale ionico lisosomiale e coordinandosi con il sensore del DNA STING, aiuta le cellule a scegliere la via più sicura. Quando questo sistema fallisce—per assenza di TMEM110, mutazione di STING o sovraccarico dei lisosomi—il mtDNA fuoriesce, l’allarme rimane acceso e segue danno multiorgano. Mirare a questo asse TMEM110–TRPML1–STING, per esempio con terapie mRNA mirate ai lisosomi, potrebbe offrire un nuovo modo per prevenire o trattare l’insufficienza d’organo e le complicanze di tipo autoimmune dopo traumi gravi.
Citazione: Feng, Z., Pan, Y., Zhou, J. et al. Tmem110 regulates the conformation of TRPML1 to maintain endolysosomal homeostasis and prevent mitochondrial DNA leakage and pathological self-DNA processing. Nat Commun 17, 1678 (2026). https://doi.org/10.1038/s41467-026-68382-8
Parole chiave: trauma cranico, DNA mitocondriale, lisosomi, interferone di tipo I, via cGAS‑STING