Clear Sky Science · it
Microaghi con nanomotori azionati dalla luce nel vicino infrarosso per la terapia attiva dell’acne infettata da batteri
Perché questa ricerca sull’acne è importante
L’acne viene spesso liquidata come un fastidio estetico, ma per adolescenti e adulti può essere dolorosa, lasciare cicatrici e avere un impatto emotivo. I trattamenti standard, in particolare gli antibiotici, possono causare effetti collaterali e favorire batteri resistenti ai farmaci. Questo studio descrive un cerotto a microaghi alimentato da una luce innocua nel vicino infrarosso che rilascia piccolissimi “nanomotori” direttamente nelle lesioni dell’acne. Queste particelle intelligenti generano il proprio ossigeno, si muovono attivamente attraverso gli strati di muco batterico e si riscaldano il giusto per uccidere i germi e calmare l’infiammazione—offrendo uno sguardo su una futura cura dell’acne più mirata e meno dipendente dagli antibiotici.
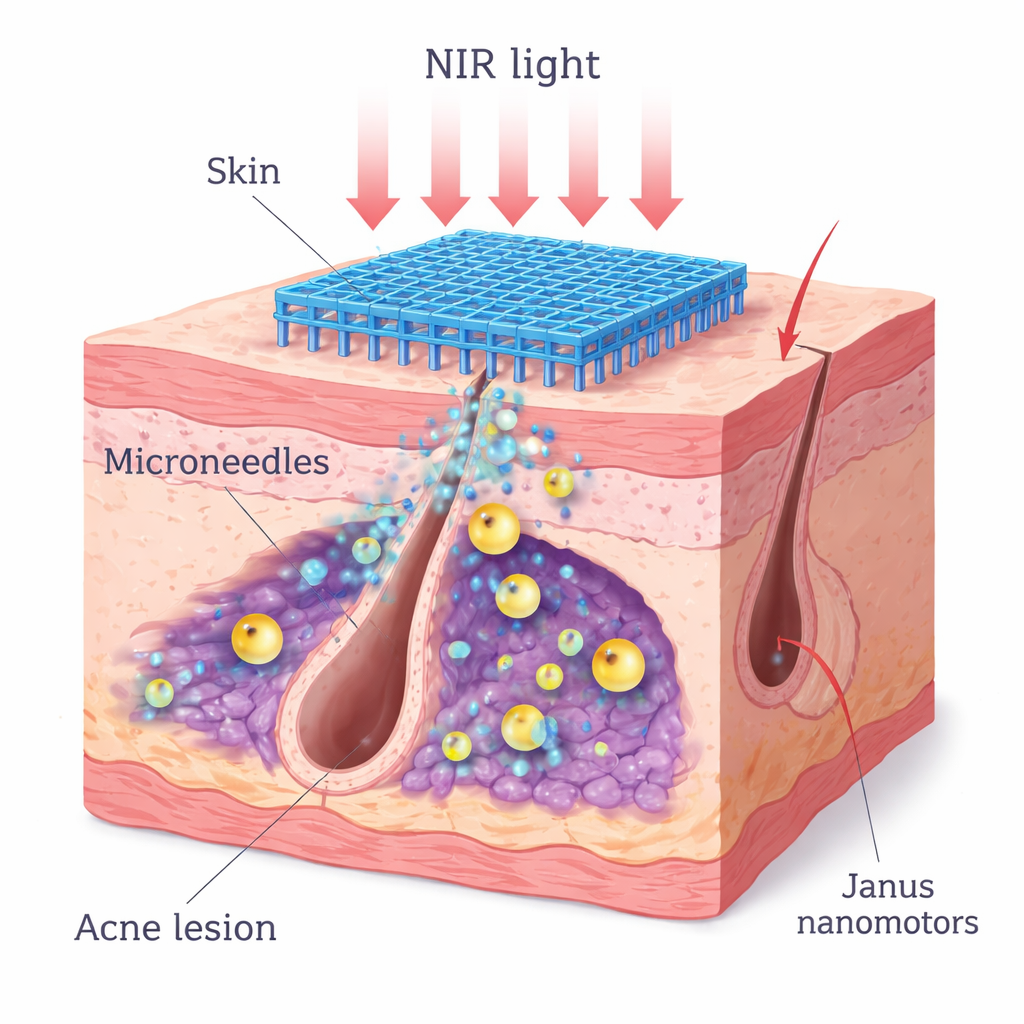
Come l’acne si trasforma in un rigonfiamento infiammato
La maggior parte dell’acne inizia quando pori e follicoli piliferi si ostruiscono con sebo e cellule morte. All’interno di questi follicoli bloccati, un batterio chiamato Cutibacterium acnes (precedentemente Propionibacterium acnes) si moltiplica in un ambiente povero di ossigeno. I microrganismi formano biofilm protettivi—comunità appiccicose avvolte in una matrice densa—che li proteggono dai farmaci. Mentre si nutrono del sebo cutaneo, rilasciano acidi grassi che riducono ulteriormente l’ossigeno e irritano le cellule vicine. La pelle risponde producendo segnali infiammatori come TNF‑α e interleuchine, e le cellule immunitarie locali che normalmente mantengono l’equilibrio microbico si esauriscono. Questi cambiamenti insieme causano arrossamento, gonfiore e talvolta cicatrici tipiche dell’acne ostinata.
Perché le creme e le pillole spesso non bastano
Creme e gel topici faticano a superare la barriera esterna della pelle, e gli antibiotici orali diffondono il farmaco in tutto l’organismo solo per raggiungere una piccola area, aumentando il rischio di effetti collaterali e ceppi resistenti. All’interno di una lesione acneica matura, il biofilm spesso attorno a C. acnes ostacola ulteriormente la penetrazione. Anche la fototermia—l’uso di particelle assorbenti di luce per produrre calore che uccide i batteri—fa fatica, perché le particelle non riescono a muoversi in profondità nel biofilm, e l’ambiente povero di ossigeno e acido intorno alla lesione alimenta un’infiammazione cronica invece della guarigione.
Un cerotto a microaghi attivato dalla luce con minuscoli motori
I ricercatori hanno progettato un cerotto a microaghi solubile che penetra indolore appena sotto la superficie cutanea e rilascia nanomotori ingegnerizzati. Ogni nanomotore ha un nucleo di perossido di zinco che si decompone lentamente in condizioni acide, rilasciando perossido di idrogeno, il quale viene poi convertito in ossigeno da un guscio di biossido di manganese. Un lato della particella è rivestito con uno strato assorbente di luce di polidopamina e biossido di manganese, creando una struttura “Janus” (bifacciale). Quando un laser nel vicino infrarosso a 808 nm illumina la pelle, questo rivestimento asimmetrico riscalda un lato più dell’altro, creando un gradiente di temperatura che spinge la particella in avanti. Questa autopropulsione aiuta i nanomotori a diffondersi attraverso biofilm densi e spazi follicolari mentre contemporaneamente erogano calore per indebolire le difese batteriche.
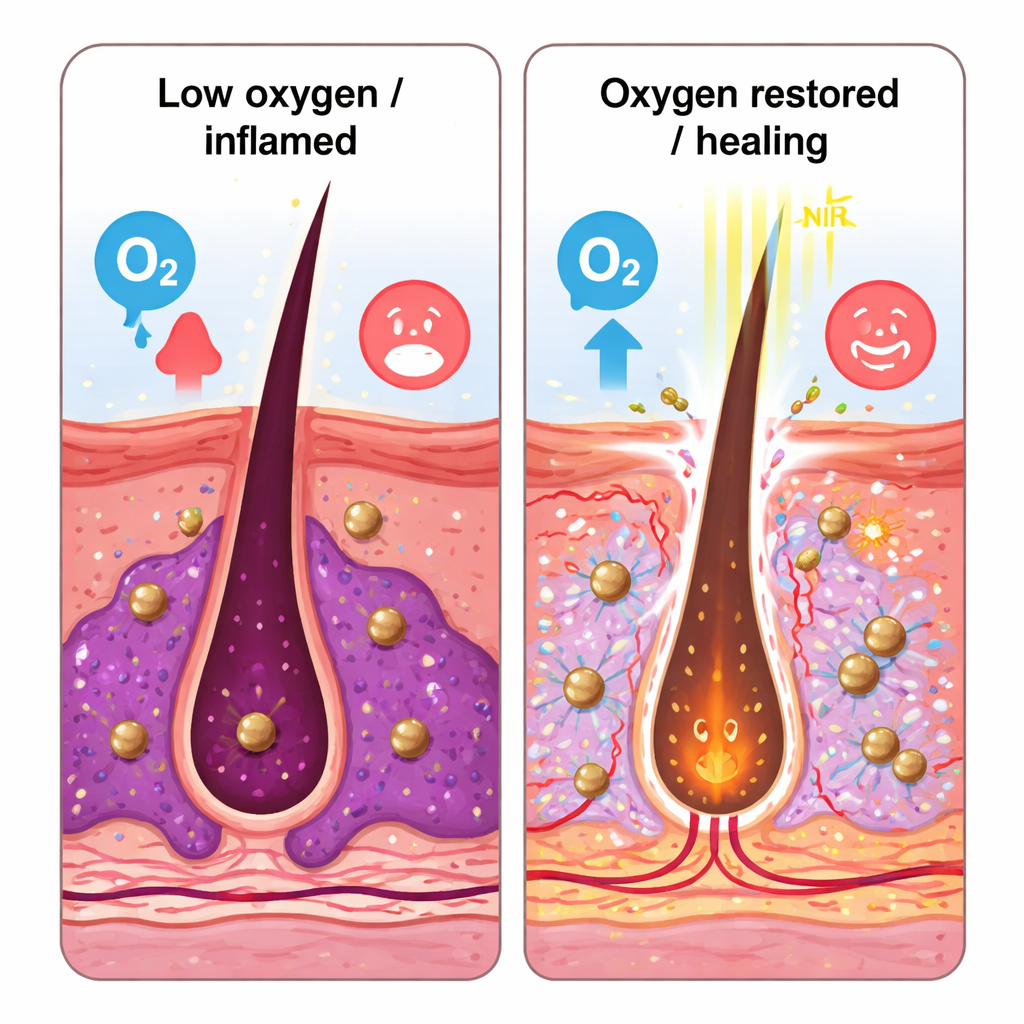
Dalla piastra di laboratorio alla pelle del topo
Nei test di laboratorio, i nanomotori si sono riscaldati in modo efficiente sotto la luce nel vicino infrarosso, sono rimasti stabili su cicli ripetuti e hanno rilasciato più perossido di idrogeno e ossigeno in condizioni acide simili al biofilm. I cerotti a microaghi realizzati con acido ialuronico compatibile con la pelle erano abbastanza resistenti da perforare la cute ma si dissolvevano in circa mezz’ora, liberando i nanomotori nel derma. Sotto il fascio luminoso, le particelle hanno mostrato un moto chiaramente aumentato e hanno penetrato più in profondità sia nei biofilm artificiali sia nella pelle di maiale. In colture batteriche di C. acnes e di Staphylococcus aureus resistente ai farmaci, la combinazione di microaghi, nanomotori e cinque minuti di esposizione nel vicino infrarosso ha ridotto la massa del biofilm e la sopravvivenza batterica di oltre il 90%, causando danni visibili alle membrane microbiche e al DNA.
Calmare l’infiammazione e ripristinare l’equilibrio
In un modello murino di acne, creato inoculando C. acnes nella pelle, il cerotto attivato dalla luce ha ridotto le dimensioni delle lesioni e il numero di batteri con efficacia paragonabile all’antibiotico eritromicina, ma senza danni tissulari evidenti. Le sezioni cutanee dei topi trattati mostravano meno cellule infiammatorie, livelli più bassi di molecole infiammatorie (IL‑6, TNF‑α) e una ridotta attività di HIF‑1α, un marcatore di ipossia. Allo stesso tempo sono aumentati i marcatori di neoangiogenesi e riparazione della ferita, e cellule immunitarie chiave chiamate ILC3, che erano state soppresse dall’infezione, sono rimbalzate tornando a produrre più fattore riparativo IL‑22. Gli autori suggeriscono che fornendo ossigeno e rompendo fisicamente i biofilm, i nanomotori aiutino a normalizzare sia il microbioma locale sia l’ambiente immunitario della pelle.
Cosa potrebbe significare per la cura futura dell’acne
Per un lettore non specialistico, il messaggio è che questo sistema microaghi‑nanomotori funziona come un trattamento intelligente e localizzato: apre delicatamente un percorso attraverso la pelle, guida minuscoli motori nel cuore della lesione acneica e, sotto un breve impulso di luce invisibile, fornisce calore e ossigeno esattamente dove servono. Nei topi, questo approccio ha eliminato l’infezione, alleviato l’infiammazione e favorito la guarigione dei tessuti, eguagliando l’efficacia degli antibiotici senza somministrare farmaci a tutto l’organismo. Sebbene siano necessari studi clinici sull’uomo e valutazioni a lungo termine della sicurezza, il lavoro indica una nuova classe di terapie per l’acne che combinano penetrazione meccanica, attivazione su richiesta e produzione autonoma di ossigeno per affrontare le infezioni basate su biofilm in modo più preciso e con meno effetti collaterali.
Citazione: Hu, Z., Gan, Y., Song, Y. et al. Near-infrared light-driven nanomotors-based microneedles for the active therapy of bacterial infected acne. Nat Commun 17, 1675 (2026). https://doi.org/10.1038/s41467-026-68376-6
Parole chiave: trattamento dell’acne, cerotto a microaghi, nanomotori, terapia nel vicino infrarosso, biofilm batterici