Clear Sky Science · it
Struttura Cryo‑EM del complesso ligasi ubiquitina umano COP1‑DET1
Come le cellule decidono quali proteine distruggere
All’interno di ogni cellula, migliaia di proteine devono essere continuamente sintetizzate, rimodellate o eliminate al momento giusto. Questo articolo esamina una delle macchine chiave di «controllo qualità» della cellula: un trituratore molecolare che decide quando rimuovere potenti regolatori genici implicati nello sviluppo e nel cancro. Rivelandone la struttura tridimensionale a dettaglio quasi atomico, gli autori mostrano come questa macchina possa alternare uno stato impilato e inattivo e una forma attiva che processa i substrati — un’intuizione che potrebbe in futuro aiutare a progettare farmaci per attivarla o inibirla.
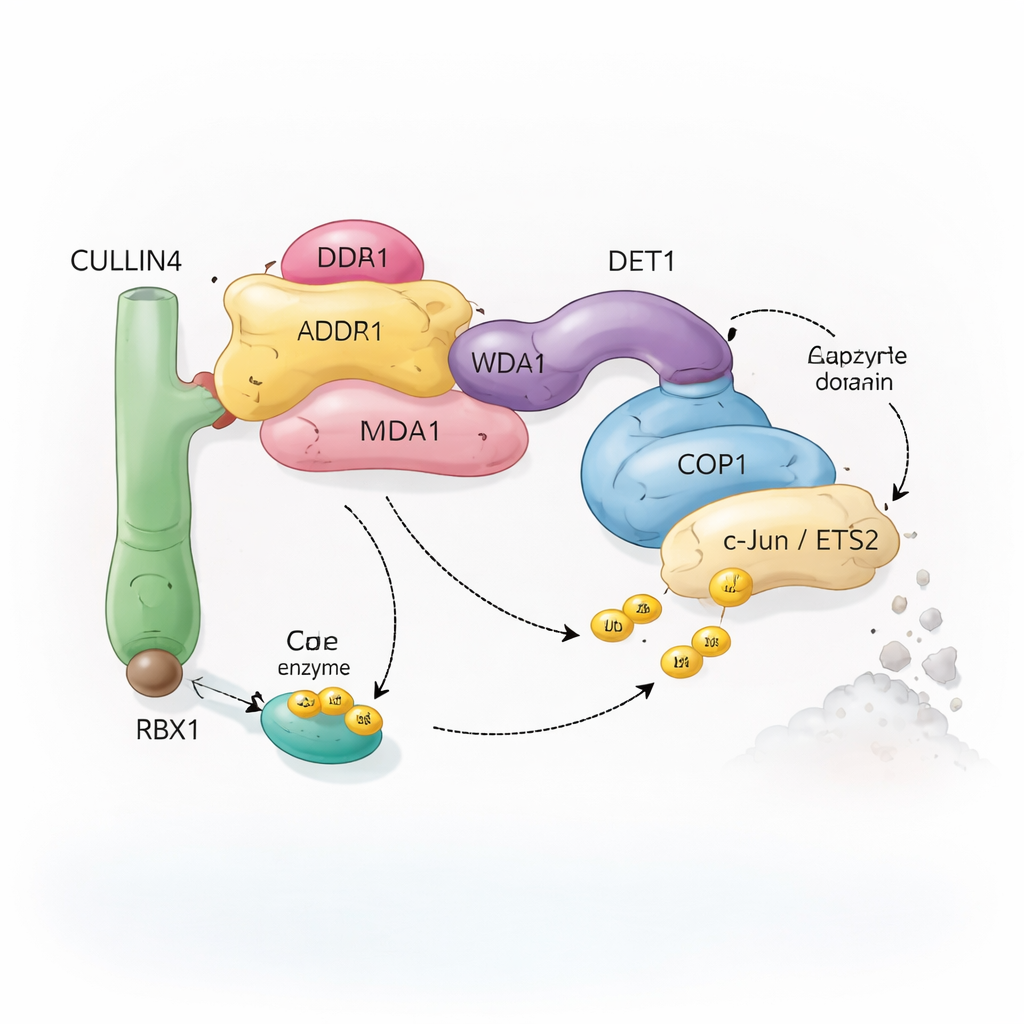
Una squadra di riciclaggio molecolare con molte componenti
Le cellule si affidano a un sistema chiamato ubiquitinazione per marcare le proteine da riciclare. Piccole molecole di ubiquitina agiscono come bandierine rimovibili che indicano alla cellula se una proteina deve essere modificata, riposizionata o distrutta. Complessi enzimatici speciali, noti come ligasi dell’ubiquitina, attaccano queste bandierine ai bersagli selezionati. Il complesso studiato qui ruota attorno a COP1, una proteina presente dalle piante agli esseri umani, che aiuta a marcare importanti fattori di trascrizione — proteine che controllano quali geni vengono attivati o repressi. COP1 non agisce da sola: può inserirsi in un assemblaggio più ampio costruito attorno a una proteina impalcatura chiamata CULLIN4, insieme a diversi adattatori denominati DDB1, DDA1 e DET1. Insieme, questi componenti formano una «squadra di riciclaggio» flessibile che riconosce specifici fattori di trascrizione come c‑Jun e ETS2, molti dei quali sono coinvolti nella crescita cellulare e nel cancro.
Catturare il complesso in 3D
Per capire come opera questa squadra, i ricercatori hanno usato la criomacroscopia elettronica a particella singola (cryo‑EM), una tecnica che raccoglie immagini di proteine vitrificate istantaneamente e ricostruisce le loro forme ad alta risoluzione. Hanno ricostituito il sistema umano COP1–DET1 in cellule coltivate, purificato i complessi e visualizzato diversi stati strutturali distinti. Per prima cosa hanno risolto la struttura del modulo DDB1–DDA1–DET1, che funge da fulcro centrale. DET1 adotta una forma insolita, in parte flessibile piuttosto che un disco rigido, con una «zampa» sporgente in grado di afferrare enzimi partner. Poi, aggiungendo COP1 e una classe di enzimi helper noti come E2, hanno catturato assemblaggi più grandi che mostrano come tutti i pezzi si incastrino, rivelando sia impilamenti compatti sia disposizioni dimeriche più aperte (due COP1).
Uno stack inattivo e un dimero attivo
Una delle scoperte più evidenti è una struttura impilata simile a un filamento composta da strati ripetuti del complesso. In ogni strato, otto molecole di COP1 si intrecciano attraverso i loro segmenti a coiled‑coil, formando un anello a forma di diamante. Le loro regioni di riconoscimento del substrato, chiamate domini WD40, sono tutte rivolte nella stessa direzione e in parte schermate dagli strati adiacenti. Questo impacchettamento stretto rappresenta verosimilmente uno stato «spento» in cui l’accesso per le proteine bersaglio è limitato. Al contrario, quando il team ha esaminato complessi co‑espressi con substrati di COP1 come c‑Jun o ETS2, ha osservato una forma dimerica diversa: due molecole di COP1 affiancate, con i domini WD40 rivolti verso l’esterno e disponibili per legare i brevi motivi «VP» presenti in molti fattori di trascrizione. Test biochimici hanno confermato che solo questo stato dimerico supporta in modo efficiente la costruzione di catene lunghe di ubiquitina su c‑Jun.
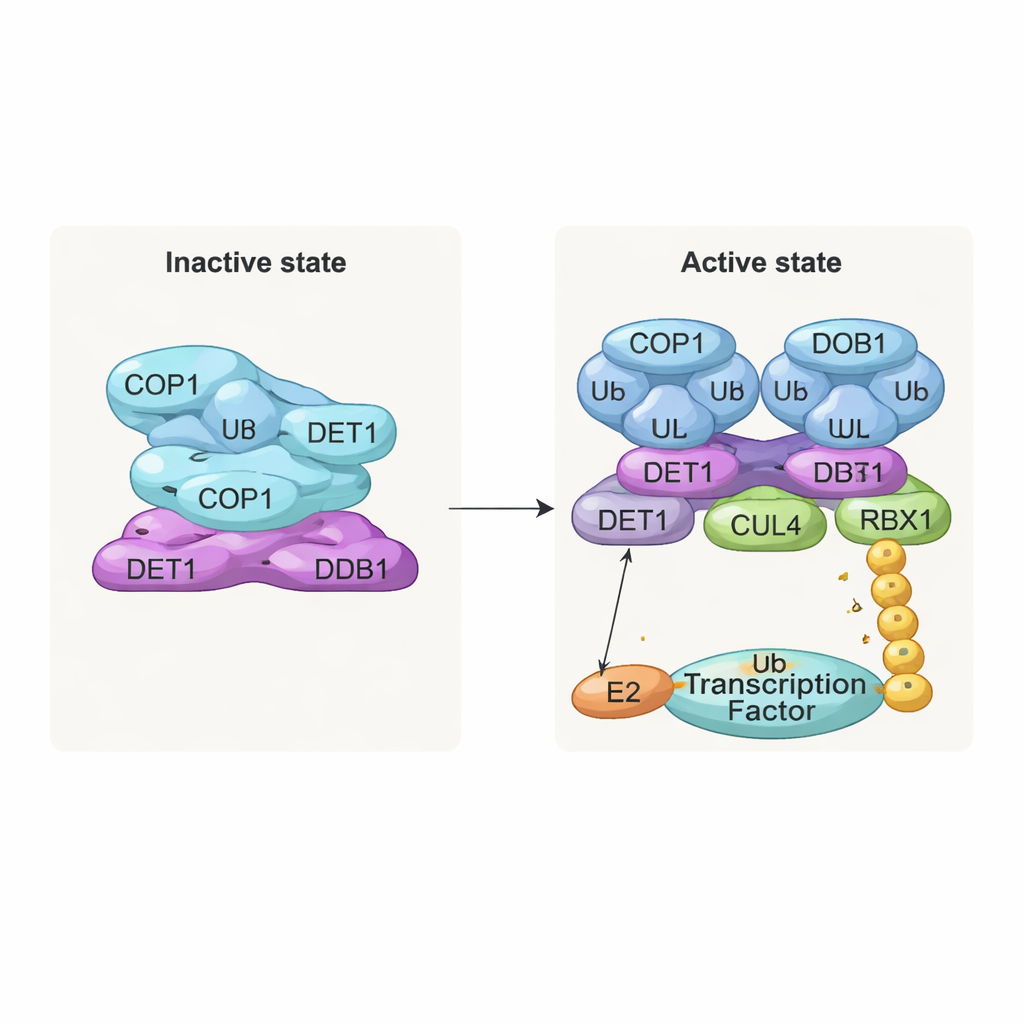
DET1 come ponte flessibile e direttore del traffico
DET1 emerge come l’organizzatore chiave che collega tutte le parti della macchina. La sua regione N‑terminal si insinua in DDB1, ancorando il complesso all’impalcatura CULLIN4, mentre la sua zona a «zampa» avvolge una famiglia di enzimi E2 chiamata Ube2e. Esperimenti dettagliati di mutazione mostrano che è DET1, non COP1, a impugnare direttamente questi E2, posizionandoli vicino alla regione catalitica RING di COP1. In questa disposizione, Ube2e pare aiutare a collocare le primissime etichette di ubiquitina sul substrato. Un secondo enzima E2, Ube2d3, viene poi richiamato tramite il braccio CULLIN4–RBX1 per estendere queste etichette in catene più lunghe che segnalano la degradazione completa. In altre parole, DET1 funge da ponte flessibile che presenta un E2 a COP1, mentre la più ampia impalcatura porta un secondo E2 a completare il lavoro.
Perché questo è importante per salute e malattia
Mappando questi stati strutturali e le loro attività, lo studio spiega come lo stesso insieme di proteine possa alternare una forma inattiva impilata e un dimero attivo che prende di mira fattori di trascrizione per la distruzione. Questo interruttore è particolarmente importante per fattori come c‑Jun, che guidano la divisione cellulare e sono strettamente collegati al cancro quando regolati in modo errato. Capire come COP1 e DET1 cooperano — come la «zampa» di DET1 seleziona specifici enzimi E2, come la superficie WD40 di COP1 riconosce substrati contenenti VP e come si forma il dimero attivo — fornisce una mappa per lavori futuri. A lungo termine, farmaci che stabilizzino lo stack inattivo o favoriscano il dimero attivo potrebbero offrire nuovi modi per modulare le vie di controllo genico nel cancro e in altre malattie in cui la degradazione proteica è alterata.
Citazione: Wang, S., Teng, F., Stjepanovic, G. et al. Cryo-EM structure of the human COP1-DET1 ubiquitin ligase complex. Nat Commun 17, 543 (2026). https://doi.org/10.1038/s41467-026-68375-7
Parole chiave: ligasi dell’ubiquitina, COP1, degradazione proteica, struttura cryo‑EM, c‑Jun